-
下列说法不正确的是( )
A. Na2O2是呼吸面具中氧气的来源
B. Na2O和Na2O2投入水中都能生成NaOH,都是氧化还原反应,它们都是碱性氧化物
C. Na2CO3可用于制玻璃、肥皂、造纸、纺织等工业,而NaHCO3可用于治疗胃酸过多,制造发酵粉等
D. NaCl的性质稳定,可用作调味品
难度: 简单查看答案及解析
-
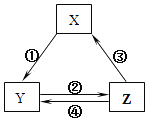
已知常温下在溶液中可发生如下两个离子反应:Ce4++Fe2+=Fe3++Ce3+,Sn2++2Fe3+=2Fe2++Sn4+,由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是 ( )
A.Sn2+ 、Fe2+、Ce3+ B.Sn2+、Ce3+、Fe2+
C.Ce3+、Fe2+ 、Sn2+ D.Fe2+、Sn2+、Ce3+
难度: 中等查看答案及解析
-
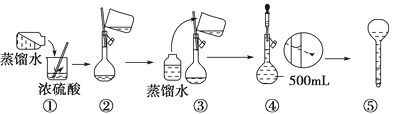
用98%的浓硫酸(密度为1.84 g·cm-3)配制80 mL 1 mol·L-1的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒 ⑧80 mL容量瓶 按使用仪器的先后顺序排列正确的是( )
A.④③⑦⑧⑥ B.②⑤⑦⑥
C.①③⑧⑥⑦ D.②⑥③⑦⑤⑥
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是( S-32 O-16 )
A.标准状况下,22.4L氦气含有2NA个氦原子
B.在常温常压下,11.2L Cl2含有的分子数为0.5NA
C.常温常压下,64g SO2中含有的氧原子数为2NA
D.标准状况下,11.2LH2O含有的分子数为0.5NA
难度: 简单查看答案及解析
-
下列实验操作与安全事故处理错误的是
A. 使用水银温度计测量烧杯中的水的温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残破的温度计插入装有硫粉的广口瓶中
B. 试管夹从试管底由下往上夹住试管口约
处,手持试管夹长柄末端进行加热
C. 燃着的酒精灯翻倒,酒精洒到桌面并且燃烧,为了人身安全,应立即撤离现场
D. 将玻璃管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻璃管插入端并缓慢旋进塞孔中
难度: 中等查看答案及解析
-
为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装了盛有Na2O2(或K2O2)颗粒的装置,它的用途是产生氧气。下列有关Na2O2的叙述正确的是
A.Na2O2中阴、阳离子的个数比是1∶1
B.Na2O2分别与水及CO2反应产生相同量氧气时,需水和CO2的质量相等
C.Na2O2的漂白原理与SO2的漂白原理相同
D.与CO2、H2O反应产生等量氧气,转移电子数相同,耗Na2O2的质量相同
难度: 中等查看答案及解析
-
对下列事实的解释错误的是()
A.氨溶于水的喷泉实验,说明氨气极易溶于水
B.常温下,浓硝酸可用铝罐来贮存,说明浓硝酸具有强氧化性
C.向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有吸水性
D.氯气可使湿润的红色布条褪色,而不能使干燥的有色布条褪色,说明次氯酸具有漂白性
难度: 简单查看答案及解析
-
现有下列几个离子反应:
① Cr2O
+14H++6Cl-===2Cr3++3Cl2↑+7H2O
② 2Fe2++Br2===2Fe3++2Br- ③ 2Br-+Cl2=== Br2+2Cl-
④ 2Fe3++SO2+2H2O===2Fe2++SO
+4H+
下列有关性质的比较中正确的是( )。
A. 氧化性:Cr2O
>Cl2>Fe3+ B. 氧化性:Cl2>Br2>Cr2O
C. 还原性:SO2<Fe2+<Br- D. 还原性:Cl->Cr3+>Fe2+
难度: 中等查看答案及解析
-
下列实验操作对应的实验现象及解释或结论都正确的是
选项
实验操作
实验现象
解释或结论
A
用某无色溶液进行焰色反应
透过钴玻璃,火焰呈紫色
原溶液一定是钾盐溶液
B
向NaOH溶液中滴加足量的MgCl2溶液,然后再滴加足量的CuCl2溶液
先产生白色沉淀,然后沉淀变成蓝色
Ksp[Cu(OH)2]sp[Mg(OH)2]
C
将水蒸气通过灼热的铁粉
粉末变红
铁与水蒸气在高温下发生反应
D
将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液
有气体生成,溶液呈红色
稀硝酸将Fe氧化为Fe3+
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
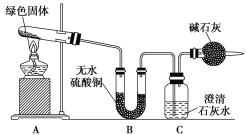
某实验小组通过下图所示实验探究Na2O2与水的反应:
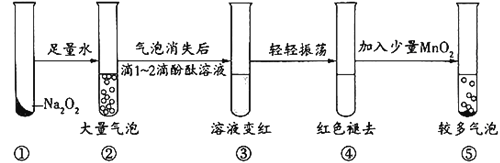
下列说法不正确的是
A.②中的大量气泡主要成分是氧气
B.③中溶液变红,说明有碱性物质生成
C.④中现象可能是由于溶液中含有强氧化性物质造成的
D.⑤中MnO2的主要作用是降低了水中氧气的溶解度
难度: 中等查看答案及解析
-
NaNO2像食盐一样有咸味,有很强的毒性,误食亚硝酸钠(NaNO2)会使人中毒。已知亚硝酸钠能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O。下列说法正确的是( )
A.该反应的氧化剂为HI
B.反应产物中能使淀粉变蓝的物质有I2、NaI
C.该反应中氧化剂与还原剂物质的量之比为1:1
D.人误食亚硝酸钠中毒时,可以服用HI溶液解毒
难度: 中等查看答案及解析
-
下列关于分散系的叙述不正确的是( )

A. 分散系的分类:

B. 用平行光照射FeCl3溶液和Fe(OH)3胶体,可以加以区分
C. 把FeCl3饱和溶液滴入到氢氧化钠溶液中,以制取Fe(OH)3胶体
D. 如图显示的是树林的晨曦,该现象与丁达尔效应有关
难度: 简单查看答案及解析
-
右图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是

A.该硫酸试剂的物质的量浓度为18.4 mol/L
B.稀释该硫酸时应把水倒入硫酸中,边倒边搅拌
C.50 mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46 mol
D.标准状况下2.7 g Al与足量的该硫酸反应可得到H23.36 L
难度: 简单查看答案及解析
-
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO
的物质的量浓度之比为1∶3,则Cl2与NaOH溶液反应时,被还原的氯元素与被氧化的氯元素的物质的量之比为
A.21∶5 B.11∶3 C.3∶1 D.4∶1
难度: 中等查看答案及解析
-
下列有关氢氧化铁胶体说法正确的是
A.将外加直流电源通过该胶体,阴极处颜色变深,则说明该胶体带正电荷
B.鉴别FeCl3溶液和Fe(OH)3胶体,可用利用丁达尔效应
C.采用过滤,可将Fe(OH)3胶体中的FeCl3杂质除去
D.向Fe(OH)3胶体中加入大量盐酸,则最终可引起胶体聚沉
难度: 简单查看答案及解析