-
下列关于“尖上的化学”说法正确的是
A.为了预防缺碘性疾病,每天都要食用大量的加碘盐
B.为了满足人体对维生素的需求,唯一的途径是食用大量蔬菜、水果
C.为了延长食品保质期,可在食品中添加适量的防腐剂
D.为了防止水产品腐烂,可用适量的甲醛(福尔马林)溶液浸泡
难度: 简单查看答案及解析
-
组成和结构决定性质。下列是小江同学总结的有关结构与性质的关系,其中错误的是
A.CO和CO2化学性质不同的原因是由于它们的分子构成不同
B.金刚石和石墨物理性质不同的原因是它们的碳原子排列方式不同
C.酸类物质具有相似化学性质的原因是不同的酸溶液中都含有相同的H+
D.钠原子与氯原子化学性质不同的原因是它们原子核外电子数不同
难度: 简单查看答案及解析
-
下列离子能在pH = 12的水溶液中大量共存的是
A.SO42-、NO3-、K+、H+ B.Na+、Cl-、OH-、Al3+
C.Cl-、NO3-、K+、Na+ D.Ag+、Cl-、CO32-、K+
难度: 困难查看答案及解析
-
鉴别下列各组物质,所用三组试剂均正确的是( )
待鉴别的物质
鉴别试剂1
鉴别试剂2
鉴别试剂3
A
稀盐酸和稀硫酸
氯化钡溶液
碳酸钠溶液
氧化铜
B
氯化铵和氯化钙
硝酸银溶液
熟石灰
碳酸钠溶液
C
硝酸铵固体和氢氧化钠固体
熟石灰
水
硝酸铜溶液
D
氧气、二氧化碳、氢气
燃着的木条
澄清石灰水
水
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
除去食盐溶液中的Na2SO4和CaCl2杂质的操作有:①加入过量BaCl2溶液;②过滤;③加入适量盐酸;④蒸发结晶;⑤加入过量Na2CO3溶液,正确的操作顺序是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列物质间的转化,在一定条件下均能一步实现的是( )
①C→CO→CO2
②Al→Al2O3→AlCl3
③Na2CO3→NaCl→NaNO3
④CaCO3→CaO→Ca(OH)2
A. ①②③ B. ①③④ C. ①②④ D. ①②③④
难度: 困难查看答案及解析
-
La(镧)是一种活动性比锌强的金属元素,其氧化物为La2O3,对应的碱La(OH)3,难溶于水,而LaCl3、La(NH3)3都易溶于水,下列各组物质中,不能直接反应生成LaCl3的是( )
A.La+HCl B.La2O3+HCl C.La(OH)3+HCl D.BaCl2+La(NO3)3
难度: 简单查看答案及解析
-
若向NaOH和Na2CO3的混合溶液中逐滴加入过量稀盐酸,下列图象正确的是( )
A.
 B.
B. C.
C.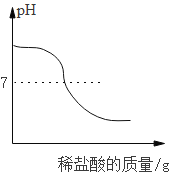 D.
D.
难度: 中等查看答案及解析
-
有一包白色粉末,可能由氯化钠、硫酸钠、硫酸铜、碳酸钠、碳酸钙中的一种或几种组成,为确定其组成,进行如下实验:
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A。
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得到无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为
。
③在
白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出。
④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀。
由上述实验得出的下列判断,正确的是( )
A.白色粉末中不含碳酸钙、硫酸钠、硫酸铜 B.无色溶液B中一定含有一种溶质
C.白色粉末中一定含有氯化钠 D.步骤③生成的气体质量可能是
难度: 困难查看答案及解析
-
氯化钡是一种可溶性重金属盐,广泛应用于化工领域,用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如下:下列说法不正确的是
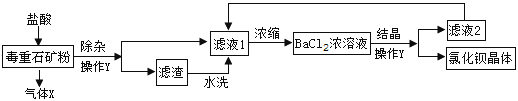
A. 气体X是二氧化碳 B. 工艺流程中氯化钡溶液可以循环利用
C. 操作Y的名称是过滤 D. 室温下洗涤氯化钡晶体可选用饱和氯化钠溶液
难度: 困难查看答案及解析