-
纳米铁粉在空气中能自燃并生成一种红色氧化物。对比铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧的事实,某同学得出的下列结论不正确的是
A. 纳米铁粉在空气中自燃的产物不是四氧化三铁
B. 相同的反应物在不同条件下生成物可能不同
C. 有些物质燃烧时温度不需要达到着火点
D. 反应物间的接触面积大小是反应能否发生的因素之一
难度: 中等查看答案及解析
-
描述物质变化的成语有:①滴水成冰;②死灰复燃;③木已成舟;④火烧赤壁;⑤沙里淘金;⑥火上浇油;⑦百炼成钢;⑧花香四溢;⑨玉石俱焚,其中属于化学变化的是
A.②③④⑤⑥⑦ B.④⑤⑥⑦⑨ C.①③④⑤⑧⑨ D.②④⑥⑦⑨
难度: 简单查看答案及解析
-
下列物质的用途与性质对应关系错误的是
A.熟石灰可用来改良酸性土壤——熟石灰呈碱性
B.金刚石能裁玻璃——金刚石是硬度最大的金属
C.氮气常用作保护气——氮气化学性质不活泼
D.稀盐酸用来除锈——稀盐酸能与某些金属氧化物反应
难度: 简单查看答案及解析
-
正确的实验操作是科学探究成功的基础。下列操作中正确的是
A.
取用少量液体 B.
 过滤 C.
过滤 C. 闻气味 D.
闻气味 D.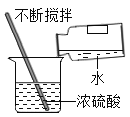 稀释浓硫酸
稀释浓硫酸难度: 简单查看答案及解析
-
下列实验现象描述正确的是
A.打开浓盐酸、浓硫酸的试剂瓶,瓶口都看到白雾
B.灼烧鸡蛋清,产生烧焦羽毛的特殊气味
C.硫在氧气中燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的二氧化硫气体
D.实验室电解水,正负极产生的气体体积比约为2∶1
难度: 简单查看答案及解析
-
“宏观辨识与微观探析”是化学学科的核心素养之一。对下列事实或做法的解释正确的是
A.铁质水龙头表面镀铬可防锈——改变了金属的内部结构
B.伍德合金可作为保险丝——合金的熔点比其组成金属高
C.用明矾净水——明矾可降低水中钙、镁离子的含量
D.氧气能被液化贮存于钢瓶——分子间有间隔且间隔能改变
难度: 简单查看答案及解析
-
从6月1日起,国内所有的超市、商场等商品零售场所开始实行塑料购物袋有偿使用制度,这将有助于减少因使用不可降解塑料引起的“白色污染”。很多包装袋是由聚氯乙烯塑料(PVC)加工而成的,其分子可表示为-[ClCHCH2]n-, 可看作由n个ClCHCH2 (氯乙烯)连接而成,是一种不可降解塑料。下列有关聚氯乙烯的说法,不正确的是
A.相对分子质量为62.5n B.在长时间光照下可以分解
C.它属于有机合成材料 D.氢元素的质量质量分数最小
难度: 简单查看答案及解析
-
下列有关碳和碳氧化物的说法中,错误的是
A.古代用墨书写或绘制的字画长久不变色,是因为在常温下碳的化学性质不活泼
B.金刚石和石墨物理性质不同,是因为它们的碳原子排列方式不同
C.用煤火取暖时应注意通风,防止一氧化碳中毒
D.二氧化碳的排放是导致酸雨的原因之一
难度: 简单查看答案及解析
-
研发高性能“中国芯”是我国信息产业的当务之急。“中国芯”的主要材料是高纯度的单质硅,工业上用SiO2+2C
Si+2CO↑来制取粗硅,下列说法正确的是
A.生成CO的原因是O2不足 B.该反应体现了CO的还原性
C.该反应为置换反应 D.硅元素在地壳中的含量比氧元素多
难度: 简单查看答案及解析
-
推理是学习化学的一种重要方法,下列推理合理的是
A.化学变化中分子种类发生改变,则分子种类发生改变的变化一定是化学变化
B.离子是带电荷的粒子,则带电荷的粒子一定是离子
C.单质是由同种元素组成的物质,则只含一种元素的物质一定是单质
D.元素是指具有相同质子数的一类原子的总称,则具有相同质子数的粒子一定是同种元素
难度: 简单查看答案及解析
-
下列实验设计能达到实验目的的是( )
选项
实验目的
实验方案
A
除去氧化钙中少量的碳酸钙
加水溶解、过滤
B
检验碳酸钠溶液中是含有氯化钠
加过量的稀盐酸后,再滴加硝酸银溶液
C
鉴别Fe、CuO、C 三种固体粉末
滴加稀硫酸
D
分离CO2和CO
将气体通过盛有足量NaOH溶液的洗气瓶
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
(资料获悉)铁在高温条件下与氧化铜反应:
;铜在氯化铁溶液中发生反应:
;铁在氯化铁溶液中发生反应:
。
一定质量的铁与氧化铜的混合物,在高温条件下恰好完全反应。将反应后的固体粉末倒入盛有足量稀盐酸的烧杯中,振荡,充分反应后静置,然后从烧杯中取适量溶液(表示为“甲”)于试管中并加入一定质量的锌粉,充分反应后过滤,得到滤液乙和固体丙。下列判断正确的是( )
①甲中不含FeCl3 ②甲中含有FeCl3 ③若向固体丙加稀盐酸无明显现象,则滤液乙中一定含有ZnCl2、FeCl2,可能含有CuCl2 ④若向固体丙加稀盐酸有气体产生,则固体丙中一定含有锌和铜
A.①③ B.②③ C.①④ D.②④
难度: 困难查看答案及解析




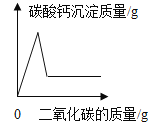 B
B 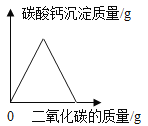 C
C