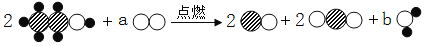-
下列离子在溶液中能大量共存,并形成无色透明溶液的是的是( )
A.H+、NO3﹣、CO32﹣ B.K+、Na+、SO42﹣
C.NH4+、OH﹣、SO42﹣ D.Fe3+、H+、Cl﹣
难度: 中等查看答案及解析
-
水是生命之源。下列“水”属于纯净物的是( )
A. 海水 B. 蒸馏水 C. 矿泉水 D. 雨水
难度: 简单查看答案及解析
-
预防新冠病毒的日常措施中涉及化学变化的是( )
A.少聚集 B.多通风 C.带口罩 D.勤消毒
难度: 简单查看答案及解析
-
下列材料中属于复合材料的是( )
A.聚乙烯 B.合金 C.玻璃钢 D.钢铁
难度: 简单查看答案及解析
-
下列有关营养成分与人体健康关系叙述中,不正确的是
A.缺氟元素会得龋齿
B.缺碘或碘过量均会导致甲状腺疾病
C.铁、钙、硒等都是人体必需的微量元素
D.缺维生素A会引起夜盲症
难度: 简单查看答案及解析
-
下列食品中能为人类提供大量蛋白质的是( )
A.鸡蛋 B.米饭 C.黄瓜 D.菜油
难度: 简单查看答案及解析
-
从安全角度考虑,下列做法不正确的是( )
A.家用电器着火时,立即浇水灭火 B.炒菜时油锅着火,立即把锅盖盖上
C.酒精灯着火,立即用湿布盖灭 D.浓硫酸滴到皮肤上,立即用大量水冲洗
难度: 中等查看答案及解析
-
下列标识,与消防安全无关的是
A.
 B.
B. C.
C. D.
D.
难度: 简单查看答案及解析
-
能保持氢气化学性质的微粒是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
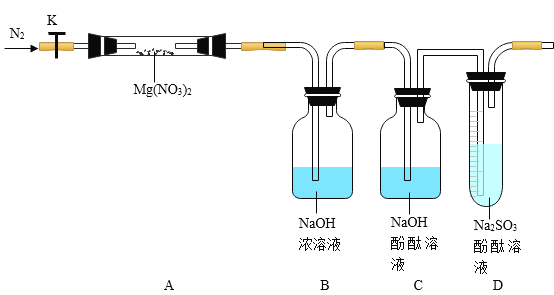
化学试剂常因与空气中的一些成分作用而发生变化.对下列试剂在空气中发生变化的分析错误的是
A.浓盐酸变稀与空气中的水蒸气有关 B.氢氧化钠溶液变质与空气中二氧化碳有关
C.铁钉生锈与空气中的水蒸气和氧气有关 D.氧化钙的变质与空气中的水和二氧化碳有关
难度: 中等查看答案及解析
-
下图所示基本操作正确的是( )
A.
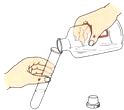 倾倒液体 B.
倾倒液体 B. 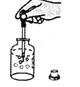 吸取液体
吸取液体C.
量取液体 D.
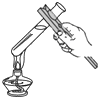 加热液体
加热液体难度: 简单查看答案及解析
-
下列有关实验现象的描述,错误的是( )
A.铁丝在氧气中剧烈燃烧时,火星四射,生成黑色固体
B.分别点燃一小团棉花和羊毛,都产生了烧焦羽毛的气味
C.打开盛有浓盐酸的试剂瓶瓶盖,瓶口出现白雾
D.打磨后的铝丝放入硫酸铜溶液中,铝丝表面有红色物质析出
难度: 简单查看答案及解析
-
烟花爆竹中黑火药爆炸的化学方程式:
,下列说法正确的是
A.X的化学式为K2SO4
B.该反应过程中共有2种氧化物
C.燃放烟花爆竹时闻到刺激性气味,说明微粒在不断运动
D.黑火药配方是一硫二硝三木炭,其中的“一、二、三”是各成分质量比
难度: 简单查看答案及解析
-
不法分子常用“金元宝”(铜锌合金)蒙骗人们,下列方法不可用于鉴别真假金元宝的是
A.测密度 B.在火焰上灼烧 C.滴加稀盐酸 D.看颜色
难度: 简单查看答案及解析
-
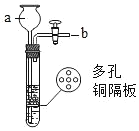
如图所示,试管中盛有某种液体,将气球中的某种固体小心的倒入试管中,能观察到气球先变大后复原的一组物质是( )
A.氯化钠和水 B.铁粉和稀硫酸
C.氢氧化钠和水 D.二氧化锰和过氧化氢溶液
难度: 困难查看答案及解析
-
已知 KNO3的溶解度如下表所示,下列说法不正确的是
温度/℃
10
20
30
40
50
60
70
溶解度/g
20.9
31.6
45.8
63.9
85.5
110
138
A.在 10℃-70℃之间,随着温度的升高,KNO3的溶解度增大
B.20℃时,向 100 g 水中加入 35 g KNO3,充分搅拌,所得溶液质量为 131.6 g
C.将 70℃时不饱和的 KNO3溶液降低温度,有可能转化为饱和溶液
D.50℃时,饱和 KNO3溶液中溶质的质量分数为 85.5%
难度: 中等查看答案及解析
-
用足量含杂质的食盐(杂质不溶于水),配制成w g a%的食盐溶液,实验操作有:①称量;②过滤;③蒸发结晶;④计算;⑤溶解;⑥干燥。正确顺序是( )
A.④①⑤②③⑥⑤ B.③④②③①⑥⑤ C.⑤②③⑥④①⑤ D.④①⑤③⑥①⑤
难度: 简单查看答案及解析
-
如表实验方法一定能达到实验目的的是()
选项
实验目的
实验方法
A
鉴别氢氧化钠溶液和稀硫酸
加入适量的稀盐酸
B
鉴别一氧化碳和甲烷
用燃着的小木条
C
鉴别奶粉和面粉
看颜色
D
检验某矿石中是否含碳酸盐
加入足量的稀盐酸,若产生气体再将气体通入澄清石灰水
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
已知在一定条件下发生反应:甲+乙→丙+丁,下列判断不正确的是( )
A.甲、乙、丙、丁可能含有同一种元素
B.丙为盐、丁为水,则该反应不一定为复分解反应
C.若甲、乙为化合物,则该反应一定为复分解反应
D.若甲、丙为单质,则该反应可能为置换反应
难度: 困难查看答案及解析
-
将10g氧化铜粉末加入到100g一定质量分数的稀硫酸中,微热到氧化铜全部溶解,再向溶液中加入ag铁粉,使溶液中的溶质完全反应后,过滤,将滤渣在低温下烘干,得到干燥固体质量仍然为ag,下列分析不正确的是
A. 稀硫酸中溶质质量分数为12.25%
B. 滤渣中一定含有铜,可能含有铁
C. 加入铁粉后有红色固体产生,还有少量气泡产生
D. a的取值范围:a≥8
难度: 困难查看答案及解析