-
下列实验操作:①用50 mL量筒量取5 mL蒸馏水;②称量没有腐蚀性的固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要立即用大量水冲洗;④倾倒液体时试剂不对准容器口;⑤块状药品都要用药匙取用;⑥固体药品用细口瓶保存。其中错误的是
A. ①②③ B. ③④ C. ②⑤⑥ D. ①②③④⑤⑥
难度: 中等查看答案及解析
-
下列实验仪器不宜直接用来加热的是( )
A.试管 B.坩埚 C.蒸发皿 D.烧杯
难度: 简单查看答案及解析
-
下列实验操作中正确的是 ( )
A. 蒸发操作时,应使混合物中的水分完全蒸干后才能停止加热
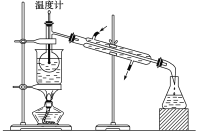
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出后,再将上层液体从下口放出到另一个烧杯
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
难度: 简单查看答案及解析
-
用CuSO4·5H2O配制0.1 mol/LCuSO4水溶液,下面所列的方法正确的是( )
A.取25 g CuSO4·5H2O溶于1 L水中
B.将CuSO4·5H2O干燥去掉结晶水,取16 g溶于水制成1 L溶液
C.将25 g CuSO4·5H2O溶于水制成1 L溶液
D.取12.5 g CuSO4·5H2O溶于500 mL水中
难度: 简单查看答案及解析
-
在过滤操作中,除了使用铁架台、烧杯、玻璃棒外,还需要用到的仪器是( )
A.漏斗 B.蒸发皿 C.酒精灯 D.天平
难度: 简单查看答案及解析
-
在盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的( )
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是( )
A.②③④ B.②③ C.①②④ D.①②③④
难度: 简单查看答案及解析
-
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序是 ( )
A.⑤②④③① B.④①②⑤③
C.②⑤④①③ D.①④②⑤③
难度: 简单查看答案及解析
-
下列对于“摩尔”的理解正确的是 ( )
A. 1 mol任何物质所含有的原子数都相同
B. 摩尔是物质的量的单位,简称摩,符号为mol
C. 摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D. 国际上规定,0.012 kg C中所含有的碳原子数目为1摩
难度: 中等查看答案及解析
-
x g H2O中含有y个氢原子,则阿伏加德罗常数为 ( )
A.9x/y mol-1 B.9y/x mol-1
C.x/y mol-1 D.y/x mol-1
难度: 简单查看答案及解析
-
设NA代表阿伏加德罗常数的值。下列说法正确的是( )
A. 2.4 g金属镁变成镁离子时失去的电子数目为0.1NA
B. 18 g水中含有0.1NA个水分子
C. 1 mol氮气所含的电子数目为NA
D. 17 g氨气所含电子数目为10NA
难度: 简单查看答案及解析
-
下列说法正确的是 ( )
A.镁原子的质量就是镁的相对原子质量
B.一个氧原子的实际质量约等于
g
C.水的相对分子质量等于18 g
D.二氧化硫的摩尔质量是64 g
难度: 简单查看答案及解析
-
将溶质的质量分数为14%的KOH溶液加热蒸发掉100 g水后,得到溶质的质量分数为28%的溶液80 mL,此时溶液的物质的量浓度为( )
A.5 mol·L-1 B.6.25 mol·L-1
C.7 mol·L-1 D.6.75 mol·L-1
难度: 中等查看答案及解析
-
将5mol·L-1盐酸10mL稀释到200mL,再取出5mL,这5mL溶液的物质的量浓度是( )
A. 0.05mol·L-1 B. 0.25mol·L-1 C. 0.1mol·L-1 D. 0.5mol·L-1
难度: 中等查看答案及解析
-
在标准状况下,由0.5gH2、11g CO2和4g O2组成的混合气体,其体积约为
A.8.4L B.11.2L C.14.0L D.16.8L
难度: 中等查看答案及解析
-
如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(式中NA为阿伏加德罗常数的值) ( )
A.
L B.
L C.
L D.
L
难度: 中等查看答案及解析
-
在两个密闭容器中,分别充有质量相等的甲乙两种气体。若两容器的温度和压强均相等,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多 B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小 D.甲的相对分子质量比乙的相对分子质量小
难度: 简单查看答案及解析
-
等体积硫酸铝、硫酸锌、硫酸钠溶液分别与足量的氯化钡溶液反应。若生成的硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐溶液的物质的量浓度比为( )
A.1:2:3 B.1:6:9 C.1:3:3 D.1:3:6
难度: 中等查看答案及解析
-
某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的溶质质量分数是 ( )
A. 30% B. [(26.5+3.5)/(100+6.5)]×100%
C. 26.5% D. [(26.5+3.5)/(100+6.5+3.5)]×100%
难度: 极难查看答案及解析
-
V L Al2(SO4)3溶液中含Al3+ m g,则溶液中SO42-的物质的量浓度为 ( )
A.
mol/L B.
mol/L
C.
mol/L D.
mol/L
难度: 简单查看答案及解析