-
NA代表阿伏加德罗常数。下列有关NA的叙述中,正确的是( )
A. 1 mol 任何物质所含的微粒数均为NA
B. 14 g氮气所含的N原子数为NA
C. 标准状况下,22.4 L水所含的H2O分子数为NA
D. 在钠与氧气的反应中,1 mol钠失去电子的数目为2 NA
难度: 简单查看答案及解析
-
实验室需配制450 ml 0.1 mol/L的Na2CO3溶液,以下操作正确的是( )
A. 称取4.77 g Na2CO3固体溶于水配成450 mL溶液
B. 称取5.3 g Na2CO3固体溶于水配成500 mL溶液
C. 称取12.9 g Na2CO3·10H2O 固体溶于水配成450mL溶液
D. 量取90 mL 0.5mol/L Na2CO3溶液加360mL水稀释
难度: 中等查看答案及解析
-
在无色透明强酸性溶液中,能大量共存的离子组是( )
A. K+、Cu2+、NO3﹣、SO42﹣ B. K+、Na+、Cl﹣、ClO﹣
C. Zn2+、NH4+、NO3﹣、Cl﹣ D. K+、Na+、Ba2+、SO42﹣
难度: 中等查看答案及解析
-
下列各组离子在无色水溶液中能大量共存的是( )
A. Na+ 、Mg2+ 、 Cl﹣、OH﹣ B. MnO4﹣、HCO3﹣、OH﹣、K+
C. Fe3+、H+、SO42﹣、CH3COO﹣ D. K+、NO3﹣、CO32﹣、Na+
难度: 中等查看答案及解析
-
0.5L 1mol/L FeCl3溶液与0.2L1mol/L KCl溶液中的Cl-的数目之比
A. 5:2 B. 3:1 C. 15:2 D. 1:3
难度: 中等查看答案及解析
-
下列仪器:①容量瓶②蒸镏烧瓶③漏斗④燃烧匙⑤天平⑥分液漏斗⑦胶头滴管,常用于物质分离的是( )
A. ①③⑤ B. ②④⑦ C. ①②⑥ D. ②③⑥
难度: 简单查看答案及解析
-
关于a g 氢气 和b g氦气,下列说法正确的是( )
A. 同温、同压下,氢气和氦气的体积比是a:2b
B. 同温、同压下,若a=b,则氢气 和氦气的物质的量之比为2:1
C. 体积相同时,氦气的质量一定大于氢气的质量
D. 同温同压下,若二者的物质的量相同,其所含原子数也相同
难度: 简单查看答案及解析
-
标准状况下V L的HCl气体溶解在1 L水中(水的密度近似为1 g/mL),所得溶液的密度为ρ g/mL,质量分数为ω,物质的量浓度为c mol/L,则下列关系中不正确的是( )
A. c=1000Vρ/(36.5V+22400) B. ω=36.5V/(36.5V+22400)
C. ω=36.5c/(1000ρ) D. ρ=(36.5V+22400)/(22.4+22.4V)
难度: 中等查看答案及解析
-
下列关于物质分类正确组合是( )
分类组合
碱
酸
盐
氧化物
A
Na2CO3
H2SO4
NaCl
CO2
B
NaOH
HCl
NaHCO3
H2SiO3
C
NaOH
H2CO3
CaCl2
SO2
D
KOH
NaHSO4
CaCO3
CO2
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列关于胶体的叙述不正确的是( )
A. 胶体区别于其它分散系的本质特征是分散质的微粒直径在1nm~100nm
B. Fe(OH)3胶体带正电
C. 往Fe(OH)3胶体中逐滴滴入硫酸溶液,现象是:先有红褐色沉淀后沉淀溶解
D. Fe(OH)3胶体能够吸附水中悬浮的固体颗粒沉降,达到净水目的
难度: 中等查看答案及解析
-
溶液中可能大量存在的一组离子是( )
A. H+、Cl﹣、PO43﹣、Na+ B. H+、Fe2+、SO42﹣、NO3﹣
C. K+、H+、NO3﹣、Na+ D. OH﹣、Br﹣、SO42﹣、NH4+
难度: 简单查看答案及解析
-
某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或两种,现将6.9g样品溶于足量水中,得到澄清溶液,若再加入过量的CaCl2溶液,得到4.5g沉淀,对样品所含杂质的正确判断是( )
A. 肯定有KNO3和Na2CO3,没有Ba(NO3)2
B. 肯定有KNO3,没有Ba(NO3)2,可能还有Na2CO3
C. 肯定没有Na2CO3和Ba(NO3)2,可能有KNO3
D. 以上判断都不正确
难度: 极难查看答案及解析
-
在电解质溶液的导电性实验(装置如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
A. 盐酸中逐滴加入氢氧化钠溶液
B. 硫酸铜溶液中逐滴加入氢氧化钡溶液
C. 硫酸中逐滴加入氯化钡溶液
D. 盐酸中逐滴加入硝酸银溶液
难度: 困难查看答案及解析
-
下列离子方程式中正确的是( )
A. 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑
B. 用小苏打治疗胃酸过多:HCO3﹣+H+═CO2↑+H2O
C. 锌片插入硝酸银溶液中:Zn+Ag+═Zn2++Ag
D. 硫酸溶液与氢氧化铜反应:H++OH﹣═H2O
难度: 中等查看答案及解析
-
一定量某营养液中溶质的配方分别如下:
配方一:0.3mol KCl,0.2mol K2SO4,0.1molZnSO4
配方二:0.1mol KCl,0.3mol K2SO4,0.1molZnCl2
对于两种营养液的成分,下列说法中正确的是( )
A. 只有n(K+)相同 B. 只有n(Cl﹣)相同
C. 完全相同 D. 各离子的物质的量完全不同
难度: 中等查看答案及解析
-
若m g密度为ρ g·cm-3的Al2(SO4)3溶液中含SO42— n g,则该Al2(SO4)3溶液的物质的量浓度是( )
A.
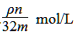 B.
B. 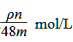 C.
C.  D.
D. 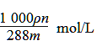
难度: 中等查看答案及解析