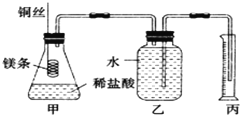
-
下列检验方法和结论正确的是 ( )
A. 加入硝酸银溶液有白色沉淀生成,证明原溶液中一定有Cl-
B. 在加入稀硝酸后的溶液中,再滴加氯化钡溶液有白色沉淀生成,证明原溶液中一定有SO42—
C. 加入盐酸后加热,放出能使澄清石灰水变浑浊的无色无味气体,证明原溶液中一定含有CO32—
D. 加入紫色石蕊试液,溶液显红色,证明溶液一定呈酸性
难度: 中等查看答案及解析
-
“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
A.①④⑥ B.②③④ C.②③⑤ D.①③④⑥
难度: 中等查看答案及解析
-
在 KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O 的反应中,被还原与被氧化的氯原子数之比是
A.6:1 B.1:6 C.5:1 D.1:5
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列关于0.2 mol/L Ba(NO3)2溶液的叙述不正确的是
A. 2 L溶液中阴阳离子总数为1.2NA
B. 500 mL溶液中NO3-浓度为0.2 mol/L
C. 500 mL溶液中Ba2+浓度为0.2 mol/L
D. 500 mL溶液中NO3-物质的量为0.2 mol
难度: 中等查看答案及解析
-
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是
A.Na+、K+、OH-、Cl- B.Na+、Cu2+ 、SO42-、NO3-
C.Mg2+、Na+、SO42-、Cl- D.Ba2+、HCO3-、NO3-、K+
难度: 简单查看答案及解析
-
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序是 ( )
A.⑤②④③① B.④①②⑤③
C.②⑤④①③ D.①④②⑤③
难度: 简单查看答案及解析
-
《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是( )
A.蒸馏 B.升华 C.过滤 D.萃取
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.从碘水中提取单质碘时,不能用无水乙醇代替CCl4
B.
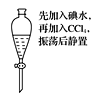 进行该图操作后,实验现象为:液体分层,下层呈紫红色
进行该图操作后,实验现象为:液体分层,下层呈紫红色C.
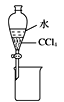 利用该装置可以分离CCl4和水
利用该装置可以分离CCl4和水D.萃取操作时,应选择有机萃取剂,且萃取剂密度必须比水大
难度: 简单查看答案及解析
-
下列变化过程只有通过氧化反应才能实现的是( )
A.HCl→H2 B.HCl→FeCl2 C.H2SO4(浓)→SO2 D.Fe→Fe2O3
难度: 简单查看答案及解析
-
下列叙述中,正确的是
A.纯碱、烧碱均属于碱 B.凡能电离出H+的化合物均属于酸
C.CuSO4·5H2O属于纯净物 D.盐类物质一定含有金属阳离子
难度: 简单查看答案及解析
-
下列物质的溶液能导电,但不属于电解质的是( )
A.Ba(OH)2 B.CH4 C.Cl2 D.HCl
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
A.常温常压下,32 g氧气的体积约为22.4L
B.1.8 g NH4+中含有的质子数为NA
C.常温常压下,48g O3含有的氧原子数为3NA
D.2.4 g金属镁变为镁离子时失去的电子数为0.1NA
难度: 简单查看答案及解析
-
我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人,这种做法的化学原理是( )
A. 胶体的电泳 B. 血液的氧化还原反应 C. 胶体的聚沉 D. 血液中发生复分解反应
难度: 简单查看答案及解析
-
与离子方程式H++OH-===H2O相对应的化学方程式是( )
A.Mg(OH)2+2HCl===MgCl2+2H2O
B.2NaOH+H2SO4===Na2SO4+2H2O
C.Ba(OH)2+H2SO4===BaSO4↓+2H2O
D.Cu(OH)2+2HCl===CuCl2+2H2O
难度: 中等查看答案及解析
-
下列判断正确的是( )
A.同温同压下,相同体积的氮气和氦气所含的原子数相等
B.标准状况下,5.6 L以任意比例混合的氯气和氧气所含的原子数为0.5NA
C.标准状况下,22.4 L SO3与水反应生成1 mol硫酸
D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子
难度: 简单查看答案及解析
-
在标准状况下有:① 6.72 L CH4,② 3.01×1023个HCl分子,③ 13.6 g H2S,④ 0.2 mol NH3。下列对这四种气体的描述正确的是( )
A.体积②>③>①>④ B.密度 ②<③<④<①
C.质量②>③>④>① D.氢原子个数 ①<③<④<②
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数,如果a g某气态物质的分子数为p,则b g该气体在标准状况下的体积V(L)是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列对对应现象的描述与离子方程式都正确的是( )
A.金属镁与稀盐酸反应:有气体生成,Mg+2H++2Cl-=MgCl2+H2↑
B.氯化钡溶液与硫酸反应:有白色沉淀生成:SO42-+Ba2+ =BaSO4↓
C.碳酸钠溶液与盐酸反应:有气泡逸出:Na2CO3+2H+=2Na++CO2↑+H2O
D.过量铁粉与氯化铜溶液反应:溶液南蓝色变成浅绿色,同时有红色固体生成:Fe+Cu2+=Fe3++Cu
难度: 简单查看答案及解析
-
实验室里需要配制480mL 0.10mol·L-1的硫酸铜溶液,下列实验方案及实验操作正确的是( )
容量瓶容积
溶质质量
实验操作
A
480mL
硫酸铜:7.68g
加入 500mL水
B
480mL
胆矾:12.0g
配成500mL溶液
C
500mL
硫酸铜:8.0g
加入500mL水
D
500mL
胆矾:12.5g
配成500mL溶液
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列离子方程式书写错误的是( )
A.三氧化硫与水反应:SO3+H2O=2H++SO42—
B.碳酸钙与盐酸:CaCO3+2H+=Ca2++CO2↑+H2O
C.氧化铜与稀硫酸:CuO+2H+=Cu2++H2O
D.碳酸氢钠溶液与氯化钡溶液反应:Ba2++CO32—=BaCO3↓
难度: 简单查看答案及解析
-
如果Mg2+、M、Fe3+和Cl-四种离子以物质的量之比1∶3∶2∶2共存于同一溶液,那么M可能是
A. CO32- B. NO3- C. OH- D. SO42-
难度: 中等查看答案及解析
-
下列装置中,不添加其他仪器无法检查气密性的是( )
A.
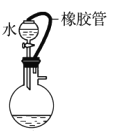 B.
B.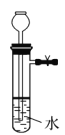 C.
C.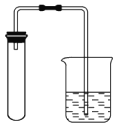 D.
D.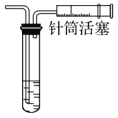
难度: 中等查看答案及解析
-
氮化铝( AlN)广泛应用于电子、陶瓷工业等领域。在一定条件下,AlN可通过如下反应制取:Al2O3+N2+3C
2AlN+3CO。下列叙述正确的是( )
A.AlN中氮的化合价为+3
B.AlN的摩尔质量为41 g
C.上述反应中,N2是氧化剂,Al2O3既不是氧化剂也不是还原剂。
D.上述反应中,每生成1 mol AlN需转移6 mol电子
难度: 简单查看答案及解析
-
把V L含有MgS04和K2S04的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A. (b-a)/V mol·L-1 B.(2b-a)/V mol·L-1
C.2(2b-a)/V mol·L-1 D.2(b-a)/V mol·L-1
难度: 中等查看答案及解析
-
在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如下图所示。下列分析不正确的是
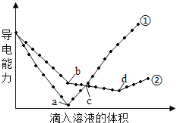
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点,两溶液中含有相同物质的量的OH-
难度: 中等查看答案及解析