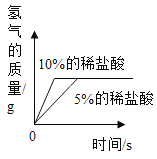
-
水是一种重要的资源。
(1)电解水实验中,生成的氧气和氢气的体积比约是_____,该实验证明了水是由_____元素组成的。
(2)日常生活中,常用_____吸附水中的色素和异味,常用_____区别硬水和软水,可用_____的方法将硬水软化。
难度: 简单查看答案及解析
-
元素周期表是学习和研究化学的重要工具,下图是元素周期表的部分内容及碳原子的结构示意图,完成相关问题。

(1)碳元素的相对原子质量是_____;x的数值为_____。
(2)碳、氧两种元素的本质区别是_____不同,二者能组成一种产生温室效应的气体,其化学式为______。
难度: 简单查看答案及解析
-
人类的衣、食、住、行离不开材料和能源。
(1)地球上的金属资源,除少数不活泼的金属外,大部分是以_____形式存在。工业上用赤铁矿(主要成分是 Fe2O3)和一氧化碳炼铁的化学方程式为__________。
(2)汽油是石油分馏的产品之一,汽油中主要含有_____元素,在汽油中加入乙醇作为汽车燃料的主要目的是节约化石燃料和_____,以氢能源为动力的汽车能真正实现“零排放”但氢能源目前还不能广泛使用的原因之一是_____。
难度: 简单查看答案及解析
-
下图是甲、乙两种固体物质的溶解度曲线。
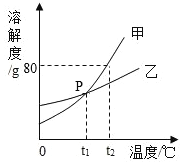
(1)P点的含义是_____。将乙的饱和溶液从t1℃升温至t2℃,溶液的质量分数_____(填“变大”、“不变”或“变小”)。
(2)t2℃时,将50g甲加入50g水中,充分搅拌,所得溶液的质量为_____g。将甲的饱和溶液变成不饱和的方法之一是__________。
(3)乙的饱和溶液中含有少量甲,可用______________方法提纯乙。
难度: 简单查看答案及解析
-
写出下列反应的化学方程式,并注明反应的基本类型。
(1)铁与硫酸铜溶液反应__________、____________
(2)用生石灰与水反应制熟石灰____________、____________
(3)用含氢氧化镁的药物中和过多的胃酸__________、____________
难度: 简单查看答案及解析
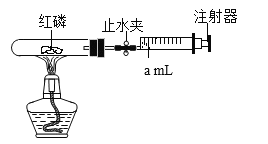
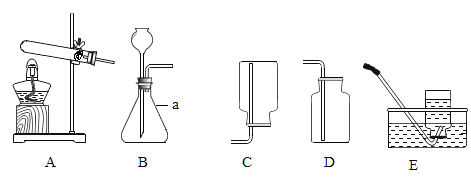
 B
B  C
C