-
下列有关物质分类或归类正确的一组是( )
A. 漂白粉是化合物 B. 水玻璃是纯净物
C. 盐酸是电解质 D. 纯碱不属于碱
难度: 简单查看答案及解析
-
相同条件下,ag的A气体与bg的B气体占有相同体积。下列叙述错误的是 ( )
A. a∶b等于A与B的相对分子质量之比
B. a∶b等于等质量的A与B的分子数之比
C. a∶b等于同温同压下A与B的密度之比
D. b∶a等于同温同体积等质量的A与B的压强比
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 阴离子只有还原性
B. 含有最高价元素的化合物,只有氧化性,不具有还原性
C. Zn和稀硫酸反应既属于离子反应,也属于氧化还原反应
D. 没有单质参加也没有单质生成的反应一定不是氧化还原反应
难度: 中等查看答案及解析
-
下列关于二氧化硅的说法错误的是( )
A. 二氧化硅是一种非金属氧化物
B. 二氧化硅不存在单个的分子
C. 二氧化硅中硅元素与氧元素的质量比为7∶8
D. 二氧化硅分子由一个硅原子和两个氧原子构成
难度: 简单查看答案及解析
-
下列离子方程式正确的是( )
A.氧化钠固体与水反应:2O2-+2H2O=4OH-
B.碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑
C.氢氧化铜与稀硫酸反应:OH-+H+=H2O
D.醋酸跟氢氧化钠溶液反应:H++OH-=H2O
难度: 中等查看答案及解析
-
下列物质中属于纯净物、化合物、无机化合物、盐、钙盐的是
A. 石灰石 B. 氢氧化钙 C. 碳酸钙 D. 甲烷
难度: 简单查看答案及解析
-
下列关于硅的说法不正确的是( )
A.硅是非金属元素,它的单质是灰黑色有金属光泽的固体
B.硅的导电性能介于导体和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质发生反应
D.加热到一定温度时,硅能与氯气、氧气等非金属反应
难度: 简单查看答案及解析
-
使用胆矾配制1 L 0.1 mol·L-1的CuSO4溶液,正确的做法是( )
①将胆矾加热除去结晶水后,称取16 g溶于1 L水中
②称取胆矾25 g溶于1 L水中
③将25 g胆矾溶于少量水,然后将此溶液稀释至1 L
④将16 g CuSO4溶于少量水,然后将此溶液稀释至1 L
A. ①② B. ③④ C. ①③ D. ②④
难度: 简单查看答案及解析
-
下列溶液中溶质的物质的量浓度为1mol/L的是( )
A.将40gNaOH溶解在1L水中
B.将1L10mol/L的浓盐酸加入9L水中
C.将22.4LHCl气体溶于水配成1L溶液
D.将10gNaOH溶解在少量水中,再加蒸馏水直到溶液体积为250mL
难度: 中等查看答案及解析
-
下图是利用二氧化硅制备硅及其化合物的流程,下列说法正确的是
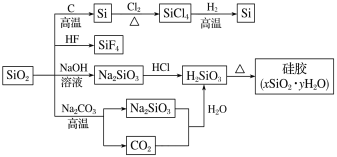
A.SiO2属于两性氧化物 B.酸性:H2SiO3>H2CO3
C.硅胶吸水后可重复再生 D.图中所示转化反应都是氧化还原反应
难度: 简单查看答案及解析
-
等质量的下列物质在常温常压下体积最大的是
A. 浓硫酸 B. 二氧化碳 C. 铁 D. 冰水混合物
难度: 简单查看答案及解析
-
下列反应中不能得到氢氧化铝沉淀的是 ( )
A. 硫酸铝溶液与过量的氨水混合 B. 氯化铝溶液中加入几滴烧碱溶液
C. 偏铝酸钠溶液中加入过量的盐酸 D. 偏铝酸钠溶液中通入过量的二氧化碳
难度: 简单查看答案及解析
-
钢笔的笔头通常由合金钢制成,其笔头尖端是用机器轧出的便于书写的圆珠体。为了改变笔头的耐磨性能,在笔头尖端点上铱金粒,为区别于钢笔,而叫作铱金笔,铱金笔是笔头用黄金的合金制成、笔尖用铱的合金制成的高级自来水笔。下列说法错误的是( )
A. 钢笔的笔头不易被氧化,耐腐蚀性能好
B. 铱金笔的耐磨性能比钢笔好
C. 钢笔的笔头只含有碳和铁两种元素
D. 铱金笔经久耐磨,书写时弹性好,是一种理想的硬笔
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 1molCH5+中含有的电子数为11NA
B. 常温常压下,2.24LCO和CO2的混合气体中含有的碳原子数为0.1NA
C. 室温下,0.1mol·L-1的NaOH溶液中所含OH-的个数为0.1NA
D. 常温常压下,18gH2O中含有的原子总数为3NA
难度: 简单查看答案及解析
-
欲使明矾溶液中的铝离子完全沉淀下来,适宜的试剂是( )
A.氢氧化钠溶液 B.氢氧化钾溶液 C.氨水 D.盐酸
难度: 中等查看答案及解析
-
100 mL 2 mol/L的稀盐酸与一定量的锌充分反应,锌全部溶解,生成的氢气在标准状况下体积为1.12 L,设反应后溶液的体积仍为100 mL,则反应后溶液中H+的物质的量的浓度为
A.1.5mol/L B.1mol/L C.0.5mol/L D.0.25mol/L
难度: 中等查看答案及解析
-
下列反应中既是分解反应又属于氧化还原反应的是( )
A.C + O2
CO2
B.CaCO3
CaO + CO2↑
C.2KMnO4
K2MnO4+ MnO2 + O2↑
D.Zn+H2SO4=ZnSO4+H2↑
难度: 中等查看答案及解析
-
下列关于二氧化硅的说法正确的是( )
A.二氧化硅溶于水显酸性
B.二氧化硅是酸性氧化物,它不溶于任何酸
C.二氧化硅是制造光电池的材料
D.二氧化硅制作的玻璃纤维丝,可用作光导纤维
难度: 中等查看答案及解析
-
下列说法正确的是
A. 同温同压下甲烷和氧气的密度之比为2∶1
B. 1 g甲烷和1 g氧气的原子数之比为5∶1
C. 等物质的量的甲烷和氧气的质量之比为2∶1
D. 在标准状况下等质量的甲烷和氧气的体积之比为1∶2
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA
B.标准状况下,22.4 L空气含有NA个单质分子
C.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA
D.常温下,23 g NO2含有NA个氧原子
难度: 中等查看答案及解析
-
将BaCl2溶液加入某无色溶液后,生成白色沉淀,再加入稀HNO3,则沉淀不溶解,下列说法正确的是( )
A.一定存在Ag+ B.一定存在CO32— C.一定存在SO42— D.以上说法都不对
难度: 中等查看答案及解析
-
反应3NO2+H2O===2HNO3+NO中,当有6 mol e-发生转移时,被氧化的物质与被还原的物质的物质的量之比为( )
A.1∶1 B.1∶2 C.2∶1 D.3∶1
难度: 中等查看答案及解析
-
在xR2+ +yH++O2=mR3+ +nH2O的离子方程式中,对m和R3+判断正确的是
A. m=4,R3+是氧化产物 B. m=2y,R3+是氧化产物
C. m=2,R3+是还原产物 D. m=y,R3+是还原产物
难度: 中等查看答案及解析
-
古代有火烧孔雀石炼铜(加入炭)和湿法炼铜(在溶液中加铁),下列有关说法不正确的是( )
A.火烧孔雀石炼铜发生的反应有Cu2(OH)2CO3
2CuO+CO2↑+H2O
B.火烧孔雀石炼铜发生的反应有2CuO+C
CO2↑+2Cu
C.湿法炼铜发生的主要反应为Fe+Cu2+===Cu+Fe2+
D.两种炼铜的方法涉及的主要反应都是氧化还原反应
难度: 简单查看答案及解析
-
在水溶液中,下列电离方程式正确的是( )
A.NaOH=
+
B.NaOH=Na++H++O2-
C.H2SO4
H2++SO42- D.NaOH=Na++OH-
难度: 简单查看答案及解析