-
朱自清在《荷塘月色》冲写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的班驳的黑影……”月光穿过薄雾形成的种种美景本质原因是
A. 空气中的小水滴颗粒直径大小约为1nm--100nm
B. 空气中的小水滴颗粒的布朗运动
C. 雾是一种胶体,胶粒带相同电荷
D. 发生丁达尔效应
难度: 简单查看答案及解析
-
成语是中华民族灿烂文化中的瑰宝,许多成语中蕴含着丰富的化学原理,下列成语中涉及氧化还原反应的是
A.木已成舟 B.蜡炬成灰 C.铁杵成针 D.滴水成冰
难度: 简单查看答案及解析
-
分类是学习和研究化学的一种重要方法,下列分类合理的是( )
A.Na2O和Na2O2都属于碱性氧化物 B.SO3和SO2都属于酸性氧化物
C.漂白粉和CuSO4∙5H2O都属于混合物 D.烧碱和纯碱都属于碱
难度: 中等查看答案及解析
-
将质量相等、体积相同的金属钠分别投入到水和0.1mol/L的CuSO4溶液中,下列有关说法不正确的是( )
A.金属钠均熔成闪亮的小球 B.在硫酸铜溶液中可得到红色的铜
C.金属钠均浮在液面上,且四处游动 D.均有置换反应发生
难度: 中等查看答案及解析
-
两个体积相同的容器,一个盛有NO,另一个盛有N2和O2,在同温同压下两容器内的气体一定具有相同的
A.电子总数 B.质子总数 C.原子总数 D.质量
难度: 简单查看答案及解析
-
实验室用NaCl固体配200mL 1.0 mol/L NaCl溶液,下列判断不对的是
A.用托盘天平称取NaCl固体11.7g
B.应选用250 mL的容量瓶来配制此溶液
C.在转移操作中不慎将溶液洒到容量瓶外面,应该重新配制溶液
D.加蒸馏水至离刻度线1~2 cm时改用胶头滴管定容
难度: 中等查看答案及解析
-
下列实验操作正确的是( )
A.用灼热的氧化铜除去CO2中混有的少量CO
B.用NaOH溶液除去SO2中混有的HCl
C.用100mL量筒量取8.53mL蒸馏水
D.为加快过滤速度,可用玻璃棒在漏斗中搅拌
难度: 中等查看答案及解析
-
设NA为阿伏伽德罗常数的值。下列说法正确的是( )
A.2.3g的金属钠与足量的O2反应,转移的电子数目为0.1NA
B.室温下,0.2mol·L-1的Na2SO4溶液中含Na+数目为0.4NA
C.标准状况下,NA个H2O分子所占的体积约为22.4L
D.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA
难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A.铁跟盐酸的反应:Fe+2H+=Fe3++H2↑
B.向小苏打溶液中滴入盐酸:CO32-+2H+=CO2↑+H2O
C.氯气通入水中:Cl2+H2O=2H++ClO-+Cl-
D.氨水中通入少量二氧化碳:2NH3·H2O+CO2=2NH4++CO32-+H2O
难度: 中等查看答案及解析
-
在无色透明溶液中,下列各组离子能够大量共存的是( )
A.K+、Na+、MnO4-、SO42- B.Mg2+、Cl-、H+、SO42-
C.Na+、OH-、Ba2+、CO32- D.OH-、HCO3-、Na+、Cl-
难度: 中等查看答案及解析
-
下列反应中,HCl只表现还原性的是( )
A.Zn+2HCl=ZnCl2+H2↑ B.O2+4HCl=2Cl2+2H2O
C.MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O D.2HCl=Cl2+H2
难度: 中等查看答案及解析
-
溶洞和钟乳石是大自然的杰作。溶洞和钟乳石的形成与自然界中碳及其化合物间的转化有着密切联系。下列有关自然界中碳及其化合物间的转化的说法,不正确的是( )
A.溶洞是通过CaCO3与H2O、CO2作用生成可溶性的Ca(HCO3)2形成的
B.游客的参观不会对其造成影响
C.溶洞和钟乳石的形成过程中没有涉及氧化还原反应
D.钟乳石是在一定条件下可溶性的Ca(HCO3)2转化成CaCO3的结果
难度: 中等查看答案及解析
-
下列反应起了氮的固定作用是( )
A.N2和H2在一定条件下反应生成NH3 B.硝化细菌分解铵盐生成硝酸盐
C.NO与O2反应生成NO2 D.由NH3制碳铵或硫铵
难度: 中等查看答案及解析
-
已知气体的摩尔质量越小,扩散速度越快。右图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是( )
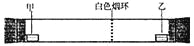
A.甲是浓氨水,乙是浓硫酸 B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸 D.甲是浓硝酸,乙是浓氨水
难度: 中等查看答案及解析
-
下列叙述不正确的是( )
A. 氨易液化,液氨常用作制冷剂
B. 与金属反应时,稀硝酸可能被还原为更低价态,稀硝酸氧化性强于浓硝酸
C. 铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处
D. 稀硝酸和活泼金属反应时得不到氢气
难度: 简单查看答案及解析
-
如图所示转化关系中不能一步实现的是( )
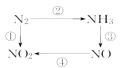
A.① B.② C.③ D.④
难度: 中等查看答案及解析
-
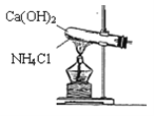
下列实验装置正确的是( )
A.
 加热分解碳酸氢钠
加热分解碳酸氢钠B.
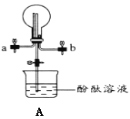
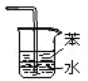 吸收氨气
吸收氨气C.
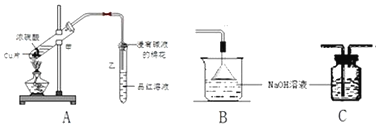
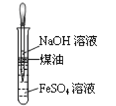 制取氢氧化亚铁并观察颜色
制取氢氧化亚铁并观察颜色D.
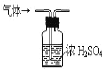 干燥氨气
干燥氨气难度: 中等查看答案及解析
-
下列有关说法正确的是( )
A.因为硫单质具有氧化性,故铁粉与硫粉共热可以生成Fe2S3
B.硫在空气中燃烧的产物是SO2,在纯氧中燃烧的产物是SO3
C.SO2的水溶液能导电,所以SO2是电解质
D.二氧化硫可用于抑制酒类中细菌的生长,可在葡萄酒中微量添加
难度: 中等查看答案及解析
-
下列四种有色溶液与SO2气体作用,其实质相同的是( )
①酸性高锰酸钾溶液;②品红溶液;③溴水;④滴有酚酞的氢氧化钠溶液;
A.②③ B.①③ C.①④ D.②④
难度: 中等查看答案及解析
-
下列溶液中能够区别SO2和CO2气体的是( )
①澄清石灰水 ②H2S溶液 ③KMnO4溶液 ④品红溶液
A.①②③ B.①③④ C.②③④ D.①②③④
难度: 中等查看答案及解析
-
在稀硫酸中加入铜粉,铜粉不溶,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;④KNO3。铜粉可溶解的是( )
A.①② B.①④ C.②③ D.②④
难度: 中等查看答案及解析
-
下列实验能达到预期目的是
A.向某无色液中加入BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有SO42-
B.向某无色溶液中加入盐酸,有无色无味的气体产生,则说明原溶液中一定有CO32-
C.向某溶液中滴加KSCN溶液,溶液不变红,再滴加氯水,溶液变红,则说明有Fe2+
D.将淀粉溶液和食盐溶液混合装入半透膜,浸入纯水中,过一段时间,取半透膜内的液体滴入碘水呈蓝色,说明利用渗析可提纯胶体
难度: 简单查看答案及解析
-
NaCl是一种化工原料,可以制备一系列物质。下列说法正确的是
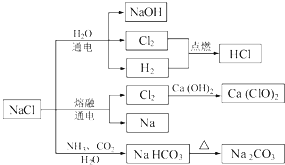
A.25℃,NaHCO3在水中的溶解度比Na2CO3的大
B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂
C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应
D.图4所示转化反应都是氧化还原反应
难度: 中等查看答案及解析
-
常温下,在溶液中可发生以下反应:①2Fe2++ Br2= 2Fe3++ 2Br-,②2Br-+ Cl2=Br2+ 2Cl-, ③2Fe3++ 2I-= 2Fe2++ I2;由此判断下列说法错误的是
A.铁元素在反应①中被氧化,在③中被还原
B.反应②中当有1 mol Cl2被还原时,有2 mol Br-被氧化
C.氧化性强弱顺序为:Cl2 > I2 > Br2 > Fe3+
D.还原性强弱顺序为:I- > Fe2+ > Br- > Cl-
难度: 简单查看答案及解析
-
Cl2和SO2都具有漂白作用,若将等物质的量的这两种气体混合通入品红与BaCl2的混合溶液中,能观察到的现象是: ①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
A.①② B.①③ C.②③ D.②④
难度: 中等查看答案及解析