-
化学式为C4H8O3的有机物,在浓硫酸存在和加热时,有如下性质:
①能分别与CH3CH2OH和CH3COOH反应。
②脱水生成一种能使溴水褪色的物质,该物质只存在一种结构简式。
③能生成一种分子式为C4H6O2的五元环状化合物。
则C4H8O3的结构简式为( )
A. HOCH2COOCH2CH3 B. CH3CH(OH)CH2COOH
C. HOCH2CH2CH2COOH D. CH3CH2CH(OH)COOH
难度: 中等查看答案及解析
-
下列结论错误的是( )
①微粒半径:r(K+)>r(Al3+)>r(S2-)>r(Cl-) ②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO ⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
A.① B.①③ C.②③④⑤⑥⑦ D.①③⑤
难度: 中等查看答案及解析
-
2015年诺贝尔生理学或医学奖授予我国女药学家屠呦呦,她从中药中分离出青蒿素应用于疟疾治疗.青蒿素的键线结构简式如图.下列关于青蒿素的说法不正确的是
A.分子式为C15H22O5
B.属于芳香族化合物
C.可发生水解反应
D.含有过氧键(-O-O-)有强氧化性
难度: 中等查看答案及解析
-
在实验室中,下列除去杂质的方法不正确的是( )
A. 溴苯中混有溴,加稀NaOH溶液反复洗涤、分液
B. 硝基苯中混有浓硝酸和浓硫酸,将其倒入NaOH溶液中,静置,分液
C. 乙烷中混有乙烯,与氢气在一定条件下反应,使乙烯转化为乙烷
D. 乙烯中混有SO2和CO2,将其通过NaOH溶液洗气
难度: 中等查看答案及解析
-
类比推理的方法在化学学习与研究中有广泛的应用,但有时会得出错误的结论,以下几种类比推理结论中正确的是( )
A.H2SO4为强酸,推出HClO4为强酸
B.Fe3Cl8可以改写为FeCl2·2FeCl3,推出Fe3I8可以改写为FeI2·2FeI3
C.NH3的沸点高于PH3,推出CH4沸点高于SiH4
D.CO2通入Ba(NO3)2溶液中无沉淀生成,推出SO2通入Ba(NO3)2溶液中无沉淀生成
难度: 中等查看答案及解析
-
下列有机物命名正确的是
A.
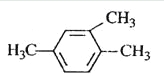 1,3,4-三甲苯
1,3,4-三甲苯B.
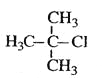 2-甲基-2-氯丙烷
2-甲基-2-氯丙烷C.
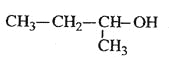 2-甲基-1-丙醇
2-甲基-1-丙醇D.
 2-甲基-3-丁炔
2-甲基-3-丁炔难度: 中等查看答案及解析
-
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实不能说明上述观点的是
A.甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色
B.乙基对羟基的影响,使羟基的活性变弱,电离H+的能力不及H2O
C.乙烯能发生加成反应,而乙烷不能发生加成反应
D.苯酚中的羟基氢能与NaOH溶液反应,而醇羟基氢不能与NaOH溶液反应
难度: 中等查看答案及解析
-
有机物甲的分子式为CxHyO2,其中氧的质量分数为20.25%,碳的质量分数为68.35%。在酸性条件下,甲水解生成乙和丙两种有机物;在相同温度和压强下,同质量的乙和丙的蒸气所占的体积相同,则甲的结构可能有( )
A.10种 B.12种 C.14种 D.16种
难度: 困难查看答案及解析
-
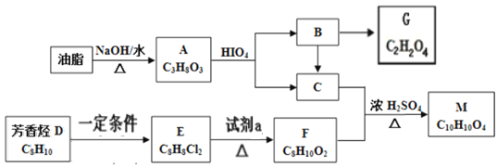
以乙醇为原料,用下述6种类型的反应:①氧化;②消去;③加成;④酯化;⑤水解⑥加聚,来合成乙二酸乙二酯(
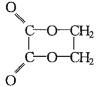 )的正确顺序是( )
)的正确顺序是( )A.①⑤②③④ B.①②③④⑤ C.②③⑤①④ D.②③⑤①⑥
难度: 中等查看答案及解析
-
下列说法中正确的是 ( )
①晶体中分子间作用力越大,分子越稳定 ②原子晶体中共价键越强,熔点越高 ③干冰是CO2分子通过氢键和分子间作用力有规则排列成的分子晶体 ④在Na2O和Na2O2晶体中,阴、阳离子数之比相等 ⑤正四面体构型的分子,键角都是109°28′,其晶体类型可能是原子晶体或分子晶体 ⑥分子晶体中都含有化学键 ⑦含4.8 g碳元素的金刚石晶体中的共价键的物质的量为0.8 mol
A.①②③④⑤ B.②④⑦ C.②④⑥⑦ D.③④⑤⑥⑦
难度: 中等查看答案及解析
-
X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W分别与Y形成的最高价化合物为甲、乙、丙。结合如图转化关系,下列判断错误的是( )
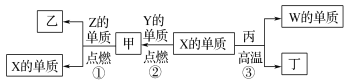
A.反应③可用于工业上制取W的单质 B.X位于元素周期表第二周期ⅣA族
C.甲、丙、丁均为酸性化合物 D.工业上可以用乙来作耐火材料
难度: 困难查看答案及解析
-
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。5种元素核电荷数之和为54,最外层电子数之和为20。W、Z最外层电子数相同,Z的核电荷数是W的2倍。工业上一般通过电解氧化物的方法获得Y的单质。则下列说法不正确的是( )
A.原子半径:X>Y>Q>W
B.Q的单质都具有良好的导电性
C.Q和Z所形成的分子的空间构型为直线形
D.化合物Y2Z3不能在水中稳定存在
难度: 中等查看答案及解析
-
以下微粒含配位键的是( )
①N2H5+ ②CH4③OH-④NH4+ ⑤Fe(CO)3 ⑥Fe(SCN)3 ⑦H3O+⑧[Ag(NH3)2]OH
A.①④⑤⑥⑦⑧ B.①②④⑦⑧ C.①③④⑤⑥⑦ D.全部
难度: 中等查看答案及解析
-
下列叙述及评价均合理的是( )
选项
叙述
评价
A
可以用新制的Cu(OH)2悬浊液鉴别乙醇溶液、乙酸溶液和葡萄糖溶液
错,用新制的Cu(OH)2悬浊液不能鉴别乙醇溶液和乙酸溶液。
B
淀粉与20%的硫酸混合溶液在沸水浴中充分加热后滴加碘水无蓝色现象,则说明淀粉水解完全
错,淀粉水解后未加碱中和至溶液呈碱性。
C
向卤代烃水解后的溶液中加入AgNO3溶液,根据沉淀颜色可以判断卤素原子种类
对,水解后溶液中有卤化氢,与AgNO3溶液反应生成卤化银沉淀。
D
乙酸乙酯在H218O中水解,产物乙醇中将含有18O
错,根据酯的水解规律,产物乙酸中将含有18O同位素,而乙醇则没有。
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
国庆期间对大量盆栽鲜花施用了S-诱抗素制剂以保证鲜花盛开,S-诱抗素的分子结构如图。下列关于该物质的说法正确的是
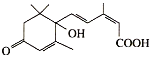
A. 该有机物的分子式为C15H21O4
B. 该有机物能发生取代、加成和水解反应
C. 1mol该有机物与足量溴反应最多消耗4mol Br2
D. 1mol该有机物与足量Na反应生成生成1mol H2
难度: 中等查看答案及解析
-
在标准状况下,11.2L由甲烷、甲醛和乙烷组成的混合气体完全燃烧后,生成15.68L相同状况下的CO2气体,则混合气体中乙烷所占体积分数为
A.20% B.40% C.60% D.80%
难度: 中等查看答案及解析