-
下列化学药品与其危险化学品图形标志不一致的一组是( )
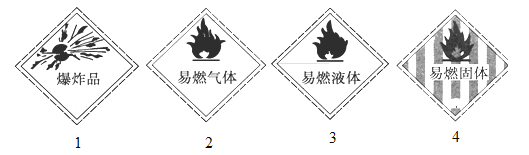
A.小苏打—1 B.甲烷—2 C.酒精—3 D.白磷—4
难度: 简单查看答案及解析
-
将下列各组物质按酸、碱、盐分类依次排列,正确的是( )
A.磷酸、熟石灰、苛性钠 B.硝酸、苛性钠、小苏打
C.硫酸氢钠、生石灰、醋酸钠 D.硫酸、纯碱、胆矾
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.直径介于1nm~100nm之间的微粒称为悬浊液
B.制备Fe(OH)3胶体的方法是将饱和FeCl3溶液加热煮沸
C.胶体与浊液的本质区别是其稳定性,胶体属于介稳体系
D.利用丁达尔效应可以区分溶液和胶体
难度: 简单查看答案及解析
-
下列说法中,错误的是( )
A.SO2水溶液能导电,但是SO2是非电解质
B.Na2CO3既是钠盐又是碳酸盐
C.铜可以导电所以铜是电解质
D.NaCl在水溶液能导电,所以NaCl是电解质
难度: 简单查看答案及解析
-
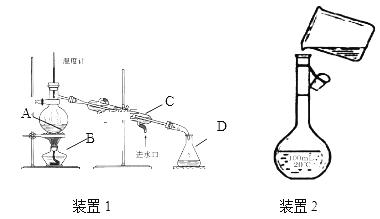
下列实验装置图所示的实验操作,不能达到相应的实验目的的是( )
A. 分离沸点相差较大液体混合物
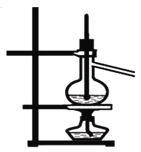
B. 除去CO气体中的CO2气体
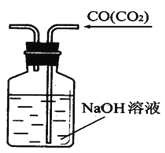
C. 向容量瓶中转移液体
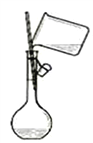
D. 分离互不相溶的两种液体
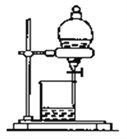
难度: 简单查看答案及解析
-
下列选项中全属于电解质的是( )
①稀盐酸 ②NaCl晶体 ③液态的醋酸 ④铜 ⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化KNO3 ⑨液态SO3 ⑩明矾
A.①④⑥⑦⑨ B.②③⑥⑦⑨
C.②③⑤⑧⑩ D.①②⑤⑧⑩
难度: 简单查看答案及解析
-
列离子方程式书写正确的是
A.铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑
B.碳酸钠与过量盐酸反应:CO32-+2H+=CO2↑+H2O
C.氢氧化钡溶液中滴加硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.硫酸铜溶液与氢氧化钡溶液反应:Cu2++2OH-=Cu(OH)2↓
难度: 简单查看答案及解析
-
下列反应能用离子方程式:H++OH-=H2O。表示的是( )
A.CH3COOH+NaOH=CH3COONa+H2O
B.2H2SO4+Cu(OH)2=CuSO4+2H2O
C.HCl+KOH=KCl+H2O
D.HCl+NH3·H2O=NH4Cl+H2O
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数,下列说法中正确的是( )
A.54g H2O中含有3NA个氢原子
B.1mol Na2SO4溶于水中,所得溶液中Na+个数为NA
C.标准状况下,NA个H2O分子所占的体积约为22.4L
D.1mol CO2和NO2的混合物中含的氧原子数为2NA
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.24g镁与27g铝中,含有相同的质子数
B.同等质量的氧气和臭氧中,氧原子数相同
C.1mol/L NaOH溶液中,含Na+数目为NA
D.标准状况下,NA个四氯化碳分子所占的体积约为22.4L
难度: 中等查看答案及解析
-
强碱性的无色透明溶液中,能大量共存的离子组是( )
A.K+、Na+、SO42-、CO32- B.Mg2+、NH4+、NO3-、Cl-
C.Ba2+、K+、Cu2+、Cl- D.Na+、Ag+、HCO3-、Cl-
难度: 简单查看答案及解析
-
下列反应不属于氧化还原反应的是( )
A.MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O B.CO2+H2O=H2CO3
C.2KClO3
2KCl+3O2↑ D.Fe2O3+3CO
2Fe+3CO2
难度: 简单查看答案及解析
-
关于Zn+2HCl=ZnCl2+H2的反应,下列说法正确的是( )
A.单质Zn中Zn的化合价升高,被还原,是氧化剂
B.HCl中H的化合价降低,被氧化,HCl是还原剂
C.H2是还原产物
D.该反应是复分解反应,也是氧化还原反应
难度: 简单查看答案及解析
-
除去某溶液里溶解的少量杂质(括号内的物质为杂质),下列做法中不正确的是( )
A.KNO3溶液(AgNO3):加过量KCl溶液,过滤
B.NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸
C.H2O中(Br2):加CCl4,萃取分液
D.ZnSO4溶液(CuSO4溶液):加过量Zn,过滤
难度: 中等查看答案及解析
-
某反应可用下式表示:xR2++yH++O2===mR3++nH2O。则m的值为 ( )
A.4 B.2x C.
D.7
难度: 简单查看答案及解析
-
有Na2CO3、AgNO3、BaCl2、HCl及NH4NO3无标签溶液, 为鉴别它们,取四支试管分别装入一种溶液,向上述四支试管中分别加入少许剩下的一种溶液A,下列结论错误的是( )
A.有三支试管出现沉淀时,则A是AgNO3溶液
B.若只有两支试管出现沉淀时,则A是BaCl2溶液
C.一支试管出现气体,两支试管出现沉淀时,则A是HCl溶液
D.若全部没有什么现象变化时,则A是NH4NO3溶液
难度: 中等查看答案及解析