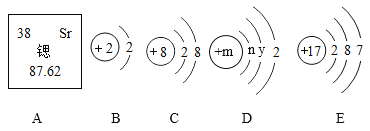
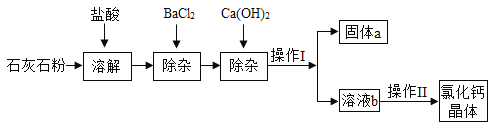
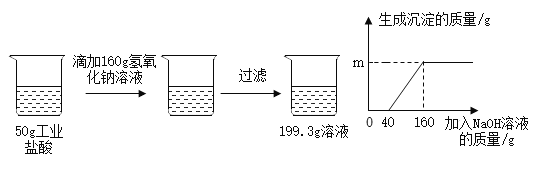
-
化学与人类的生活密切相关。下列对化学知识的应用归纳完全正确的一组是( )
A.化学与资源
B.化学与安全
①太阳能、煤、石油、天然气都是可再生资源
②我国试采新能源“可燃冰”已经成功
①在室内放一盆水能防止煤气中毒
②用甲醛的水溶液浸泡海产品防腐
C.化学与生活
D.化学与环境
①铵盐在农业生产中常用作氮肥,使用时不能与石灰、草木灰混合
②用灼烧闻气味的方法区别棉纤维和羊毛纤维
①目前,二氧化碳、臭氧等物质计入“空气污染指数”
②使用可降解的塑料可减少“白色污染”
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列物质的用途中,主要利用其物理性质的是
A.铁粉用作食品脱氧剂
B.小苏打用于治疗胃酸过多
C.氧气供给呼吸
D.干电池中,石墨用作电极
难度: 简单查看答案及解析
-
下列实验操作正确的是
A.
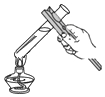 给液体加热 B.
给液体加热 B.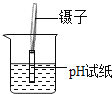 测定溶液的pH
测定溶液的pHC.
 测定氧气含量 D.
测定氧气含量 D.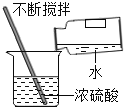 稀释浓硫酸
稀释浓硫酸难度: 简单查看答案及解析
-
下列说法正确的是
A.缺铁会引起贫血,铁是人体中的常量元素
B.用明矾可以检验硬水和软水
C.变瘪的乒乓球放入热水中能鼓起来,说明分子大小随温度改变而改变
D.棉花、羊毛和天然橡胶均属于天然有机高分子材料
难度: 简单查看答案及解析
-
化学概念在逻辑上存在如图关系,下列对概念间相互关系的说法正确的是( )
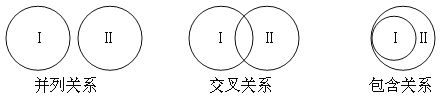
A.混合物与纯净物属于包含关系
B.合成材料与合金属于并列关系
C.复分解反应与中和反应属于并列关系
D.糖类与淀粉属于交叉关系
难度: 简单查看答案及解析
-
2018年夏天,电影《我不是药神》让无数人泪目。片中的格列宁是治疗慢粒白血病的特效药,通用名称为甲磺酸伊马替尼,化学式为C29H31N7O﹒CH4SO3。下列关于格列宁的说法正确的是
A.格列宁的相对分子质量是589g
B.一个格列宁分子中含有77个原子
C.格列宁中含有三氧化硫分子
D.格列宁中碳、氧元素的质量比为15:2
难度: 简单查看答案及解析
-
某火箭在发射过程中,发生反应的微观过程示意图如下:
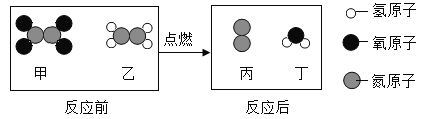
下列说法不正确的是( )
A.甲中氮、氧原子个数比是1∶2 B.乙的相对分子质量是32
C.反应前后氢元素的质量减小 D.生成的丙和丁的分子个数比是3∶4
难度: 中等查看答案及解析
-
为了达到实验目的,下列方案或结论正确的是( )
选项
实验目的
实验方案或结论
A
除去CO2中混有少量HCl气体
通入装有足量NaOH溶液的洗气瓶
B
除去KCl固体中的K2CO3
取样、溶解、加入足量的稀硫酸,蒸发
C
鉴别碳粉、铁粉和氧化铜粉末
取样后,分别加入稀盐酸
D
鉴别某溶液中是否含有SO42-
取少量溶液于试管中,滴加BaCl2溶液,有白色沉淀生成,则该溶液中一定有SO42-
A. A B. B C. C、 D. D
难度: 简单查看答案及解析
-
向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法,其中正确的是
A.滤渣中一定含有Ag,一定没有铝
B.向滤渣中加入稀盐酸,一定有气泡产生
C.向滤液中加入稀盐酸,一定有沉淀产生
D.滤液中一定含有Fe(NO3)2,一定不含AgNO3 ,可能含有Al(NO3)3
难度: 中等查看答案及解析
-
在实验室配制溶液时,可能涉及以下步骤:①称量;②过滤;③蒸发结晶、干燥;④计算;⑤溶解;⑥量取。甲同学用20g含杂质10%的粗盐(杂质不溶于水)和蒸馏水,配制100 g质量分数为12%的氯化钠溶液,正确的操作顺序是
A.④①⑥⑤
B.⑤②③⑥④①⑤
C.④⑤②③①⑤⑥
D.⑤②③④①⑥⑤
难度: 简单查看答案及解析
-
下列图像能正确反映其对应的实验操作的是
A.
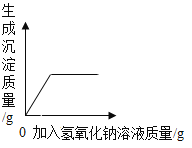 向稀硫酸和硫酸铁的混合溶液中滴加氢氧化钠溶液直至过量
向稀硫酸和硫酸铁的混合溶液中滴加氢氧化钠溶液直至过量B.
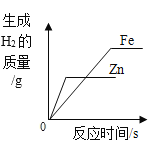 相同质量的铁和锌分别与质量分数相同的足量稀盐酸反应
相同质量的铁和锌分别与质量分数相同的足量稀盐酸反应C.
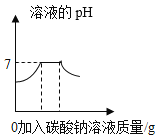 向一定量氯化钡与盐酸的混合溶液中逐滴加入碳酸钠溶液至过量
向一定量氯化钡与盐酸的混合溶液中逐滴加入碳酸钠溶液至过量D.
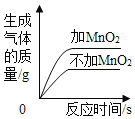 用两份等质量、等浓度的过氧化氢溶液制氧气,其中一份加入少量MnO2
用两份等质量、等浓度的过氧化氢溶液制氧气,其中一份加入少量MnO2难度: 中等查看答案及解析
-
取一定量的氧化镁与氧化铜的混合物,向其中加入溶质质量分数为7. 3%的稀盐酸100 g,恰好完全反应生成盐和水。则原混合物中氧元素的质量是
A.1.6 g B.3.6 g C.7.3 g D.4.8 g
难度: 中等查看答案及解析