-
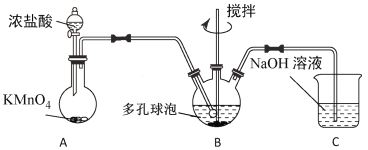
2019年诺贝尔化学奖授予约翰·B·古迪纳、斯坦利·惠廷汉和吉野彰,以表彰他们在开发锂离子电池方面做出的卓越贡献。锂电池正极材料用到的钴酸锂(LiCoO2)属于( )
A.氧化物 B.酸 C.碱 D.盐
难度: 简单查看答案及解析
-
当光束通过下列分散系时,能产生丁达尔效应的是( )
A.稀盐酸 B.CuSO4溶液 C.Fe(OH)3胶体 D.NaCl 溶液
难度: 简单查看答案及解析
-
下列生活中常见物质主要成分的化学式表示正确的是( )
A.铁红—Fe2O3 B.漂白粉—NaClO
C.生石灰—Ca(OH)2 D.纯碱—NaHCO3
难度: 简单查看答案及解析
-
下列物质属于非电解质的是( )
A.硝酸 B.氢氧化钠 C.硫酸铵 D.蔗糖
难度: 简单查看答案及解析
-
实验室制备下列气体时,不能用排空气法收集的是( )
A.NH3 B.CO2 C.NO D.NO2
难度: 简单查看答案及解析
-
实验室用NaCl固体配制100mL0.10mol·L-1NaCl溶液。下列图示实验操作中不需要进行的是( )
A.溶解
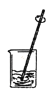 B.蒸发
B.蒸发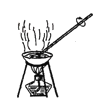
C.转移
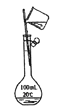 D.定容
D.定容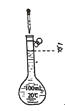
难度: 简单查看答案及解析
-
将K2CO3浓溶液喷洒到酒精灯火焰上,透过蓝色钴玻璃可以观察到火焰的颜色是( )
A.黄色 B.紫色 C.红色 D.绿色
难度: 简单查看答案及解析
-
下列物质不能与氢氧化钠溶液反应的是( )
A.NO2 B.Fe2O3 C.SO3 D.NaHCO3
难度: 简单查看答案及解析
-
下列变化中,不属于化学变化的是( )
A.活性炭使红墨水褪色 B.FeSO4溶液使酸性高锰酸钾溶液褪色
C.氯水使有色布条褪色 D.SO2使品红溶液褪色
难度: 简单查看答案及解析
-
下列试剂的保存方法错误的是( )
A.少量的钠保存在煤油中
B.亚硫酸钠固体密封保存
C.保存氯化亚铁溶液时加入铜粉以防止氧化
D.浓硝酸保存在棕色试剂瓶中并置于冷暗处
难度: 简单查看答案及解析
-
下列有关物质性质与用途具有对应关系的是( )
A.SO2具有氧化性,可用于漂白纸浆
B.氨气易液化且汽化时吸收大量的热,可用作制冷剂
C.NH4HCO3受热易分解,可用作氮肥
D.生石灰能与水反应,可用来干燥氯气
难度: 中等查看答案及解析
-
在含有大量的H+、Ba2+、Cl-的溶液中,还可能大量共存的离子是( )
A.OH- B.Mg2+ C.Ag+ D.CO32-
难度: 简单查看答案及解析
-
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.Ca(OH)2
Ca(ClO)2(aq)
HClO(aq)
B.Fe(s)
Fe2O3(s)
FeCl3(aq)
C.S(s)
SO2(g)
BaSO3(s)
D.NH3(g)
NO(g)
HNO3(aq)
难度: 中等查看答案及解析
-
下列物质间的转化一定需要加入氧化剂才能实现的是( )
A.C →CO2 B.H2O2→O2 C.SO2→ S D.KMnO4→MnO2
难度: 中等查看答案及解析
-
N2O俗称“笑气”,医疗上曾用作可吸入性麻醉剂。下述反应能产生N2O:3CO + 2NO2= 3CO2+ N2O。下列关于该反应的说法正确的是( )
A.CO是氧化剂 B.N2O是氧化产物
C.NO2被还原 D.常温常压下,生成6.72LCO2转移0.6mol电子
难度: 中等查看答案及解析
-
下列有关化学反应的叙述正确的是( )
A.用酒精灯加热Fe(OH)3生成FeO B.实验室加热NH4Cl固体制取NH3
C.SO2和过量氨水反应生成(NH4)2SO3 D.Na在空气中燃烧制取Na2O
难度: 中等查看答案及解析
-
下列指定反应的离子方程式正确的是( )
A.碳酸钙与稀盐酸反应:CO32-+2H+=CO2↑+H2O
B.金属钠与水反应:Na +2H2O=Na++2OH-+H2↑
C.氯气与水:Cl2+ H2O=2H++Cl-+ClO-
D.硫酸氢铵稀溶液和足量氢氧化钡溶液反应:NH4++H++ SO42-+Ba2++2OH-= BaSO4↓+NH3·H2O+H2O
难度: 中等查看答案及解析
-
下列实验操作及现象与结论之间对应关系错误的是( )
选项
实验操作及现象
结论
A
向某溶液中加入硝酸酸化的BaCl2溶液,有白色沉淀生成
该溶液中含SO42-
B
向某溶液中滴加NaOH浓溶液并加热,生成的气体能使湿润的红色石蕊试纸变蓝
该溶液中含NH4+
C
向某溶液中滴加KSCN溶液,无明显现象,再滴加少量氯水后,溶液变成红色
该溶液中含Fe2+
D
探究新制饱和氯水成分的实验时,向氯水中加入NaHCO3粉末,有气泡产生
氯水中含H+
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
少量Cl2通入NaOH稀溶液后所得的溶液中,主要含有Na+、Cl-、ClO-、OH-四种离子(除水分子外,其他微粒忽略不计),已知溶液中Na+和Cl-物质的量浓度分别为:c(Na+)=0.03mol·L-1、c(Cl-) =0.01mol·L-1,则溶液中c(OH-)为( )
A.0.03mol·L-1 B.0.02 mol·L-1 C.0.01 mol·L-1 D.0.005 mol·L-1
难度: 中等查看答案及解析
-
实验室有一包白色固体,可能含有Na2CO3、NaHCO3和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是( )
A.取一定量固体,溶解,向溶液中通入足量的CO2,没有固体析出,说明原固体中一定不含有Na2CO3
B.取一定量固体,溶解,向溶液中加入适量CaO粉末,有白色沉淀生成,说明原固体中一定含有Na2CO3
C.取一定量固体,溶解,向溶液中滴加适量AgNO3溶液,有白色沉淀生成,说明原固体中一定含有NaCl
D.取一定量固体,加热,将生成的气体通入澄清石灰水,石灰水变浑浊,说明原固体中一定含有NaHCO3
难度: 中等查看答案及解析