-
病毒无情,人间有情”,战疫当前,我国政府和人民为防控新冠病毒付出了巨大代价,为世界防疫工作作出了巨大贡献。以下做法涉及化学变化的是
A.
 搭建消毒棚
搭建消毒棚B.
 喷药消毒
喷药消毒C.
 穿戴防护服
穿戴防护服D.
 缝制棉被
缝制棉被难度: 简单查看答案及解析
-
“珍惜资源、爱护环境”是每位公民应尽的义务。下列相关做法不正确的是
A.我国拥有丰富的稀土资源,应科学规划,合理开采
B.提倡绿色出行,以减少化石燃料的使用
C.为减少白色污染,应停止使用塑料制品
D.利用熟石灰改良酸性土壤,以利于农作物生长
难度: 简单查看答案及解析
-
中学生正处在生长发育的关键时期,保持合理营养尤为重要。下列关于科学饮食的说法中正确的有
①维生素和水都是人体必须的营养素
②豆浆是富含蛋白质的食品
③锌、硒等元素是人体必须的微量元素,应大量服用含有这些元素的营养补剂
④骨头汤中含有钙元素,青少年可经常食用以防患佝偻病
⑤为预防甲状腺肿大,在食盐中添加大量的碘单质
A.①②④ B.②④⑤ C.①③④ D.①②④⑤
难度: 简单查看答案及解析
-
日前,科技部基础研究管理中心发布了 2019 年度中国科学十大进展。其中,阐明铕离子对提升钙钛矿太阳能电池寿命的机理入选。右图是铕元素在元素周期表中的相关信息, 下列说法正确的是
A.铕元素属于非金属元素
B.铕元素的质子数为 63
C.铕原子的中子数与核外电子数相等
D.铕元素的相对原子质量为152.0g
难度: 简单查看答案及解析
-
在国际大型体育比赛中,兴奋剂检测是对参赛运动员的一项重要检查。乙基雌烯醇是一种类固醇兴奋剂,其化学式为C20H32O。下列关于乙基雌烯醇的说法不正确的是
A.由 53个原子构成
B.属于有机化合物
C.相对分子质量为 288
D.氧元素质量分数最小
难度: 简单查看答案及解析
-
下列图示的实验操作正确的是
A.
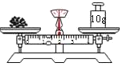 称量 10.25g 固体
称量 10.25g 固体B.
 测溶液的pH
测溶液的pHC.
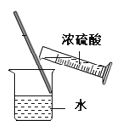 稀释浓硫酸
稀释浓硫酸D.
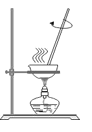 蒸发食盐水
蒸发食盐水难度: 简单查看答案及解析
-
我国科学家成功合成新型复合光催化剂,实现了太阳能人工光合成燃料,反应的微观示意图如图。下列说法正确的是
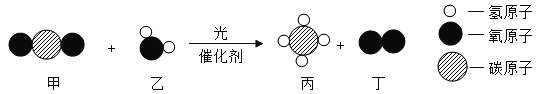
A.该反应涉及到 3 种含氧化合物
B.反应前后各元素的化合价均不变
C.参加反应的甲、乙分子个数比为 1∶1
D.该反应有利于节约化石燃料
难度: 简单查看答案及解析
-
建立模型是学习化学的重要方法下列建立的化学模型中不正确的是
A.
 充分燃烧模型
充分燃烧模型B.
铝离子模型
C.
 氧化反应和化合反应关系
氧化反应和化合反应关系D.
铁合金含碳量
难度: 简单查看答案及解析
-
逻辑推理可以实现知识迁移,下列推理正确的是
A.浓硫酸具有很强的吸水性,故可用于干燥所有气体
B.单质是由同种元素组成,故由同种元素组成的物质是单质
C.分子和原子都可以构成物质,故分子或原子都是可以保持物质化学性质的粒子
D.铝表面会形成氧化铝保护层,故铁制品表面的铁锈也可起到保护作用
难度: 简单查看答案及解析
-
如图是A、B、C 三种物质的溶解度曲线,下列叙述正确的是
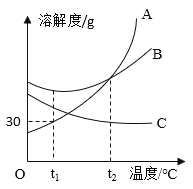
A.t1℃ 时,A 的饱和溶液溶质质量分数为30%
B.t 2℃ 时,将 A、B 溶液恒温蒸发等质量的水,析出晶体质量一定相等
C.将 C 的饱和溶液从t 2℃降低到t 1℃,其溶质的质量分数会变大
D.在接近饱和的B 溶液中混有少量A,通常采用蒸发溶剂的方法获得B
难度: 简单查看答案及解析