-
下列实验的操作或设计正确的是( )
A.药品取用:将试管竖直,垂直放入锌粒
B.区别物质:用pH试纸可以区别两种不同浓度的NaCl溶液
C.气体净化:除去CO2中混有的少量CO,可通入O2点燃
D.气体收集:CO2和O2密度比空气大,故都能用向上排空气法收集
难度: 简单查看答案及解析
-
每年的6月5日是世界环境日,2017年中国主题为“绿水青山就是金山银山”,强调尊重自然、自觉践行绿色生活。下列做法不符合这一主题的是
A. 生活垃圾分类处理 B. 大量使用一次性餐具
C. 购物时自带环保袋 D. 出行时选择公共交通工具
难度: 简单查看答案及解析
-
“牛肉粉”是某市的一道特色名小吃,其风味与众不同,汤鲜、味美、肉香,吃过的人赞不绝口。其牛肉中富含的营养素为( )

A.蛋白质 B.糖类
C.维生素 D.无机盐
难度: 简单查看答案及解析
-
2019年4月第二届“一带一路”国际合作高峰论坛在北京召开。“一带一路”是合作发展的理念和倡议,古丝绸之路将我国的发明和技术传送到国外。下列古代生产工艺中主要体现物理变化的是( )
A.粮食酿酒 B.烧制瓷器 C.纺纱织布 D.冶炼生铁
难度: 简单查看答案及解析
-
2019年7月,我省部分地区出现少量非洲猪瘟疫情,这种病原体中含有一种腺嘌呤核糖核苷酸载体目前难以攻克,目前世界卫生组织正在研究最新疫苗。腺嘌呤核糖核苷酸的化学式为C10H14O7N5P。腺嘌呤核糖核苷酸分子的下列叙述中不正确的是( )
A.每个腺嘌呤核糖核苷酸分子含有10个碳原子、14个氢原子、5个氮原子、1个磷原子和7个氧原子
B.每个腺嘌呤核糖核苷酸分子的质量为347
C.腺嘌呤核糖核苷酸是由五种元素组成
D.腺嘌呤核糖核苷酸中碳、氢、氧元素的质量比是60:7:56
难度: 简单查看答案及解析
-
对下列事实的解释错误的是( )
事 实
解 释
A
氢氧化钠溶液显碱性
溶液中含有氢氧原子
B
铁轨接头处留有一定的缝隙
原子之间有间隔
C
湿衣服晾
分子在不停运动
D
氯化钠固体不导电,溶液导电
固体中离子不能自由移动,溶液中离子能自由移动
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
活性炭可处理大气污染物NO,一定条件下的密闭容器中加入NO气体和活性炭,反应生成甲、乙气体,测得各物质如表所示,下列说法正确的是( )
反应时间min/
物质质量/g活性炭
NO
甲
乙
0
24.36
3
0
0
2
24
1.2
x
1.32
A.x的值为23.88
B.反应中活性炭只起吸附作用
C.反应中有元素化合价的升高和降低
D.生成甲、乙气体的分子数之比为1:2
难度: 简单查看答案及解析
-
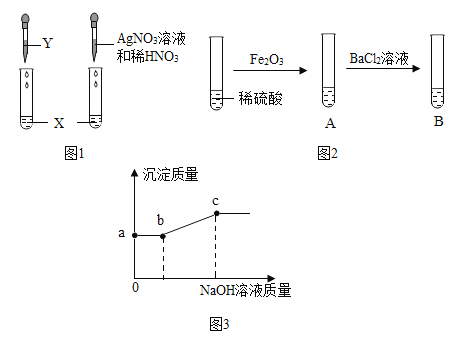
某干燥剂含有CaO、NaOH和CaCl2中的两种物质,为探究其成分,设计了如图所示实验.
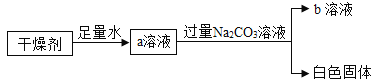
则下列说法正确的是( )
A.a、b溶液一定只含两种溶质
B.b溶液中一定有NaOH和Na2CO3
C.白色固体一定不是纯净物
D.干燥剂一定由NaOH和CaCl2组成
难度: 中等查看答案及解析
-
下表是不同温度时NaCl、KNO3的溶解度.则下列说法正确的是
温度/℃
0
20
40
60
80
溶解度/g
NaCl
35.7
36.0
36.6
37.3
38.4
KNO3
13.3
31.6
63.9
110
169
A.将60℃时KNO3的饱和溶液降温至20℃,溶质、溶剂的质量都会减少
B.将80℃时NaCl、KNO3两种饱和溶液降温至20℃,析出晶体的质量一定是:KNO3>NaCl
C.40℃时,将5g NaCl、5g KNO3分别加入10g水中,所得溶液的溶质质量分数不相等
D.用上表数据绘制成NaCl、KNO3的溶解度曲线,两条曲线交点对应的温度范围是0~20℃
难度: 中等查看答案及解析
-
已知某两种物质在一定条件下发生化学反应,其微观示意图如下图所示,下列说法不正确的是( )
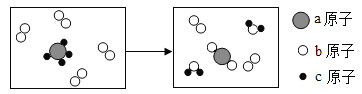
A.该反应中共涉及四种分子 B.该反应的反应物都是单质
C.该反应符合质量守恒定律 D.该反应中生成物都是化合物
难度: 简单查看答案及解析

 炒鸡蛋
炒鸡蛋  牛奶
牛奶  黄瓜
黄瓜