-
下列实验中所有可能失败的是
①为检验RX是碘代烷,将RX与NaOH水溶液混合加热后加AgNO3溶液
②为检验Fe(NO3)2样品是否变质取少量样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
③用锌和稀硝酸反应制取氢气用排水法收集氢气
④实验室制备硝基苯,加人试剂的顺序为:先加入浓硝酸,再滴加苯,最后滴加浓硫酸
⑤用苯和溴水在FeBr3催化下可制得溴苯
A.①②③④⑤ B.①④ C.②③④ D.③⑤
难度: 中等查看答案及解析
-
下列说法中错误的是
A.港珠澳大桥钢筋表面的环氧树脂涂层属于合成高分子材料
B.氨基酸残基在蛋白质肽链中的排列顺序为蛋白质的一级结构
C.“碳海绵”吸收泄露的原油时发生了化学变化
D.纤维素与浓硝酸在一定条件下反应可以得到硝化纤维
难度: 中等查看答案及解析
-
类比推理是化学中常用的思维方法,下列推理正确的是
A.乙醇、苯酚中都有羟基,推测两种有机物都可以与氢氧化钠反应。
B.苯不能使酸性高锰酸钾褪色,推测甲苯也不能使酸性高锰酸钾褪色
C.Cl2与NaOH常温下反应得到NaClO,推测F2与NaOH常温下反应得到NaFO
D.溴乙烷与氢氧化钠的醇溶液在加热时反应可以生成乙烯,推测溴丙烷可以与氢氧化钠的醇溶液在加热时能生成丙烯。
难度: 中等查看答案及解析
-
有机化合物萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是
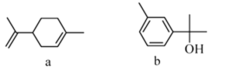
A.a和b均属于苯的同系物
B.a和b分子中所有碳原子均处于同一平面上
C.a和b均能使酸性KMnO4溶液褪色
D.1mol a物质与足量氢气加成,消耗的氢气为5mol
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法不正确的是
A.将3.4g H2S全部溶于水,所得溶液中HS-和S2-离子数之和为0.1NA
B.常温下1LpH=2的H3PO4溶液中含有的H+数目为0.01NA
C.将含有0.1molFeCl3的饱和溶液制成Fe(OH)3胶体,胶粒的数目小于0.1NA
D.400℃,1.01×105Pa,密闭容器中64gSO2与16g O2充分反应后,分子总数大于NA
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A.硫酸铝溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
B.二氧化硫与酸性高锰酸钾溶液反应:5SO2+2H2O+2MnO4-=2Mn2++5SO42-+4H+
C. Na2S2O3溶液与稀H2SO4反应的离子方程式:S2O32-+6H+=2S↓+3H2O
D.硫酸铜溶液中加少量的铁粉:3Cu2++2Fe=2Fe3++3Cu
难度: 中等查看答案及解析
-
短周期元素W、X、Y、Z的原子序数依次增加,W—与Ne具有相同的电子层结构,X的族序数等于周期数,Y与Z最外层电子数之和为10。下列说法不正确的是
A.原子半径:X>Y>Z>W B.W的单质可以与水反应产生氧气
C.气态氢化物的稳定性:W> Y > Z D.简单离子半径大小:Z>W>X
难度: 中等查看答案及解析
-
下列有关电解质溶液的说法正确的是
A.同温度下,CH3COONH4溶液显中性,所以CH3COONH4不水解。
B.在室温下稀释两种酸时pH变化如图,其中HX为弱酸,且a点与b点的
数值相同
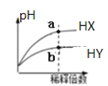
C.25℃时,等体积pH=3的HA和HB两种酸分别与足量的锌充分反应后,HA与Zn反应生成的氢气更多,HA是弱酸
D.若常温下,pH=3的HA溶液中水电离出的c(H+)为10-11mol·L-1,则能证明HA为弱酸。
难度: 中等查看答案及解析
-
某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.若向纯水中加入Na2S固体,抑制了水的电离
难度: 中等查看答案及解析
-
下表是25℃时弱酸的电离平衡常数,下列说法正确的是
CH3COOH
HClO
H2CO3
Ka=1.8×10—5
Ka=3.0×10—8
Ka1=4.1×10—7
Ka2=5.6×10—11
A.根据表中数据可知,相同浓度CH3COONa和NaClO的混合溶液中,各种离子浓度的大小关系是:c(Na+)>c(ClO﹣)>c(CH3COO﹣)>c(OH﹣)>c(H+)
B.根据表中数据可知,次氯酸钠溶液中通入少量CO2的离子方程式为:2ClO﹣+CO2+H2O=CO32﹣+2HClO
C.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中
减小
D.室温下,将碳酸钠溶液加热至70℃,溶液的中的OH—数目增多
难度: 中等查看答案及解析
-
在一个固定容积的密闭容器中,可逆反应:mA(g)+nB(g)
pC(g)+qD(g)中,当m、n、p、q为任意正整数时,达到平衡的标志是
A.气体分子的平均摩尔质量不再发生变化时 B.各组分的物质的量浓度不再改变
C.A与C的质量分数相等 D.反应速率vA∶vB∶vC∶vD=m∶n∶p∶q
难度: 中等查看答案及解析
-
下列能用勒夏特列原理解释的是
A.工业合成氯化氢时氢气过量
B.高温及加入催化剂都能使合成氨的反应速率加快
C.H2、I2、HI平衡时的混合气体加压后颜色变深
D.向饱和NaCl溶液中通入HCl,有晶体析出
难度: 中等查看答案及解析
-
三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料,在催化剂作用下可发生反应:2SiHCl3(g)
SiH2Cl2(g)+SiCl4(g),在50 ℃和70 ℃时SiHCl3的转化率随时间变化的结果如图所示。下列叙述正确的是

A.正反应方向为放热反应
B.反应速率大小:va <vb
C.70 ℃时,平衡常数K =
D.增大压强,可以提高SiHCl3的平衡转化率,缩短达平衡的时间
难度: 中等查看答案及解析
-
羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)
COS(g)+H2(g) K=0.1,反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A.CO的平衡转化率为20% B.升高温度,H2S浓度增加,表明该反应是吸热反应
C.反应前H2S物质的量为8mol D.通入CO后,正反应速率逐渐增大
难度: 中等查看答案及解析
-
下列有关同分异构体的说法正确的是
A.分子式为C5H10O2的有机物中含有
结构的同分异构体有12种
B.2-氯丁烷(CH3CHClCH2CH3)与NaOH乙醇溶液共热,得到三种烯烃。
C.有机物
的同分异构体中,其中属于酯且苯环上有2个取代基的同分异构体有2种。
D.甲醇在铜催化和加热条件下生成的产物不存在同分异构体。
难度: 中等查看答案及解析
-
下列有关实验方法和结论都正确的是
A.酸碱中和滴定时,锥形瓶需用待测液润洗2次,再加入待测液
B.检验蔗糖水解产物具有还原性:在蔗糖水解后的溶液中先加入适量稀NaOH溶液中和,再加入新制的银氨溶液并水浴加热
C.图中酸式滴定管读数为12.20 mL
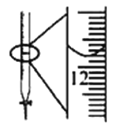
D.若用已知浓度的KMnO4溶液去测定某溶液中Fe2+浓度,KMnO4溶液放在碱式滴定管中
难度: 中等查看答案及解析
-
常温下,用浓度为
的盐酸分别逐滴加入到
的两种一元碱MOH、ROH溶液中,pH随盐酸溶液体积的变化如图所示.下列说法正确的是

A.
时,溶液中微粒浓度的关系是:
B.将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时,溶液中离子浓度的关系是:
C.
时,溶液中微粒浓度的关系是:
D.
时,不可能存在:
难度: 简单查看答案及解析
-
25℃,将浓度均为0.1mol/L的HA溶液Va mL和BOH溶液Vb mL混合,保持Va+Vb=100mL,生成物BA易溶于水。Va、Vb与混合液pH的关系如下图。下列叙述错误的是
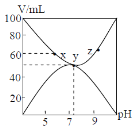
A.HA一定是弱酸
B.BOH可能是强碱
C.z点时,水的电离被促进
D.x、y、z点时,溶液中都存在c(A-)+c(OH-)=c(B+)+c(H+)
难度: 简单查看答案及解析

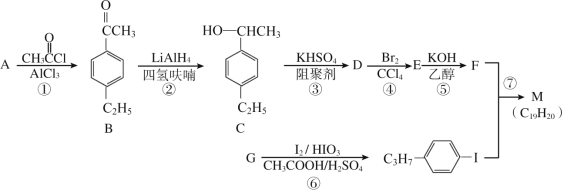
 有机物,需要_________和_____________两种有机物通过一步反应制得。(在横线上写出有机物的结构简式)
有机物,需要_________和_____________两种有机物通过一步反应制得。(在横线上写出有机物的结构简式)