-
下列气体过量排放不会导致酸雨的是
A.SO2 B.CO2 C.NO2 D.NO
难度: 简单查看答案及解析
-
当光束通过下列分散系时,能观察到丁达尔效应的是
A.NaCl溶液 B.Fe(OH)3胶体 C.Na2SO4溶液 D.蔗糖溶液
难度: 简单查看答案及解析
-
氯酸钾(KClO3)可用于制造烟花、安全火柴等,关于该物质的分类正确的是
A.盐 B.氧化物 C.酸 D.碱
难度: 简单查看答案及解析
-
下列物质属于电解质的是
A.Zn B.NaOH C.H2SO4溶液 D.MgCl2溶液
难度: 简单查看答案及解析
-
生石灰(CaO)可作食品干燥剂,属于碱性氧化物,不能与其发生反应的物质是
A.H2SO4 B.SO2 C.H2O D.NaOH
难度: 简单查看答案及解析
-
下列气体不能用排水法收集的是
A.SO2 B.NO C.O2 D.CO
难度: 简单查看答案及解析
-
下列关于氯气的说法不正确是
A.黄绿色 B.难溶于水 C.有刺激性气味 D.有毒
难度: 简单查看答案及解析
-
下列关于钠的说法不正确的是
A.银白色柔软 B.密度比水小
C.与水反应生成氢气 D.在空气中燃烧生成氧化钠
难度: 简单查看答案及解析
-
下列有关试剂的保存方法不正确的是
A.Na保存于煤油中 B.过氧化钠应密封保存
C.浓硝酸保存于无色试剂瓶中 D.浓硫酸保存于铁质容器中
难度: 简单查看答案及解析
-
下列物质的用途不正确的是
A.SO2可用于漂白纸张 B.浓硫酸具有吸水性用作干燥剂
C.Na2CO3受热易分解用作膨松剂 D.Na2O2用于呼吸面具供氧
难度: 简单查看答案及解析
-
在含有大量的OH-、K+、Cl-的溶液中,还可能大量共存的离子是
A.SO42- B.H+ C.Ag+ D.Mg2+
难度: 简单查看答案及解析
-
实现下列变化需要加入氧化剂的是
A.Cl2→Cl- B.H+→H2 C.CO32-→CO2 D.CO→CO2
难度: 简单查看答案及解析
-
Na2SO3与下列物质的反应中,体现的性质与其他3个反应不同的是
A.盐酸 B.Ca(OH)2 C.BaCl2 D.O2
难度: 中等查看答案及解析
-
下列说法中,正确的是
A.36 g H2O的物质的量为1 mol
B.常温常压下,1mol Cl2的体积是22.4 L
C.1molCO2中含有的分子数约为6.02×1023
D.0.5mol·L-1MgCl2溶液中Cl-为0.5 mol·L-1
难度: 中等查看答案及解析
-
下列试剂能用于鉴别CO2和SO2的是
A.BaCl2溶液 B.NaOH溶液
C.澄清石灰水 D.酸性高锰酸钾溶液
难度: 中等查看答案及解析
-
下列解释实验事实的离子方程式不正确的是
A.向铜粉中滴加稀HNO3溶液,产生气体:Cu + 2H+ = Cu2+ + H2↑
B.向FeCl2溶液中通入氯气,溶液变为黄色:2Fe2+ + Cl2 = 2Fe3+ + 2Cl-
C.向CuSO4溶液中滴加NaOH溶液,生成沉淀:Cu2+ + 2OH-= Cu(OH)2↓
D.Fe(OH)2由白色变灰绿,最后变为红褐色:4Fe(OH)2 + O2+2H2O = 4 Fe(OH)3
难度: 简单查看答案及解析
-
瑞典化学家舍勒在研究软锰矿矿石时,把浓盐酸和软锰矿矿石混合加热,意外得到了氯气,MnO2 + 4HCl(浓)
MnCl2 + Cl2 ↑+ 2H2O 关于该反应的叙述不正确的是
A.MnO2是氧化剂 B.HCl具有还原性
C.MnO2被HCl还原 D.氧化剂与还原剂的物质的量之比为1:4
难度: 中等查看答案及解析
-
如图是喷泉实验装置图,下列说法不正确的是

A.烧瓶中的溶液呈红色
B.该实验说明氨气可电离产生OH-
C.该实验说明氨气易溶于水
D.形成喷泉的原因是烧瓶内压强小于外界大气压
难度: 中等查看答案及解析
-
某工业废水中存在大量的Na+、Cl-、Cu2+、SO42-,欲除去其中的Cu2+、SO42-,设计工艺流程如图所示:

下列说法不正确的是
A.NaOH的作用是除去Cu2+ B.试剂a 为Na2CO3,试剂b为BaCl2
C.流程图中,操作x为过滤 D.试剂c为盐酸
难度: 中等查看答案及解析
-
下列实验所得结论不正确的是
实验Ⅰ
实验Ⅱ
实验Ⅲ
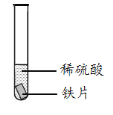


产生大量无色气体
铁片表面迅速变暗,之后无明显变化
加热后产生大量无色有刺激性气味的气体
A.实验Ⅰ中气体是H2 B.实验Ⅱ中没有发生化学反应
C.实验Ⅲ中气体是SO2 D.浓度、温度影响实验现象
难度: 中等查看答案及解析
-
下列“解释或结论”与“实验操作及现象”不相符的一组是
序号
实验操作及现象
解释或结论
A
浓硫酸滴到纸张上,纸变黑
浓硫酸有脱水性
B
向紫色石蕊溶液中加入氯水,溶液先变红,随后褪色
氯水中含有酸性物质和
漂白性物质
C
向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体
该溶液中一定有CO32-
D
向某溶液中加入浓NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体
该溶液中一定含有NH
A.A B.B C.C D.D
难度: 中等查看答案及解析



