-
同种元素的不同核素之间互称同位素,下列各组中互为同位素的是( )
A. D和T B. 40Ca和40Ar C. H2O和H2O2 D. O2和O3
难度: 简单查看答案及解析
-
下列关于Fe(OH)3胶体的说法中,不正确的是 ( )
A. 分散质粒子直径在10-9~10-7m之间 B. 是一种纯净物
C. 具有丁达尔效应 D. 具有净水作用
难度: 简单查看答案及解析
-
化学与科学、技术、社会、环境密切相关,下列有关说法中错误的( )
A. 春节燃放的焰火是某些金属元素焰色反应所呈现出来的色彩
B. 明矾可用于自来水的杀菌消毒
C. 过氧化钠可以用作潜艇或者宇宙飞船的供氧剂
D. 有色玻璃就是由某些胶态金属氧化物分散于玻璃中制成的
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 镁着火时可用二氧化碳灭火器灭火
B. 生物炼铜就是利用特殊的细菌将硫化铜直接转化为铜
C. 现代化学分析测试中,常借助一些仪器来分析化学物质的组成。如用原子吸收光谱确定物质中含有哪些金属元素
D. 铝比铁活泼,所以铝制品比铁制品更容易被腐蚀
难度: 简单查看答案及解析
-
设NA为阿伏伽德罗常数的值,下列说法中正确的是( )
A.0.1molNa2O和Na2O2固体混合物中含有的阴阳离子总数大于0.3NA
B.5.6g铁与足量的氯气反应,转移的电子数为0.2NA
C.1.8g D2O中含有的中子数为NA
D.1L 1mol/L的CH3COOH溶液中CH3COO−离子的数目小于NA
难度: 中等查看答案及解析
-
实验室用碳酸钠晶体配制1.00mol/L的Na2CO3溶液100mL,造成所配溶液浓度偏高的原因是( )
A. 烧杯和玻璃棒没有洗涤
B. 向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤
C. 定容时俯视刻度线
D. 称量碳酸钠晶体(Na2CO3⋅10H2O)的烧杯未干燥
难度: 简单查看答案及解析
-
己知在碱性溶液中可发生如下反应:
2R(OH)3+ 3C1O-+ 4OH-= 2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是( )
A.+3 B.+4 C.+5 D.+6
难度: 简单查看答案及解析
-
某温度下,将氯气通入氢氧化钾溶液中,反应后得到氯化钾,次氯酸钾,氯酸钾的混合溶液,经测定ClO−与ClO3−离子的物质的量的浓度之比为1:2,则氯气与氢氧化钾反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为( )
A. 10:3 B. 11:3 C. 2:3 D. 4:3
难度: 中等查看答案及解析
-
下列各组离子在指定溶液中可能大量共存的是( )
A. 能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、Cl−、I−
B. 能使酚酞变红的溶液:Mg2+、Fe3+、Na+、ClO−
C. 含有大量 Fe2+的溶液:Na+、NH4+、SO42−、OH−
D. 加入铝粉有氢气放出的溶液:K+、Cu2+、SO42−、Cl−
难度: 中等查看答案及解析
-
下列离子方程式中正确的是( )
A. 稀硫酸滴加在铜片上:Cu + 2H+ = Cu2+ + H2↑
B. 氧化铁粉末溶于稀盐酸:Fe2O3 + 6H+ = 2Fe3+ + 3H2O
C. 硫酸滴加到氢氧化钡溶液中:H+ + SO42− + Ba2+ + OH− = H2O + BaSO4↓
D. 碳酸氢钠和醋酸反应:HCO3− + 2H+ = CO2↑ + H2O
难度: 中等查看答案及解析
-
在含有Fe3+、Fe2+、Al3+、Na+的溶液中,加入足量的Na2O2固体,充分反应后,再加入过量的稀盐酸,完全反应后,溶液中离子数目几乎没有变化的是( )
A.Fe3+ B.Fe2+ C.Al3+ D.Na+
难度: 中等查看答案及解析
-
周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中的铜绿指的是( )
A. Cu2(OH)2CO3 B. Cu(OH)2 C. CuO D. Cu2O
难度: 简单查看答案及解析
-
下列是某兴趣小组根据课本实验设计的一个能说明Na2CO3与NaHCO3热稳定性的套管实验。请观察下图的实验装置、分析实验原理,下列说法错误的是( )

A. 甲为小苏打,乙为纯碱
B. 要证明NaHCO3受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C. 整个实验过程中可以看到丙烧杯的澄清石灰水没变浑浊
D. 同质量的甲和乙分别与足量的盐酸完全反应,产生二氧化碳的质量:乙>甲
难度: 中等查看答案及解析
-
下列各组物质中,将前者加入后者时,无论前者是否过量,都能用同一个化学方程式表示的是( )
A. 盐酸 Na2CO3溶液 B. 氢氧化钠溶液 AlCl3溶液
C. Cl2 铁粉 D. CO2 澄清石灰水
难度: 中等查看答案及解析
-
向以下六种饱和溶液中分别持续通入CO2,最终可以得到沉淀或者析出晶体的一组是( )
①Na2CO3 ②Ca(OH)2 ③ CaCl2 ④NaAlO2 ⑤NaCl和NH3
A. ①④⑤ B. ①②④⑤ C. ①②③④ D. ①②④
难度: 中等查看答案及解析
-
等物质的量过氧化钠与碳酸氢钠固体混合后,在密闭容器中充分加热。排出气体物质后冷却,残留固体可能是( )
A. Na2CO3 B. Na2CO3 NaOH C. NaOH D. Na2O2 NaOH
难度: 中等查看答案及解析
-
下列物质中,既能跟稀硫酸反应,又能跟NaOH溶液反应的化合物是( )
①Al2O3 ②Mg(OH)2 ③Al(OH)3 ④NaHCO3 ⑤AlCl3 ⑥Al
A. ①③④⑥ B. ①③④⑤⑥ C. ①③④ D. ①②③④⑤⑥
难度: 中等查看答案及解析
-
用铝热法还原下列物质,用等物质的量的铝,制得金属物质的量最少的是( )
A. MnO2 B. Fe3O4 C. Cr2O3 D. V2O5
难度: 中等查看答案及解析
-
下列实验操作中错误的是( )
A. 蒸发操作时,不能使混合物中的水分完全蒸干后,再停止加热
B. 蒸馏操作时,应使温度计水银球插入液面以下
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 萃取操作时,选择的萃取剂不能与原溶剂互溶。
难度: 简单查看答案及解析
-
有4瓶常用溶液:①BaCl2溶液,②NaCl溶液,③Na2SO4溶液,④CuSO4溶液。不用其他试剂,可通过实验方法将它们一一鉴别开来,鉴别出来的先后顺序是( )
A. ④③①② B. ①③④② C. ④①③② D. ①④②③
难度: 中等查看答案及解析
-
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为( )
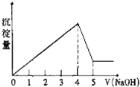
A. 1:1 B. 2:1 C. 3:1 D. 1:2
难度: 中等查看答案及解析
-
向一定量的Fe、FeO、Fe2O3的混合物中加入100mL浓度为2.0mol⋅L−1的盐酸,恰好使混合物完全溶解,放出224mL的气体((标准状况)),所得溶液中加入KSCN溶液后无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是( )
A. 11.2g B. 5.6g C. 2.8g D. 1.4g
难度: 中等查看答案及解析