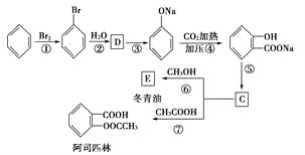
-
波音787型飞机的机身和机翼大量使用下列哪种材料( )
A. 液晶高分子材料 B. 橡胶
C. 高分子分离膜 D. 碳纤维复合材料
难度: 简单查看答案及解析
-
下列关于乙酸的说法正确的是( )
A.难溶于水 B.是一种无色无味液体
C.能发生酯化反应 D.酸性比碳酸的酸性弱
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.淀粉和油脂都是天然高分子化合物
B.由乙醇消去制乙烯和乙烯与水反应制乙醇属于同一反应类型
C.由溴乙烷水解制乙醇、乙酸和乙醇制乙酸乙酯属于同一反应类型
D.石油分馏得到乙烯、丙烯、丁二烯等有机物
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.H2N﹣CH2﹣COOH 能与酸、碱反应生成盐
B.葡萄糖既能发生银镜反应,又能发生水解反应
C.浓硝酸和醋酸铅溶液均可使鸡蛋清溶液中的蛋白质变性
D.1 mol油脂完全水解的产物是1 mol甘油和3 mol 高级脂肪酸(或盐)
难度: 中等查看答案及解析
-
将1 mol两种气态烃组成的混合气体完全燃烧后得到1.5 mol CO2和2 mol H2O。下列说法正确的是
A.一定有乙烷 B.一定有甲烷
C.一定没有甲烷 D.不一定有甲烷
难度: 中等查看答案及解析
-
能证明苯酚具有弱酸性的实验是( )
A.加入浓溴水生成白色沉淀 B.苯酚钠溶液中通入CO2后,溶液由澄清变浑浊
C.浑浊的苯酚加热后变澄清 D.苯酚的水溶液中加NaOH溶液,生成苯酚钠
难度: 中等查看答案及解析
-
在盛有稀硫酸的烧杯中,放入用导线连接的铜片和锌片,下列正确的是( )
A. 正极附近的SO42-离子浓度逐渐增大
B. 电子通过导线由铜片流向锌片
C. 正极有氧气逸出
D. 铜片上有氢气逸出
难度: 中等查看答案及解析
-
用下图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是

A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H2O
C.阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH-
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ = N2↑ + 2CO2↑ + 5Cl-+ H2O
难度: 困难查看答案及解析
-
有关下图所示化合物的说法不正确的是

A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1mol该化合物最多可以与3mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
难度: 中等查看答案及解析
-
下列关于酸碱中和滴定的叙述中,正确的是( )
A.进行酸碱中和滴定实验时,盛装待测液的锥形瓶使用前应先用待测液润洗
B.滴定前应排除尖嘴部分的气泡
C.滴定过程中两眼应注视滴定管内液面变化
D.锥形瓶内溶液颜色突变说明到达滴定终点
难度: 简单查看答案及解析
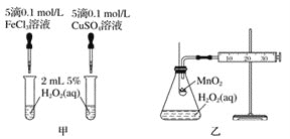
-
现用Pt电极电解1 L浓度均为0.1 mol·L-1的HCl、CuSO4的混合溶液,装置如图,下列说法正确的是( )

A.电解开始时阴极有H2放出
B.电解开始时阳极上发生:Cu2++2e-Cu
C.整个电解过程中,SO42-不参与电极反应
D.当电路中通过电子的量超过0.1 mol时,此时阴极放电的离子发生了变化
难度: 中等查看答案及解析
-
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯。用如图所示装置探究废旧塑料的再利用。下列叙述中不正确的是( )
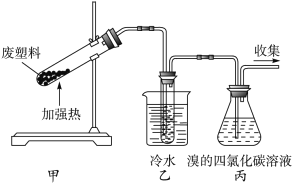
A.聚丙烯的链节是—CH2—CH2—CH2—
B.装置乙的试管中可收集到芳香烃
C.装置丙中的试剂可吸收烯烃以制取卤代烃
D.最后收集的气体可作燃料
难度: 中等查看答案及解析
-
禁止运动员使用兴奋剂是2012绿色奥运的重要举措之一,下图是兴奋剂利尿酸的结构

关于它的说法正确的是
A.利尿酸的化学式为:C13H14O4Cl2
B.利尿酸最多可与4 molH2发生反应
C.利尿酸可使溴的四氯化碳溶液褪色
D.利尿酸在一定条件下能发生消去反应
难度: 困难查看答案及解析
-
某溶液中由水电离出的c(H+)=10-10mol·L-1,那么该溶液的pH可能为( )
A.10 B.4 C.10或4 D.11
难度: 简单查看答案及解析
-
在常温下,将pH=8的NaOH溶液与pH=10的NaOH溶液等体积混合后,溶液的pH最接近于:
A.8.3 B.8.7 C.9 D.9.7
难度: 中等查看答案及解析
-
已知:25°C时,
,
。下列说法正确的是
A.25°C时,饱和
溶液与饱和
溶液相比,前者的
大
B.25°C时,在
的悬浊液加入少量的
固体,
增大
C.25°C时,
固体在20ml0.01 mol·
氨水中的
比在20mL0.01mol·
溶液中的
小
D.25°C时,在
的悬浊液加入
溶液后,
不可能转化成为
难度: 中等查看答案及解析
-
国际能源网报道:金属燃料可能成为新能源,可能带来结束化石能源时代的希望,是一种理想的储能方式。下列说法不正确的是( )
A.钠米金属燃料,更易点燃
B.铁作燃料时,可用磁性材料吸引生成物,便于产物分离
C.镁可以通过2Mg+CO2=2MgO+C,达到既节能减碳又释放能量的效果
D.可从海水中提取氯化镁,并使氯化镁分解获得镁并释放出能量
难度: 简单查看答案及解析
-
美国科学家罗伯特•莱夫科维茨和布莱恩•克比尔卡因“G 蛋白偶联受体研究”而获得2012年诺贝尔化学奖,他们将碘的同位素附着到各种激素上,借助放射学找到一些受体,进一步研究出“G 蛋白偶联受体”发挥的作用和机理,下列有关说法正确的是( )
A.放射性同位素
I 原子核内中子数与质子数的差为 78
B.蛋白质是生物体维持生命活动所需能量的主要来源
C.动物蛋白质和植物蛋白质混合摄入,更能增强蛋白质的营养作用
D.“春蚕到死丝方尽,蜡烛成灰泪始干”其中的“丝”和“泪”化学成分都是蛋白质
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.光导纤维、棉花、油脂、ABS树脂都是由高分子化合物组成的物质
B.开发核能、太阳能等新能源,推广基础甲醇汽油、使用无磷洗涤剂都可直接降低碳排放
C.红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析
D.通电时,溶液中的溶质离子分别向两极移动,胶体中的分散质粒子向某一极移动
难度: 简单查看答案及解析
-
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
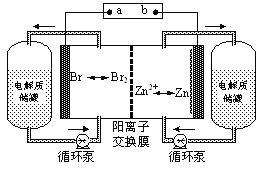
A.充电时电极a连接电源的负极
B.放电时负极的电极反应式为Zn—2e-=Zn2+
C.放电时左侧电解质储罐中的离子总浓度增大
D.阳离子交换膜可阻止Br2与Zn直接发生反应
难度: 困难查看答案及解析
-
盖斯定律在生产和科学研究中有很重要的意义。已知3.6g碳在6.4g氧气中燃烧,至反应物耗尽,放出了X kJ热量。已知碳完全燃烧的焓变△H= 一Y kJ·mol-1,则lmol C与O2反应生成CO的反应热△H为 ( ) kJ·mol-1
A.一Y B.—(10X—Y) C.一(5X—0.5Y) D.+(10X—Y)
难度: 中等查看答案及解析
-
下列有关化学反应速率的说法不正确的是( )
A.化学反应达到最大限度时,正逆反应速率也达到最大且相等
B.催化剂能降低化学反应的活化能,加快反应速率,提高生产效率
C.用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率
D.用铁片和稀硫酸反应制H2比用98%的浓硫酸产生H2的速率快
难度: 中等查看答案及解析
-
下图有机物的正确命名为 ( )

A.2-乙基-3,3-二甲基戊烷 B.3,3-二甲基-4-乙基戊烷
C.3,3,4-三甲基己烷 D.3,4,4-三甲基己烷
难度: 简单查看答案及解析
-
对如图有机物的叙述,正确的是( )

A. 该有机物的分子式为C18H15O
B. 该有机物中共线的碳原子最多有7个
C. 该有机物中共面的碳原子最多有17个
D. 该有机物在常温下易溶于水
难度: 中等查看答案及解析
-
将相同的物质的量浓度的某弱酸HX溶液与NaX溶液等体积混合后,测得混合后溶液中c(Na+)>c(X-),则下列关系错误的是( )
A.c(H+)<c(OH-) B.c(HX )<c(X-)
C.c(X-)+c(HX)=2c(Na+) D.c(X-)-c(HX)=2[c(H+)-c( OH-)]
难度: 简单查看答案及解析
-
在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表,v 的单位为(mmol·L-1·min-1)。下列判断错误的是
c(mol·L-1)
T / K0.600
0.500
0.400
0.300
318.2
3.60
3.00
a
1.80
328.2
9.00
7.50
6.00
4.50
b
2.16
1.80
1.44
1.08
A.318.2K,蔗糖起始浓度为0.400 mol·L-1,10min后蔗糖浓度略大于0.376 mol·L-1
B.b K时,若蔗糖的浓度为0.35 mol·L-1,则v = 1.26 mmol·L-1·min-1
C.b < 318.2
D.若同时改变反应温度和蔗糖的浓度,则v肯定变化
难度: 困难查看答案及解析
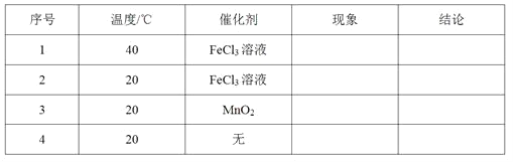


 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。