-
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是( )
A. 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B. 在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3提供空轨道
C. 向反应后的溶液加入乙醇,溶液没有发生变化
D. 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+
难度: 中等查看答案及解析
-
下列晶体熔化时不需要破坏化学键的是
A.晶体硅 B.食盐 C.干冰 D.金属钾
难度: 简单查看答案及解析
-
下列叙述中正确的是
A.NH3、CO、CO2 都是极性分子
B.CH4、CCl4 都是含有极性键的非极性分子
C.HF、HCl、HBr、HI 的稳定性依次增强
D.CS2、H2O、C2H2 都是直线形分子
难度: 中等查看答案及解析
-
下列分子中存在π键的是
A.H2 B.Cl2 C.N2 D.HCl
难度: 中等查看答案及解析
-
下列说法中正确的是 ( )
A.第3周期所包含的元素中钠的第一电离能最大
B.铝的第一电离能比镁的第一电离能大
C.在所有元素中,氟的电负性最大
D.钾的第一电离能比镁的第一电离能大
难度: 简单查看答案及解析
-
以下能级符号错误的是( )
A.6s B.2d C.3p D.4f
难度: 简单查看答案及解析
-
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
A.X与Y形成化合物时,X显负价,Y显正价
B.第一电离能可能Y小于X
C.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性
D.气态氢化物的稳定性:HmY小于HmX
难度: 简单查看答案及解析
-
用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是( )
A. 直线形;三角锥形 B. V形;三角锥形
C. 直线形;平面三角形 D. V形;平面三角形
难度: 中等查看答案及解析
-
下列分子中所有原子都满足最外层为8电子结构的是( )
A. SiCl4 B. H2O C. BF3 D. PCl5
难度: 中等查看答案及解析
-
下列分子中心原子是sp2杂化的是( )
A.PBr3 B.CH4 C.BF3 D.H2O
难度: 简单查看答案及解析
-
下列物质熔沸点高低的比较,正确的是
A.SiO2<CO2 B.CCl4<CF4 C.HF>HI D.NaCl<HCl
难度: 简单查看答案及解析
-
下列分子或离子中,能提供孤电子对与某些金属离子形成配位键的是( )
①H2O ②NH3 ③F- ④CN- ⑤CO
A.①② B.①②③ C.①②④ D.①②③④⑤
难度: 中等查看答案及解析
-
下列有关化学用语正确的是 ( )
A.某元素原子的轨道排布式
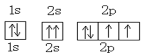
B.H2O电子式为
C.Ca2+离子基态电子排布式为1s22s22p63s23p64s2
D.钾原子的原子结构示意图为
难度: 简单查看答案及解析
-
下列有关物质性质的比较顺序中,不正确的是( )
A. 热稳定性:HF<HCl<HBr<HI B. 微粒半径:K+>Na+>Mg2+>Al3+
C. 酸性:HClO4>H2SO4>H3PO4>H2SiO3 D. 熔点:Li>Na>K>Rb
难度: 中等查看答案及解析
-
下列粒子属等电子体的是( )
A.NO和O2 B.CH4和NH4+ C.NH2ˉ 和H2O2 D.HCl和H2O
难度: 中等查看答案及解析
-
下列事实与氢键有关的是 ( )
A.水加热到很高的温度都难以分解
B.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增加而升高
C.HF、HCI、HBr、HI的热稳定性依次减弱
D.水结冰成体积膨胀,密度减少
难度: 简单查看答案及解析