-
几种短周期元素的原子半径及主要化合价如下表:
元素代号
X
Y
Z
W
原子半径/pm
160
143
70
66
主要化合价
+2
+3
+5、+3、-3
-2
下列叙述正确的是
A.X、Y元素的金属性X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
难度: 中等查看答案及解析
-
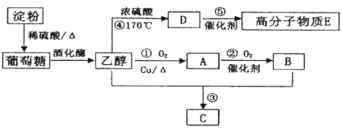
下列说法正确的是( )
A.淀粉与纤维素通式都是
,二者互为同分异构体
B.甲烷、苯、葡萄糖均不能使酸性高锰酸钾溶液褪色
C.油脂都是纯净物
D.可通过反应后的溶液不分层,判断油脂的皂化反应基本完成
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A. 铊与铝同主族,氧化铝是两性氧化物,所以氧化铊也是两性氧化物
B. 第三周期简单离子的半径从左到右依次减小
C. 用电子式表示HCl的形成过程
D. 在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料
难度: 中等查看答案及解析
-
下列叙述不正确的是( )
A.苯乙烯分子中所有原子可能共平面
B.苯、乙酸、乙醇均能发生取代反应
C.分子式为
的同分异构体共有5种(不考虑立体异构)
D.可用溴的四氯化碳溶液区分
和
难度: 中等查看答案及解析
-
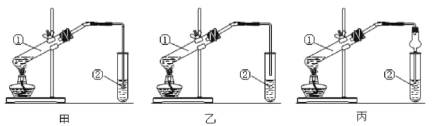
下列有关乙烯化学性质的说法,错误的是( )
A.乙烯能使酸性高锰酸钾溶液褪色,是由于乙烯发生了氧化反应
B.乙烯可在氧气中燃烧,该反应属于乙烯的氧化反应
C.将乙烯通入溴水中,反应后得到均一、透明的液体
D.乙烯能使溴的四氯化碳溶液褪色,该反应属于加成反应
难度: 简单查看答案及解析
-
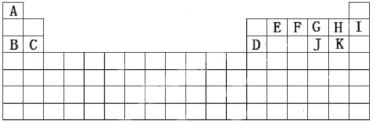
如图为元素周期表前四周期的一部分。 X 原子最外层电子数是其内层电子数的3倍。下列说法正确的是
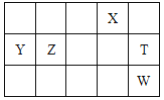
A. TX2、T2 或X3均可用于做杀菌消毒
B. W元素的单质溶于水和汽化都只破坏了分子间作用力
C. 元素T 的非金属性比W强,所以HT的酸性比HW的酸性强
D. YT3在常压、 178℃时升华,所以 YT3 中只含有离子键,而 ZT4中只含有共价键
难度: 中等查看答案及解析
-
已知
键可以旋转,下列对结构简式为
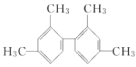 的烃的说法正确的是( )
的烃的说法正确的是( )A.该烃属于苯的同系物
B.分子中至少有11个碳原子处于同一平面上
C.分子中至少有10个碳原子处于同一平面上
D.分子中至少有9个碳原子处于同一平面上
难度: 中等查看答案及解析
-
下列有机物的鉴别中,所选用的试剂及产生的现象不完全正确的是( )
选项
有机物
试剂
现象
A
乙烯
溴水
橙色褪去
B
葡萄糖
新制氢氧化铜悬浊液
出现红色沉淀
C
淀粉
碘水
出现蓝色沉淀
D
蛋白质
浓硝酸
呈黄色
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
可逆反应达到最大反应限度的本质特征是( )
A.正反应不再继续进行
B.正反应和逆反应都在继续进行
C.各物质反应速率之比等于其化学计量数之比
D.正反应和逆反应的速率相等
难度: 简单查看答案及解析
-
反应3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g)在一可变容积的容器中进行,下列条件的改变对其反应速率几乎没有影响的是( )
A.增加Fe 的用量
B.将容器的体积缩小一半
C.保持体积不变,充入H2O(g)使体系压强增大
D.保持压强不变,充入N2使容器体积增大
难度: 中等查看答案及解析
-
少量铁粉与
的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变
的产量,可以使用如下方法中的( )
①加水 ②加
固体 ③滴入几滴浓盐酸 ④加
固体 ⑤加
溶液 ⑥滴入几滴硫酸铜溶液 ⑦适当升高温度(不考虑盐酸挥发)
A.①⑥⑦ B.③⑦ C.③⑤ D.⑤⑦
难度: 简单查看答案及解析
-
对可逆反应A(g)+B(g)
2C(g)+D(s)△H>0,向1L绝热容器中加入1molA和1mol B发生反应,下列叙述不能作为该反应达到平衡状态的标志的是( )
①单位时间内消耗amolA,同时生成2amolC
②混合气体的总压强不再变化
③混合气体的密度不再变化
④A、B、C的分子数之比为1∶1∶2
⑤反应容器中温度不变
⑥A的转化率与B的转化率相等时
A.①②④⑥ B.②④⑥ C.①④⑥ D.①②⑥
难度: 中等查看答案及解析
-
下图是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )
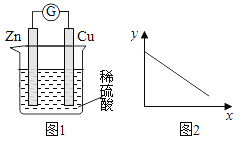
A.c(H+) B.V(H2) C.m(溶液) D.m(Cu)
难度: 中等查看答案及解析
-
分子式为
且分子结构中含有2个甲基的有机物共有( )
A.2种 B.3种 C.4种 D.5种
难度: 中等查看答案及解析
-
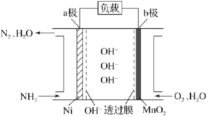
是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的
,又可以生成一定量的硫酸,下列说法不正确的是( )

A.a为负极,b为正极
B.从左下口流出的硫酸的质量分数一定大于50%
C.生产过程中氢离子由左移向右
D.负极反应式为SO2+2H2O-2e-=SO42—+4H+
难度: 中等查看答案及解析
-
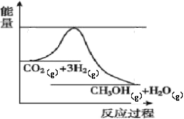
绝热恒容密闭容器中发生反应:
。一定条件下,向容器中通入
和
达平衡,正反应速率随时间变化如图所示。正确的结论是( )
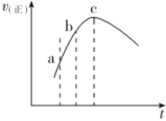
A.逆反应速率:a点小于c点
B.反应物浓度:a点小于b点
C.反应在c点时
的转化率最大
D.反应物的总能量低于生成物的总能量
难度: 中等查看答案及解析
-
下列有关除杂质(括号中为杂质)的操作中,错误的是( )
A.乙醇(水):加入足量生石灰充分振荡,蒸馏,收集馏出物
B.
(乙醇):多次加水,振荡,分液,弃水层
C.
(
):通入足量的高锰酸钾溶液
D.乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层
难度: 中等查看答案及解析
-
下列说法正确的是( )
①若
和
的电子层结构相同,则原子序数:
②
、
、
、
熔点随相对分子质量增大而升高
③
、
、
、
分子中所有原子都满足8电子结构
④干冰升华不会破坏共价键
⑤
分子很稳定是由于
分子之间能形成氢键
A.②④ B.①②④ C.②④⑤ D.③④⑤
难度: 中等查看答案及解析
-
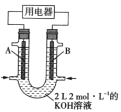
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓
溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化)( )

A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
D.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
难度: 中等查看答案及解析
-
W、X、Y、Z四种短周期元素的原子序数依次增大,W的某种原子无中子,X、Y可形成原子个数比为
的具有漂白性的物质,工业上常用电解饱和
溶液来获得Z的单质及其他产品。下列说法正确的是( )
A.W和X 、Y 、Z均能形成18电子的分子
B.X 、Y 之间形成的化合物可能同时含有离子键和非极性共价健
C.上述四种元素的原子半径大小顺序为
D.W、X 、Z三种元素形成的化合物一定是弱酸
难度: 中等查看答案及解析