-
化学与生活密切相关。下列说法正确的是( )
A.可以注射消毒液杀灭人体内的新型冠状病毒
B.干粉灭火器主要用于扑救有机溶剂、可燃气体和电气设备的初期火灾
C.家蚕丝心蛋白水解生成的甘氨酸和丙氨酸共能形成3种二肽
D.骨水泥(骨粘固剂)的主要成分聚甲基丙烯酸甲酯的单体是甲基丙烯酸和甲醇
难度: 简单查看答案及解析
-
下列说法错误的是( )
A.棉花、麻、羊毛、蚕丝都属于天然纤维
B.可用热的NaOH溶液鉴别地沟油和汽油
C.甲苯、间二甲苯的一氯代物种数相同
D.
 的不饱和度是6,核磁共振氢谱有2组峰
的不饱和度是6,核磁共振氢谱有2组峰难度: 简单查看答案及解析
-
下列说法错误的是( )
A.基态Cr原子有6个未成对电子
B.PH3和NH3分子中均含有孤电子对,且PH3提供孤电子对的能力强于NH3
C.BeO的晶格能大于MgO,可推测BeCO3的分解温度低于MgCO3
D.向1mol配合物
中加入足量AgNO3溶液,可以得到3molAgCl沉淀
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4L15NH3中含有的质子数为11NA
B.含63gHNO3的浓硝酸与足量铜完全反应,转移电子数大于0.5NA
C.常温下,1L
溶液中含有的氮原子数小于0.2NA
D.标准状况下,224mLSO2溶于水后形成的溶液中
、
、
粒子数之和等于0.01NA
难度: 中等查看答案及解析
-
近年来被网络炒得火热的抗衰老“神药”白藜芦醇结构简式如图所示,下列关于白藜芦醇说法错误的是( )
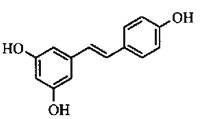
A.分子式为C14H12O3 B.存在顺反异构
C.所有碳原子可能共平面 D.属于醇类,能发生加成反应、取代反应
难度: 简单查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大,K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法错误的是( )
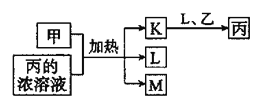
A.X、Y、Z三种元素的第一电离能:
B.X分别与Y、Z、W形成的分子中均可能含有非极性共价键
C.Z元素的最高价含氧酸的酸性在同周期和同主族元素中均最强
D.若固体
是由直线形的
和平面三角形的
组成,则
与丙溶液中的溶质阴离子相同
难度: 困难查看答案及解析
-
下列离子方程式书写正确的是( )
A.少量SO2通入BaCl2溶液中:
B.
与足量盐酸反应:

C.
中加入
酸化的KMnO4:
D.向NaClO和NaCl混合溶液中滴入少量FeSO4溶液:
难度: 中等查看答案及解析
-
下列选用的仪器和药品能达到实验目的的是
A
B
C
D
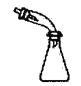

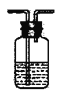
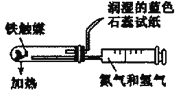
蒸馏时的接收装置
将硫酸铜溶液蒸发浓缩、冷却结晶,得到胆矾晶体
用CCl4除去HBr气体中的少量溴蒸气
模拟工业制氨气并检验产物
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
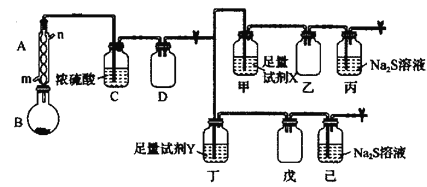
某小组为验证SO2的性质设计如图所示的实验装置,下列说法错误的是( )
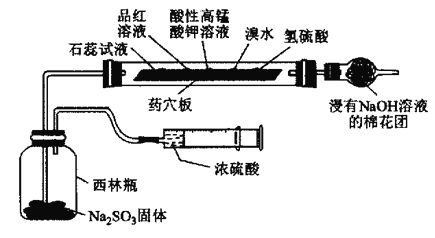
A.一段时间后石蕊溶液和品红溶液均褪色,说明SO2有漂白性
B.一段时间后酸性高锰酸钾溶液、溴水褪色,说明SO2有还原性
C.一段时间后氢硫酸溶液中有淡黄色沉淀生成,说明SO2有氧化性
D.该装置能体现实验的微型化和绿色化
难度: 简单查看答案及解析
-
溴化钙可用作阻燃剂、制冷剂,具有易溶于水、易吸潮等性质。实验室用工业大理石(含少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下(已知步骤Ⅲ的滤液中不含
)。
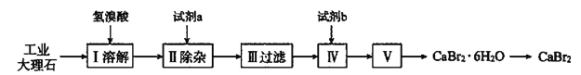
下列说法错误的是( )
A.试剂a可以是生石灰,试剂b是氢溴酸
B.步骤V所含的操作依次是蒸发浓缩、冷却结晶、过滤、洗涤、干燥
C.为将杂质离子除尽,步骤Ⅱ需加过量试剂a,保证溶液呈强碱性
D.工业上常用氨气与溴、石灰乳反应制取溴化钙,若反应中氧化剂与还原剂的物质的量比为3∶2,则产物中会生成一种无色气体
难度: 困难查看答案及解析
-
t℃时,两种碳酸盐MCO3(M表示X2+或Y2+)的沉淀溶解平衡曲线如图所示。已知:
,
,
。
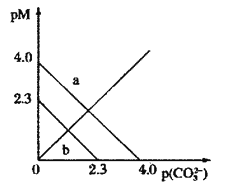
下列说法正确的是( )
A.线a表示YCO3的溶解平衡曲线
B.
C.t℃时,向XCO3悬浊液中加入饱和
溶液,可能有YCO3生成
D.t℃时,向饱和YCO3溶液中加入Na2CO3溶液,一定能产生YCO3沉淀
难度: 中等查看答案及解析
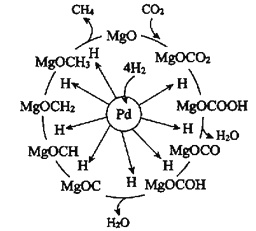
 CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
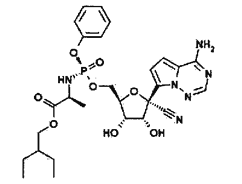
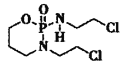 (异环磷酰胺)常用作抗癌药,1mol该物质含
(异环磷酰胺)常用作抗癌药,1mol该物质含


 的路线(其他试剂任选)。__________
的路线(其他试剂任选)。__________