-
据国外有关资料报道,在“独居石”(一种共生矿,化学成分为Ce、La、Nd等的磷酸盐)中,查明有尚未命名的116、124、126号元素。试判断116号元素应位于周期表中的( )
A.第六周期ⅣA族 B.第七周期ⅥA族
C.第七周期ⅦA族 D.第八周期ⅥA族
难度: 简单查看答案及解析
-
氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2KJ,形成1 mol 氯化氢中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A. Q1+ Q2<2Q3 B. Q1+ Q2>Q3 C. Q1+ Q2<Q3 D. Q1+ Q2>2Q3
难度: 中等查看答案及解析
-
相同温度下,有关反应速率的下列说法中正确的是( )
A. 0.1 mol·L-1盐酸和0.1 mol·L-1硫酸与2 mol·L-1 NaOH溶液反应的速率相同
B. 大理石块和大理石粉与0.1 mol·L-1盐酸反应的速率相同
C. 等量的镁粉.铝粉和0.1 mol·L-1盐酸反应的速率相同
D. 0.1 mol·L-1盐酸和0.1 mol·L-1硝酸与相同形状和大小的大理石反应的速率相同
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层有6个电子,Y是至今发现非金属性最强的元素,Z的周期序数等于族序数,W与Z相邻。下列说法不正确的是( )
A.X2与X3互为同位素 B.Y的氢化物可刻蚀玻璃
C.Z的氧化物可用作耐火材料 D.W的氧化物可用作光导纤维
难度: 简单查看答案及解析
-
金属钛对人体体液无毒且有惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称,下列有关
和
的说法正确的是( )
A.
和
原子中均含有22个质子 B.
和
的中子数相同
C.Ti元素的相对原子质量为49 D.
和
为同一核素
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A.在多电子原子里能量高的电子通常在离核近的区域内运动
B.核外电子总是先排在能量低在电子层上
C.两种微粒,若核外电子排布相同,则其化学性质一定相同
D.微粒的最外层只能是8个电子才稳定
难度: 简单查看答案及解析
-
已知R2+核外有a个电子,b个中子,表示R原子的符号正确的是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列有关性质的比较,不能用元素周期律解释的是( )
A.Al(OH)3与NaOH溶液反应,Mg(OH)2不与NaOH溶液反应
B.F2在暗处遇H2爆炸,I2在暗处遇H2几乎不反应
C.酸性:HNO3>H3PO4
D.热稳定性:Na2CO3>NaHCO3
难度: 简单查看答案及解析
-
下列各组元素中按微粒半径递增顺序排列的是 ( )
A. K Na Li B. N O F C. Ca2+ K+ Cl- D. Ba2+ Ca2+ Mg2+
难度: 简单查看答案及解析
-
根据元素周期律,由下列事实进行归纳推测,推测不合理的是( )
选项
事实
推测
A
铬(Cr)的金属性位于锌和铁之间
铬能与稀盐酸发生反应
B
Si是半导体材料,同族的Ge也是半导体材料
第ⅣA族的元素的单质都可作半导体材料
C
HCl在1500 ℃时分解,HI在230 ℃时分解
HBr的分解温度介于二者之间
D
Si与H2高温时反应,S与H2加热能反应
P与H2在高温时能反应
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列叙述不正确的是( )
①分子内一定含有共价键
②离子键就是阴、阳离子的静电引力
③沸点:SnH4>GeH4>SiH4>CH4
④非金属原子间不可能形成离子化合物
⑤H和O可形成既含极性共价键又含非极性共价键的化合物
⑥水分子很稳定,是因为水分子之间存在氢键作用
⑦金属性:Be<Mg<Ca<K
A.①②④⑥ B.②③④⑦ C.①④⑤⑥ D.全部都不正确
难度: 中等查看答案及解析
-
下列物质中,从化学键的角度看,有一种与其他三种明显不同,这种物质是( )
A.Na2O2 B.CH4
C.SO2 D.H2O2
难度: 简单查看答案及解析
-
下列化学用语中,正确的是( )
A.CCl4的电子式为
B.CaCl2的电子式为
C.HClO的结构式为H—Cl—O
D.用电子式表示HCl的形成过程为
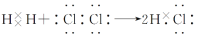
难度: 简单查看答案及解析
-
对于反应Zn+H2SO4=ZnSO4+H2↑,1 mol Zn反应时放出Q kJ热量。下列叙述不正确的是( )

A.反应过程中的能量关系可用如图表示 B.滴入少许CuSO4溶液后反应速率减小
C.若将该反应设计成原电池,则锌为负极 D.理论上当转移4 mol电子时放出2QkJ热量
难度: 中等查看答案及解析
-
如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
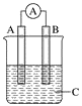
A. A是Zn,B是Cu,C为稀硫酸
B. A是Cu,B是Zn,C为稀硫酸
C. A是Fe,B是Ag,C为稀AgNO3溶液
D. A是Ag,B是Fe,C为稀AgNO3溶液
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.镍镉电池、锂电池和锌锰电池都是二次电池
B.燃料电池是一种高效但是会污染环境的新型电池
C.化学电池的反应原理是氧化还原反应
D.铅蓄电池放电时正极是Pb,负极是PbO2
难度: 简单查看答案及解析
-
微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别为Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-= ZnO+H2O, Ag2O+H2O+2e-=2Ag+2OH-,总反应式为:Ag2O+ Zn = 2Ag+ZnO。根据上述反应式,下列说法正确的是( )
A.在使用过程中,电池负极区溶液的碱性增强
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
难度: 中等查看答案及解析
-
LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )
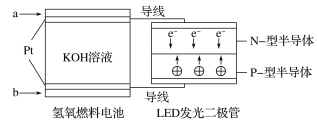
A.a处通入氧气,b处通入氢气
B.通入H2的电极发生反应:H2-2e-=2H+
C.通入O2的电极为电池的正极
D.该装置将化学能最终转化为电能
难度: 中等查看答案及解析
-
下列对化学反应速率和限度的叙述正确的是( )
A.决定化学反应速率的主要因素是光照、超声波、压强和催化剂
B.用Cu和稀硝酸反应制备NO时,改用63%的浓硝酸可以加快产生NO的速率
C.可逆反应进行到一定限度时,正、逆反应速率相等,各物质的浓度也相等
D.工业生产过程中,提高化学反应的限度有利于节约原料和能源
难度: 简单查看答案及解析
-
在2A(g)+B(g)⇌3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.v(A)=0.5 mol·L-1·s-1 B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1 D.v(D)=1 mol·L-1·s-1
难度: 简单查看答案及解析
-
在容积固定容器中,发生反应2HI(g)
H2(g)+I2(g), 下列方法中能证明已达到平衡状态的是( )
①混合气体的颜色不再变化 ②
各组分浓度相等 ③
④一个H-H键断裂的同时有两个H-I 键断裂 ⑤混合气体的平均摩尔质量不再变化
A.①④ B.①②④ C.①③⑤ D.①④⑤
难度: 中等查看答案及解析
-
一定温度下,在一容积不变的密闭容器中发生可逆反应2X(g)
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
A.混合气体的密度不再变化 B.反应容器中Y的质量分数不变
C.X的分解速率与Y的消耗速率相等 D.单位时间内生成1 mol Y的同时生成2 mol X
难度: 中等查看答案及解析