-
下列实验过程中,始终无明显现象的是
A.NO2通入FeSO4溶液中 B.NH3通入AlCl3溶液中
C.CO2通入CaCl2溶液中 D.SO2通入Ba(NO3)2溶液中
难度: 中等查看答案及解析
-
近年来,我国大力弘扬中华优秀传统文化,体现了中华民族的“文化自信”。下列有关说法错误的是( )
A.成语“百炼成钢”“蜡炬成灰”中均包含了化学变化
B.制备“陶冶新平肇汉唐,宋明瓷夺宝珠光”中的瓷,主要原料为黏土
C.谚语“雷雨肥庄稼”,其过程中包含了氧化还原反应
D.诗句“折戟沉沙铁未销”中的金属在常温下能溶于浓硝酸
难度: 简单查看答案及解析
-
能鉴别Na2SO4、NH4NO3、KCl、(NH4)2SO4四种溶液(可以加热)的一种试剂是( )
A.Ba(OH)2溶液 B.Ba(NO3)2溶液 C.BaCl2溶液 D.AgNO3溶液
难度: 简单查看答案及解析
-
下列关于氮及其化合物,说法不正确的是
A.氮气是空气中含量最高的气体,性质比较稳定
B.“光化学烟雾”、“硝酸酸雨”的形成都与氮氧化物有关
C.工业硝酸往往会发黄,因为其中含有Fe3+
D.常温下,浓硝酸可以利用铁罐车进行运输
难度: 简单查看答案及解析
-
下列反应最终没有固体析出的是
A. 向氯化钡溶液中通入少量CO2
B. 向饱和氢氧化钠溶液中加入钠单质
C. 向饱和碳酸钠溶液中通入过量CO2
D. 向NaHCO3溶液中加入过量澄清石灰水
难度: 困难查看答案及解析
-
下列离子方程式书写正确的是( )
A.向水中通入NO2:2NO2+H2O=2H++NO3-+NO
B.向Cu(NO3)2溶液中加入氨水:Cu2++2OH-=Cu(OH)2↓
C.向Fe(NO3)3溶液中加入少量铁粉:2Fe3++Fe=3Fe2+
D.铝与氢氧化钠溶液的反应:Al+2OH-=AlO2-+H2↑
难度: 简单查看答案及解析
-
下列关于氮及其化合物的说法,不正确的是
A.铵盐一般都溶于水,且都可分解放出氨气
B.液氨气化时会吸收大量的热,所以NH3可用作制冷剂
C.汽车尾气中的氮氧化物是造成光化学烟雾的主要原因之一
D.工业浓硝酸通常呈黄色,是因为溶解了NO2气体
难度: 简单查看答案及解析
-
下列各组气体在通常情况下既能用浓硫酸又能用碱石灰干燥的是
A.SO2 B.CO2 C.NH3 D.O2
难度: 简单查看答案及解析
-
将标准状况下的 aLHCl气体溶于1000g水中,得到盐酸密度为bg/cm3,则该盐酸的物质的量浓度是( )
A.
mol/L
B.
mol/L
C.
mol/L
D.
mol/L
难度: 中等查看答案及解析
-
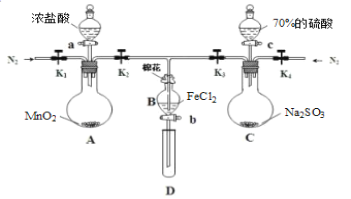
某研究小组利用如图装置探究SO2和Fe(NO3)3溶液的反应原理。下列说法错误的是( )
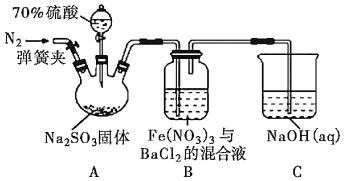
A.装置B中若产生白色沉淀,说明Fe3+能将SO2氧化成SO
B.实验室中配制加70%的硫酸需要的玻璃仪器有量筒、烧杯、玻璃棒
C.三颈烧瓶中通入N2的操作应在滴加浓硫酸之前,目的是排尽装置内的空气
D.装置C可能发生倒吸,同时还不能完全吸收反应产生的尾气
难度: 中等查看答案及解析
-
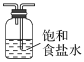
如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
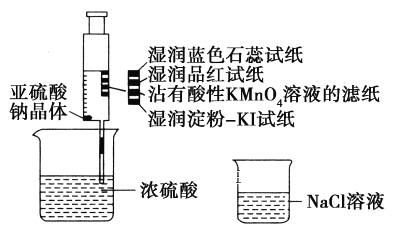
A.蓝色石蕊试纸先变红后褪色
B.品红试纸、沾有酸性KMnO4溶液的滤纸均褪色,证明SO2具有漂白性
C.湿润淀粉-KI试纸未变蓝说明SO2的氧化性弱于I2
D.NaCl溶液可用于除去实验中多余的SO2
难度: 中等查看答案及解析
-
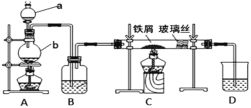
氨能被氧气氧化,经一系列反应得到硝酸。分析如图实验所得结论错误的是( )
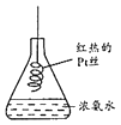
A.浓氨水具有挥发性
B.浓氨水中含有NH3•H2O
C.若Pt丝始终保持红热,则该反应放热
D.锥形瓶口有少量红棕色气体出现,图中反应为:4NH3+7O2
4NO2+6H2O
难度: 中等查看答案及解析
-
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示,下列关于海洋氮循环的说法中,正确的是( )
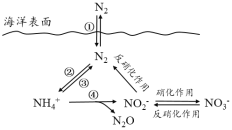
A.海洋中不存在游离态的氮
B.②中的含氮物质转化属于氮的固定
C.④中的含氮物质转化属于氮的还原
D.向海洋中排放含NO3-的废水不会影响NH4+的含量
难度: 中等查看答案及解析
-
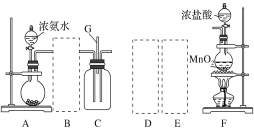
某化学学习小组利用如图装置来制备无水AlCl3(已知:无水AlCl3178℃升华,遇水能迅速发生反应)。下列说法正确的是( )
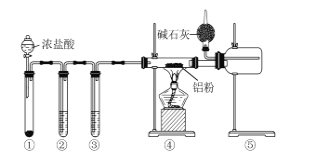
A.装置①中的试剂可能是二氧化锰
B.装置②、③中的试剂分别为浓硫酸、饱和食盐水
C.④和⑤之间使用粗玻璃管是为了防堵塞
D.球形干燥管中碱石灰的作用只有处理尾气
难度: 中等查看答案及解析