-
下列有关说法错误的是( )
A.聚丙烯纤维是生产医用口罩的重要材料
B.在月饼包装盒中放入生石灰,可防止月饼氧化变质
C.84消毒液、医用酒精等都可以用于新冠病毒的消毒
D.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.苯的硝化、油脂的皂化均可看作取代反应
B.蛋白质和淀粉都是高分子化合物,都能水解生成葡萄糖,提供生命活动的能量
C.用酸性KMnO4溶液无法鉴别乙醇与苯
D.分子式为C4H9Cl的同分异构体有5种
难度: 简单查看答案及解析
-
复旦大学研发的一种新型水锂电池,一极采用复合膜包裹的金属锂,另一极采用锰酸锂(LiMn2O4),以0.5mol·L-1Li2SO4水溶液作电解质,安全性能和成本较现有的锂离子电池都具有明显的优势。下列有关该电池的说法不正确的是( )
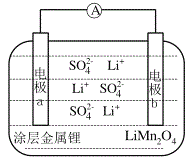
A.电极a是负极,电极b是正极
B.工作时电池的总反应为:LiMn2O4+Li=Li2Mn2O4
C.放电时,溶液中Li+从a向b迁移
D.电池放电时的阳极反应式为:Li2Mn2O4−e-=LiMn2O4+Li+
难度: 中等查看答案及解析
-
有原子序数依次增大的a、b、c、d四种元素,最外层电子数分别为4、1、x、7,已知c原子的电子层数等于x,d-的电子层结构与Ar元素相同。下列说法错误的是( )
A.元素a与氢形成原子比为1:1的化合物有多种
B.元素b的单质能与水、无水乙醇反应
C.c的简单离子与d-的简单离子最外层电子数和电子层数都不相同
D.元素a与元素d可形成既含有极性共价键又含非极性共价键的化合物
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1.0L0.5mol·L-1FeBr2溶液与1molCl2反应时转移的电子数目为2NA
B.25℃,1LpH=9的CH3COONa溶液中,发生电离的水分子数为1×10-9NA
C.3.0g甲醛(HCHO)和冰醋酸的混合物中含有的原子总数为0.4NA
D.标准状况下,2.24L二氯甲烷中含有的原子数目为0.5NA
难度: 中等查看答案及解析
-
下列实验过程可以达到实验目的的是
编号
实验目的
实验过程
A
测定NaHCO3溶液的浓度
用标准HCl溶液滴定NaHCO3溶液来测定其浓度,并选择酚酞为指示剂
B
鉴别KI、AgNO3、Na2CO3、NaAlO2四种溶液
向盛有KI、AgNO3、Na2CO3、NaAlO2四种溶液的试管中分别滴加盐酸,观察实验现象
C
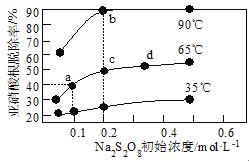
探究浓度对反应速率的影响
向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液,观察实验现象
D
除去乙醇中混有的乙酸
混合液蒸馏,收集78.3℃左右的馏分(乙醇的沸点为78.3℃)
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
常温下,用AgNO3溶液分别滴定浓度均为0.01mol·L-1的KCl、K2C2O4溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O42-的水解)。下列叙述正确的是( )

A.Ksp(Ag2C2O4)=10-7
B.a点表示的是AgCl的不饱和溶液
C.向c(Cl-)=c(C2O42-)=0.1mol·L-1的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀
D.Ag2C2O4(s)+2Cl-(aq)
2AgCl(s)+C2O42-(aq)的平衡常数为109.04
难度: 困难查看答案及解析