-
下列化合物中既含有离子键又含有共价键的是 ( )
A.HNO3 B.CaCl2 C.NH4Cl D.H2SO4
难度: 中等查看答案及解析
-
下列物质互为同分异构体的一组是
A.35Cl和37Cl B.CH3CH2OH和CH3OCH3
C.O2和O3 D.H2O和H2O2
难度: 简单查看答案及解析
-
在科学史上每一次重大的发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于( )
A.提出了元素周期律
B.开发了合成氨的生产工艺
C.揭示了燃烧的本质
D.提取了治疟药物青蒿素
难度: 简单查看答案及解析
-
对于反应中的能量变化,表述正确的是( )
A.放热反应中,反应物的总能量大于生成物的总能量
B.断开化学键的过程会放出能量
C.加热才能发生的反应一定是吸热反应
D.氧化反应均为吸热反应
难度: 简单查看答案及解析
-
有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为:
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>D>C>A
难度: 中等查看答案及解析
-
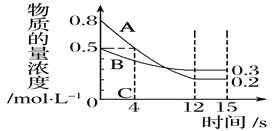
已知一定温度时:2SO2(g)+O2(g) ⇌2SO3(g),当生成2mol SO3时,放出热量197kJ,在相同温度和压强下,向密闭容器中通入2mol SO2和1molO2,达到平衡时放出热量Q,则下列关系式中正确的是
A.Q=197 kJ B.Q<197×2 kJ C.Q<197 kJ D.Q>197 kJ
难度: 简单查看答案及解析
-
I可用于治疗甲状腺疾病。该原子的质子数是
A. 53 B. 78 C. 131 D. 184
难度: 简单查看答案及解析
-
下列化学用语表示正确的是
A. 乙酸的结构简式:C2H4O2 B. N2的电子式:N ::: N
C. S2-的结构示意图:
D. KCl的电离方程式:KCl = K++ Cl-
难度: 简单查看答案及解析
-
下列选项描述的过程能实现化学能转化为热能的是
A.
 光合作用 B.
光合作用 B. 烧炭取暖
烧炭取暖C.
 风力发电 D.
风力发电 D. 电解冶炼
电解冶炼难度: 简单查看答案及解析
-
下列物质属于共价化合物的是
A. H2O B. MgO C. CaCl2 D. KBr
难度: 简单查看答案及解析
-
下列物质不属于高分子化合物的是
A. 蛋白质 B. 聚乙烯 C. 油脂 D. 淀粉
难度: 简单查看答案及解析
-
将等质量的下列各烃,完全燃烧生成CO2和H2O,耗氧量最大的是( )
A. CH4 B. C2H4 C. C6H6 D. C3H6
难度: 中等查看答案及解析
-
近日,我国渤海探明超千亿立方的天然气田。天然气的主要成分为
A. H2 B. CH4 C. CO2 D. NH3
难度: 简单查看答案及解析
-
CO2 + 4H2
CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是
A. 适当升温能加快反应速率 B. 催化剂对反应速率无影响
C. 达到平衡时,正反应速率为0 D. 达到平衡时,CO2能100%转化为CH4
难度: 简单查看答案及解析
-
今有下列各组反应,放出H2的平均速率最快的是(不考虑酸根对速率的影响)( )。
编号
金属
酸的浓度及体积
反应温度/℃
A
2.4 g镁条
3 mol·L-1硫酸100 mL
30
B
2.4 g镁粉
3 mol·L-1盐酸200 mL
40
C
2.4 g镁粉
3 mol·L-1硫酸100 mL
40
D
5.6 g铁粉
3 mol·L-1硫酸100 mL
40
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列各个装置中能组成原电池的是
A.
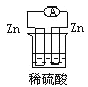 B.
B.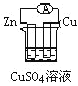
C.
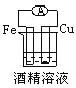 D.
D.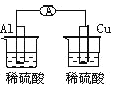
难度: 中等查看答案及解析
-
某元素的原子结构示意图为:
,则该元素在元素周期表中的位置是
A.第二周期,第ⅠA族 B.第二周期,第ⅤA族
C.第三周期,第ⅣA族 D.第三周期,第ⅤA族
难度: 中等查看答案及解析
-
下列事实不能说明氯元素的非金属性比硫元素强的是( )
A.氯气与氢硫酸能发生置换反应 B.HClO4酸性比H2SO4强
C.盐酸是强酸,氢硫酸是弱酸 D.受热时,氯化氢比硫化氢稳定
难度: 中等查看答案及解析
-
下列能用分液漏斗分离的是
A. 植物油和乙醇 B. 乙酸乙酯和水
C. 乙酸和乙醇 D. 汽油和煤油
难度: 简单查看答案及解析
-
下列关于淀粉的说法正确的是( )
A.化学式为C6H12O6 B.不属于糖类
C.不能发生水解反应 D.常温下其水溶液遇碘变蓝
难度: 简单查看答案及解析
-
一定温度下,反应N2(g)+3H2(g)
2NH3(g)达到化学平衡状态的标志是
A. N2、H2和NH3的质量分数不再改变
B. c(N2)∶c(H2)∶c(NH3)=1∶3∶2
C. 断裂1 mol N≡N键的同时,形成6 mol N—H键
D. N2与H2的物质的量之和是NH3的物质的量的2倍
难度: 中等查看答案及解析
-
下列有机反应属于加成反应的是
A. C3H8 + 5O2
3CO2 + 4H2O
B. CH2 = CH2 + Br2 →
C. 2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
D.
+ HNO3
+ H2O
难度: 简单查看答案及解析