-
乙烯是一种重要的化工原料。下列物质中,不能通过乙烯的加成反应一步制得的是
A. CH3CH2Cl B. CH3CH2OH C. CH3COOH D. CH2BrCH2Br
难度: 简单查看答案及解析
-
下列物质在一定条件下能与甲烷发生取代反应的是
A. 氯气 B. 酸性高锰酸钾溶液
C. 氢氧化钠溶液 D. 溴的四氯化碳溶液
难度: 简单查看答案及解析
-
已知下列实验事实:
①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;
②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液;
③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
A.化合物KCrO2中Cr元素为+3价
B.实验①证明Cr2O3是两性氧化物
C.实验②证明H2O2既有氧化性又有还原性
D.实验③证明氧化性:Cr2O72- > I2
难度: 中等查看答案及解析
-
运输汽油的车上,贴有的危险化学品标志是( )
A.

B.

C.

D.

难度: 中等查看答案及解析
-
我国科学家屠呦呦发现抗虐新药青蒿素(C15H22O5),该成果获得2015年诺贝尔奖。青蒿素属于( )
A.无机物 B.有机化合物 C.氧化物 D.单质
难度: 简单查看答案及解析
-
下列物质中属于碱性氧化物的是( )
A.CO2 B.Na2O2 C.Na2O D.Al2O3
难度: 简单查看答案及解析
-
下列物质中,只含有非极性共价键的是( )
A.KOH B.H2S C.Cl2 D.MgO
难度: 简单查看答案及解析
-
下列物质性质与用途的对应关系不正确的是( )
选项
性质
用途
A.
氧化铁呈红棕色
红色涂料
B.
次氯酸钠具有漂白性
漂白剂
C.
浓硫酸具有脱水性
干燥剂
D.
液氨汽化时要吸收大量的热
制冷剂
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
用化学用语表示 NH3+ HCl
NH4Cl中的相关微粒,其中正确的是( )
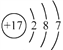
A. 中子数为8的氮原子:
B. HCl 的电子式:
C. NH3的结构式:
D. Cl−的结构示意图:
难度: 简单查看答案及解析
-
NA是阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,3.2gO2中氧分子数为0.1NA
B.标准状况下,22.4L正己烷中碳原子数为6NA
C.78gNa2O2在足量CO2中充分反应转移的电子数约为2NA
D.密闭容器中,3molH2和1molN2充分反应后氨分子数为2NA
难度: 中等查看答案及解析
-
2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(37Rb)同周期。下列说法不正确的是
A.In是第五周期第ⅢA族元素
B.11549In的中子数与电子数的差值为17
C.原子半径:In>Al
D.碱性:In(OH)3>RbOH
难度: 中等查看答案及解析
-
下列各组性质比较中,正确的是( )
①最高化合价:F>O>N
②离子还原性:S2->Cl->Br->I-
③酸性:HClO4>HBrO4>HIO4
④金属性:K>Na>Mg>Al
⑤气态氢化物稳定性:HF>HCl>H2S
⑥半径:O2->F->Na+>Mg2+
A.①②③ B.③④⑤⑥ C.②③④ D.①③④⑤⑥
难度: 中等查看答案及解析
-
2019年为“国际化学元素周期表年”。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法不正确的是( )
A.原子半径:W<X
B.X的最高价氧化物的水化物是强碱
C.Y单质可用做半导体材料
D.气态氢化物热稳定性:Z<W
难度: 中等查看答案及解析
-
下列烷烃中,与
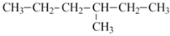 互为同分异构体的是
互为同分异构体的是A.2,3-二甲基丁烷 B.2,2,3-三甲基丁烷
C.2-甲基丁烷 D.2,2,3,3-四甲基丁烷
难度: 简单查看答案及解析
-
对于反应4NH3+5O2=4NO+6H2O,下列为4种不同情况下测得的反应速率,其中能表明该反应进行最快的是()
A.v(NH3)=0.2mol·L-1·s-1 B.v(O2)=14mol·L-1·s-1
C.v(H2O)=0.25mol·L-1·s-1 D.v(NO)=9mol·L-1·s-1
难度: 简单查看答案及解析
-
把镁条(去除氧化膜)投入到盛有盐酸的敞口容器中,产生H2的速率v与时间t的关系如下图所示,其中影响AB段速率的主要因素是
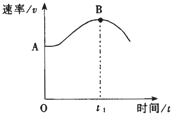
A. H+的浓度 B. 体系的压强 C. 溶液的温度 D. Cl-的浓度
难度: 中等查看答案及解析
-
在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应A(s)+3B(g)
2C(g)+D(g)已达平衡状态的是
A.B的物质的量浓度 B.混合气体的密度
C.混合气体的压强 D.v(B消耗)=3v(D消耗)
难度: 中等查看答案及解析
-
已知反应A+B=C+D的能量变化如图所示,下列关于此反应的说法不正确的是( )
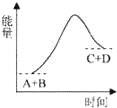
A. 是吸热反应
B. 只有在加热条件下才能进行
C. 生成物的总能量高于反应物的总能量
D. 反应中断开化学键吸收的总能量高于形成化学键放出的总能量
难度: 简单查看答案及解析
-
如图所示的装置中,M为铁棒,N为石墨棒。关于此装置的下列叙述中,不正确的是( )
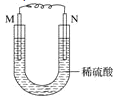
A.M为负极,N为正极
B.N上发生的反应为2H++2e=H2↑
C.M上发生的反应为Fe-3e-=Fe3+
D.溶液中的硫酸根离子向M移动
难度: 简单查看答案及解析
-
利用下列装置或操作进行实验,不能达到目的的是( )
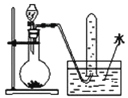
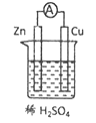
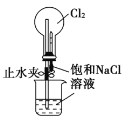

置于光亮处
A.用稀硝酸与Cu反应制取NO
B.验证氧化还原反应中有电子转移
C.进行喷泉实验
D.验证甲烷和氯气能发生反应
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
利用如图装置可以进行实验并能达到实验目的的是( )
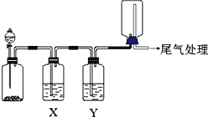
选项
实验目的
X中试剂
Y中试剂
A
用KMnO4和浓盐酸制取并收集纯净干燥的Cl2
饱和食盐水
浓硫酸
B
用Cu与浓硝酸制取并收集纯净干燥的NO2
水
浓硫酸
C
用生石灰与浓氨水制取并收集纯净干燥的NH3
水
浓硫酸
D
用铜片和浓硫酸制取并收集纯净干燥的SO2
饱和NaHSO3溶液
浓硫酸
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列变化中,气体反应物既被氧化又被还原的是( )
A.金属钠露置在空气中迅速变暗
B.充满二氧化氮的试管倒扣在水槽中,试管内液面上升
C.露置在空气中的过氧化钠固体变白
D.将氨气与氯化氢混合,产生大量白烟
难度: 简单查看答案及解析
-
下列实验中的颜色变化,与氧化还原反应无关的是( )
A
B
C
D
实验
NaOH溶液滴入FeSO4溶液中
石蕊溶液滴入氯水中
氧化铜加入稀硝酸中
热铜丝插入稀硝酸中
现象
产生白色沉淀,随后变为红褐色
溶液变红,随后迅速褪色
溶液变蓝
产生无色气体,随后变为红棕色
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
数字化实验是利用传感器和信息处理终端进行数据采集与分析的实验手段。下图是利用数字化实验测定光照氯水过程中得到的图像,该图像表示的意义是
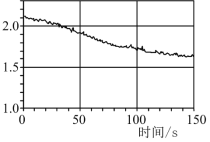
A.氯离子浓度随时间的变化
B.氧气体积分数随时间的变化
C.氯水的pH随时间的变化
D.氯水导电能力随时间的变化
难度: 简单查看答案及解析
-
室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1mol·L-1Fe2(SO4)3溶液:H+、NH
、NO
、Cl-
B.0.1mol·L-1Na2SO3溶液:K+、NH
、SO
、ClO-
C.0.1mol·L-1KHCO3溶液:Na+、Ba2+、Cl-、OH-
D.0.1mol·L-1H2SO4溶液:K+、NH
、NO
、HSO
难度: 简单查看答案及解析
-
某混合溶液中所含离子的浓度如下表,则X离子可能为( )
所含离子
NO
SO
H+
X
浓度mol/L
2
1
2
1
A.Cl- B.Ba2+ C.Fe2+ D.Mg2+
难度: 简单查看答案及解析
-
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.Fe3O4(s)
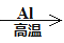 Fe(s)
Fe(s)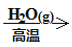 Fe2O3
Fe2O3B.NH4HCO3(s)
NH3(g)
NO2(g)
C.S(s)
SO3(g)
H2SO4(aq)
D.NaHCO3(s)
Na2CO3(s)
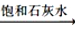 NaOH(aq)
NaOH(aq)难度: 中等查看答案及解析
-
下列解释事实的离子方程式正确的是( )
A.用过量氨水除去烟气中的二氧化硫:SO2+NH3·H2O=
+
B.过量的Fe和稀硝酸反应:Fe+4H++
=Fe3++NO↑+2H2O
C.稀硫酸与氢氧化钡溶液混合产生沉淀:Ba2++
=BaSO4↓
D.实验室用MnO2和浓盐酸制Cl2:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
难度: 简单查看答案及解析
-
下列叙述Ⅰ和Ⅱ均正确,并有因果关系的是( )
选项
叙述Ⅰ
叙述Ⅱ
A
Al有一定的非金属性
向氢氧化铝沉淀中滴加盐酸,沉淀溶解
B
相同条件下NaHCO3的溶解度比Na2CO3的小
向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊
C
钠比铜的金属性强
金属钠可从硫酸铜溶液中置换出铜单质
D
I-还原性弱于Cl-
向NaI溶液中滴入少量氯水和CCl4,振荡、静置,溶液下层呈紫红色
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
根据实验操作及现象所得出的解释或结论不正确的是( )
选项
实验操作及现象
解释或结论
A.
向某溶液中加入足量稀盐酸,无明显现象,再加入BaCl2溶液,有白色沉淀产生
该溶液中一定含有SO
B.
向某溶液中加入浓NaOH溶液,加热,产生
能使湿润的红色石蕊试纸变蓝的气体
该溶液中一定含有NH
C.
向某钾盐中滴加盐酸,产生使澄清石灰水变浑浊的无色无味气体
该钾盐是K2CO3或KHCO3
D.
酸性硝酸铁溶液中加入几滴碘化钾淀粉溶液,出现蓝色
铁离子具有较强氧化性,将I-氧化生成I2
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列实验方法能达到实验目的的是( )
A.将气体通入HNO3酸化的AgNO3溶液,检验SO2中是否含有HCl
B.用溴的四氯化碳溶液鉴别CH4和C2H4
C.加热去除NaHCO3固体中少量的Na2CO3
D.向溶液中滴加少量氯水,再滴加KSCN溶液,检验原溶液中是否含有Fe2+
难度: 中等查看答案及解析
-
某工业废水中存在大量的Na+、Cl-、Cu2+、SO42-,欲除去其中的Cu2+、SO42-,设计工艺流程如图所示:

下列说法不正确的是
A.NaOH的作用是除去Cu2+ B.试剂a 为Na2CO3,试剂b为BaCl2
C.流程图中,操作x为过滤 D.试剂c为盐酸
难度: 中等查看答案及解析
-
某同学设计了蔗糖与浓硫酸反应的改进装置,并对气体产物进行检验,实验装置如图所示。下列结论中正确的是( )
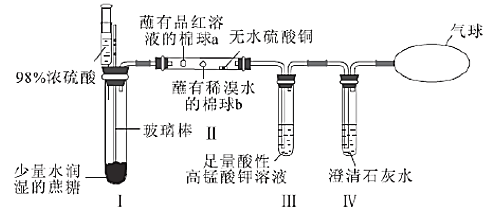
选项
现象
结论
A.
Ⅰ中注入浓硫酸后,可观察到试管中白色固体变为黑色
体现了浓硫酸的吸水性
B.
Ⅱ中观察到棉球a、b都褪色
均体现了SO2的漂白性
C.
Ⅱ中无水硫酸铜变蓝
说明反应产物中有H2O
D.
Ⅲ中溶液颜色变浅,Ⅳ中澄清石灰水变浑浊
说明有CO2产生
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,不正确的是( )
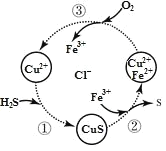
A.过程①中,生成CuS的反应为H2S+Cu2+=CuS↓+2H+
B.过程②中,Fe3+作氧化剂
C.转化图中化合价不变的元素只有铜和氯
D.回收S的总反应为2H2S+O2=2H2O+2S↓
难度: 中等查看答案及解析
-
2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如图。

下列说法正确的是( )
A.过氧化氢的电子式为:
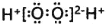
B.反应Ⅰ的离子方程式为:2Fe2++H2O2=2Fe3++2OH-
C.反应Ⅱ的离子方程式为:Fe3++PO
=FePO4↓
D.反应Ⅲ的化学方程可能为:2FePO4+2LiI=2LiFePO4+I2
难度: 中等查看答案及解析
-
以下工业流程制备无机功能材料MnO2,粗MnO2的提纯是工业生产的重要环节,某研究性学习小组设计了将粗MnO2(含有较多MnO和MnCO3)样品转化为纯MnO2实验。

针对上述工业流程,下列选项错误的是( )
A.第①步加稀
时,粗MnO2样品中的MnO、MnCO3转化为可溶性物质
B.不考虑操作过程中的损失,本流程中的
固体能全部循环,不需额外补充
C.第②步反应的离子方程式
D.实验室模拟上述工业流程中得到MnO2固体的操作必须用到的玻璃仪器有玻璃棒、烧杯、漏斗
难度: 困难查看答案及解析
-
某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号
I
II
III
实验步骤
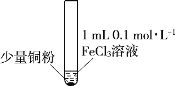
充分振荡,加2mL蒸馏水

充分振荡,加入2mL蒸馏水

充分振荡,加入2mL蒸馏水
实验现象
铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象
铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀
铜粉有剩余,溶液黄色褪去,
变成蓝色,加入蒸馏水后无白色沉淀
下列说法不正确的是( )
A.实验I、II、III中均发生了反应2Fe3++Cu=2Fe2++Cu2+
B.对比实验I、II、III说明白色沉淀的产生可能与铜粉的量及溶液的阴离子种类有关
C.实验I、III中加入蒸馏水后c(Cu2+)相同
D.向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
难度: 中等查看答案及解析