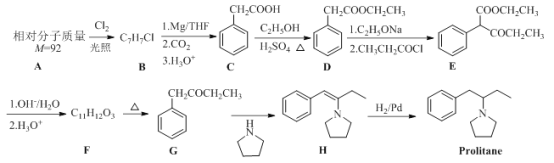
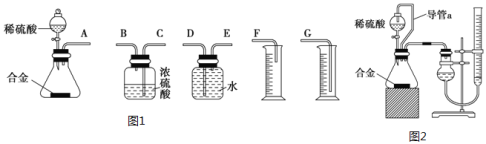
-
化学与生活密切相关,下列叙述中不正确的是( )
A. 用氟利昂做制冷剂会加剧雾霾天气的形成
B. 严格地讲实验室中的“通风厨”是一种不负责任的防污染手段,因为实验产生的有害气体一般没有得到转化或吸收
C. “长征九号”运载火箭的壳体通常采用纤维作增强体,金属作基体的复合材料
D. 漂洗衣服时,可以采用萃取原理中的“少量多次”来节约用水
难度: 中等查看答案及解析
-
锌–空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O===2Zn(OH)42-。下列说法正确的是( )
A.充电时,电解质溶液中K+向阳极移动
B.充电时,电解质溶液中c(OH-) 逐渐减小
C.放电时,负极反应为:Zn+4OH–-2e–= Zn(OH)42-
D.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
难度: 中等查看答案及解析
-
下列有关实验操作与结论都正确的是( )
选项
实验操作及现象
实验结论
A
用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色
说明该食盐不含KIO3
B
向某无色溶液中滴加NaOH溶液,先产生白色沉淀,后沉淀又会全部消失
该无色溶液中一定有Al3+,无Mg2+
C
向尿液中加入新制Cu(OH)2悬浊液,没有砖红色沉淀生成
说明尿液中不含有葡萄糖
D
某待测液中先滴入氯水无明显现象,后滴入硫氰化钾溶液出现血红色
该待测液中一定含有Fe2+
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
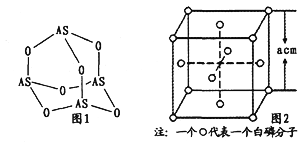
W、X、Y、Z四种短周期元素,在元素周期表中的位置如图所示,其中W元素的原子序数为Z元素原子序数的两倍,则下列说法正确的是
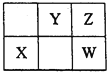
A. X位于元素周期表中的第3周期第ⅥA族
B. X、Y、Z三种元素对应原子的半径依次减小
C. XZ2和YZ2的结构和化学性质相似
D. 利用Y的含氧酸酸性强于W的含氧酸酸性,可证明非金属性W强于Y
难度: 中等查看答案及解析
-
微信热传的“苯宝宝表情包”可看作是由苯衍生的物质配以相应文字形成的(如图)。下列说法正确的是
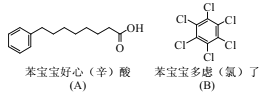
A.化合物(A)不能与乙醇发生反应
B.化合物(B)分子式为C6H6Cl6
C.化合物(B)可通过苯与Cl2发生加成反应制得
D.1mol化合物(A)可与3molH2发生加成反应
难度: 中等查看答案及解析
-
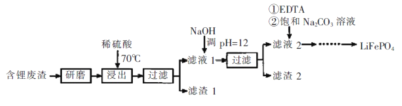
氢氧化铈[Ce(OH)4]是一种重要的稀土氢氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2),某课题组以此粉末为原料回收铈,设计实验流程如下:
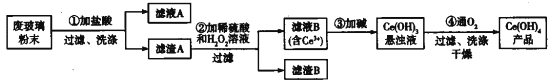
下列说法错误的是
A. 滤渣A中主要含有SiO2、CeO2
B. 过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒
C. 过程②中发生反应的离子方程式为CeO2+H2O2+3H+=Ce3++2H2O+O2↑
D. 过程④中消耗 11.2L O2(已折合成标准状况),转移电子数为2×6.02×1023
难度: 困难查看答案及解析
-
常温下,向100mL0.01mol⋅L-1HA溶液中逐滴加入0.02mol⋅L -1MOH溶液,图中所示曲线表示混合溶液的pH变化情况体积变化忽略不计)。下列说法中不正确的是( )
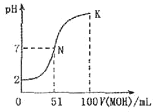
A.MOH为一元弱碱
B.MA稀溶液pH<7
C.N点水的电离程度大于K点水的电离程度
D.K点对应的溶液的pH=10,则c(MOH)+c(OH)-c(H+)=0.01mol⋅L-1
难度: 困难查看答案及解析