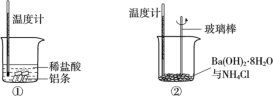-
下列物质不属于天然高分子化合物的是
A.淀粉 B.蚕丝 C.葡萄糖 D.纤维素
难度: 简单查看答案及解析
-
主族元素在周期表中的位置取决于该元素原子的( )
A.相对原子质量和核外电子数 B.电子层数和最外层电子数
C.相对原子质量和最外层电子数 D.电子层数和次外层电子数
难度: 简单查看答案及解析
-
元素性质呈周期性变化根本原因是( )
A.元素的相对原子质量逐渐增大
B.核外电子排布呈周期性变化
C.核电荷数逐渐增大
D.元素化合价呈周期性变化
难度: 简单查看答案及解析
-
安徽宣城所产的宣纸、宣笔、徽墨、宣砚举世闻名。做宣笔常用羊、兔等动物的毛,其主要成分是
A. 蛋白质 B. 纤维素 C. 糖类 D. 油脂
难度: 简单查看答案及解析
-
下列物质能使酸性高锰酸钾溶液褪色的是
A. 聚乙烯 B. 甲烷 C. 苯 D. 乙烯
难度: 中等查看答案及解析
-
下列物质中既有离子键,又有共价键的是( )
A.H2O B.CaCl2 C.KOH D.Cl2
难度: 简单查看答案及解析
-
下列各组性质的比较中,不正确的是
A.碱性:NaOH>Mg(OH)2 B.热稳定性:NH3>PH3
C.金属性:K>Na D.原子半径:Cl>S
难度: 简单查看答案及解析
-
下列几种酸中,酸性最弱的是
A.HClO4 B.H2SO4 C.H3PO4 D.H2CO3
难度: 简单查看答案及解析
-
放射性同位素钬
可用于治疗肝癌。该原子的中子数是
A.67 B.99 C.166 D.233
难度: 简单查看答案及解析
-
某元素X,它的原子最外层电子数是次外层电子数的2倍,则X在周期表中位于
①第二周期②第三周期③ⅣA族④ⅤA族
A.①③ B.②③ C.②④ D.①④
难度: 简单查看答案及解析
-
下列物质互为同分异构体的一组是
A.乙醇和乙酸 B.丁烷和异丁烷 C.12C与14C D.金刚石和石墨
难度: 简单查看答案及解析
-
下列有机物中,不属于烃的是
A. CH2 = CH2 B.
C. CH3CH2CH3 D. CH3COOH
难度: 简单查看答案及解析
-
下列各组物质的相互关系描述正确的是
A.H2、D2和T2互为同位素 B.
和
互为同分异构体
C.金刚石、C60、石墨互为同系物 D.(CH3)2CHC2H5和CH3CH2CH(CH3)2属于同种物质
难度: 中等查看答案及解析
-
实验室用乙酸和乙醇在浓硫酸作用下制取乙酸乙酯的装置如图。下列说法正确的是
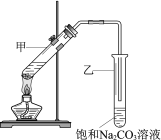
A. 向甲试管中先加浓硫酸,再加乙醇和乙酸
B. 乙试管中导管不伸入液面下,是为了防止倒吸
C. 加入过量乙酸,可使乙醇完全转化为乙酸乙酯
D. 实验完毕,可将乙酸乙酯从混合物中过滤出来
难度: 中等查看答案及解析
-
下列关于有机物的说法正确的是
A.甲烷与氯气发生取代反应,只能生成一氯甲烷
B.乙醇和乙酸都可以与钠反应生成氢气
C.苯和乙烯均能与溴水发生加成反应使溴水褪色
D.甲醛易溶于水,其水溶液具有杀菌消毒作用,可用于浸泡海鲜食品
难度: 中等查看答案及解析
-
下列各图中,表示正反应是吸热反应的图是( )
A.
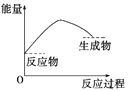 B.
B.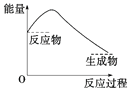
C.
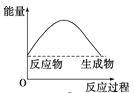 D.
D.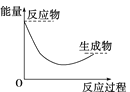
难度: 简单查看答案及解析
-
下列变化属于放热反应的是
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰
A.①④ B.⑤ C.①④⑤ D.②④
难度: 简单查看答案及解析
-
不属于自发进行的变化是
A.红墨水加到清水中使整杯水变红 B.冰在室温下融化成水
C.NaHCO3转化为Na2CO3 D.天然气的燃烧
难度: 简单查看答案及解析
-
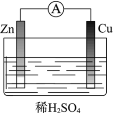
下列装置可以构成原电池的是
A.
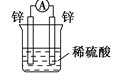 B.
B.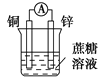
C.
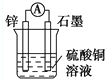 D.
D.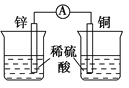
难度: 简单查看答案及解析
-
下列措施,一定不能加快化学反应速率的是
A.增大压强 B.升高温度 C.加催化剂 D.增大固体质量
难度: 简单查看答案及解析
-
下列对化学反应平衡常数(K)的叙述正确的是
A.仅升髙温度,K可能增大,也可能减小 B.仅加入催化剂,K可能增大
C.仅增大压强,K可能减小 D.仅减小浓度,K值可能减小
难度: 中等查看答案及解析
-
A、B、C都是金属,把A浸入C的硫酸盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C三种金属的活动性顺序为
A.A>B>C B.A>C>B C.B>A>C D.B>C>A
难度: 简单查看答案及解析
-
对于可逆反应C(s)+H2O(g)
CO(g)+H2(g),在一定温度下达到平衡时,其平衡常数表达式正确的是 ( )
A.K=
B.K=
C.K=
D.K=
难度: 简单查看答案及解析
-
在一密闭容器中充入一定量的H2和N2,经测定反应开始后3s内平均速率的v(H2)=0.3mol/(L•s),则3s末NH3的浓度为:
A.0.4mol/L B.0.6mol/L C.0.9mol/L D.1.2mol/L
难度: 简单查看答案及解析
-
下列热化学方程式中.△H能正确表示物质的燃烧热的是( )
A.CO(g) +
O2(g) ==CO2(g); △H=-283.0 kJ/mol
B.C(s) +
O2 ==CO(g); △H=-110.5 kJ/mol
C.H2(g) +
O2(g)==H2O(g); △H=-241.8 kJ/mol
D.2C8H18(l) +25O2(g)==16 CO2(g)+18 H2O(l); △H=-1136 kJ/mol
难度: 简单查看答案及解析
-
已知常温时红磷比白磷稳定,在下列反应中:
4P(白磷,s)+5O2(g)====2P2O5(s);△H=== -a kJ/mol
4P(红磷,s)+5O2(g)====2P2O5(s);△H=== -b kJ/mol
若a、b均大于零,则a和b的关系为
A.a<b B.a=b C.a>b D.无法确定
难度: 中等查看答案及解析
-
某温度下,反应2A(g)+B(g)⇌2C(g)的平衡常数K1=50,在同一温度下,反应2C(g)⇌2A(g)+B(g)的平衡常数K2为( )
A.2500 B.50 C.0.02 D.0.002
难度: 简单查看答案及解析
-
在容器中充入SO2和只由18O原子组成的氧气(18O2)。在一定条件下达到平衡时,18O存在于
A.只存在于O2中
B.只存在于O2和SO3中
C.只存在于SO2和SO3中
D.SO3、SO2和O2中都有可能存在
难度: 简单查看答案及解析
-
对平衡CO2(g)
CO2(aq) △H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )
A. 升温增压 B. 降温减压
C. 升温减压 D. 降温增压
难度: 简单查看答案及解析
-
对于达到平衡状态的可逆反应:N2 +NH3
2NH3 ,下列有关叙述正确的是
A.反应物和生成物浓度不再发生变化 B.反应物和生成物的浓度相等
C.N2和NH3的质量分数相等 D.正反应和逆反应不再进行
难度: 简单查看答案及解析