-
下列有关甲烷的取代反应的叙述正确的是
A. 甲烷与氯气的物质的量之比为1∶1,混合发生取代反应只生成CH3Cl
B. 甲烷与氯气的取代反应,生成的产物中CH3Cl最多
C. 甲烷与氯气的取代反应生成的产物为混合物
D. 1 mol甲烷生成CCl4最多消耗2 mol氯气
难度: 简单查看答案及解析
-
W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X可生成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z原子最外层的电子数与W的电子总数相同。下列叙述正确的是
A. X与其他三种元素均可形成两种或两种以上的二元化合物
B. Y与其他三种元素分别形成的化合物中只含有离子键
C. 四种元素的简单离子具有相同的电子层结构
D. W的氧化物对应的水化物均为强酸
难度: 中等查看答案及解析
-
下列说法正确的是
A.形成离子键的阴阳离子间只存在静电吸引力
B.HF、HCl、HBr、HI的热稳定性和还原性均依次减弱
C.第三周期非金属元素含氧酸的酸性从左到右依次增强
D.元素周期律是元素原子核外电子排布周期性变化的结果
难度: 简单查看答案及解析
-
下列有关化学用语表示正确的是( )
A.CS2的电子式为
B.次氯酸的结构式:H—Cl—O
C.中子数为16的磷原子:
D.甲烷的球棍模型:
难度: 中等查看答案及解析
-
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
A.v(W)=3v(Z) B.2v(X)=v(Y) C.2v(X)=3v(Z) D.3v(W)=2v(X)
难度: 简单查看答案及解析
-
下列有关原电池的说法中正确的是( )
A. 原电池工作时,可能会伴随着热能变化
B. 手机、电脑中使用的锂离子电池属于一次电池
C. 在内电路中,电子由正极流向负极
D. 燃料电池工作时燃料在电池中燃烧,然后热能转化为电能
难度: 中等查看答案及解析
-
以下说法错误的是( )。
A.甲烷分子是由极性键构成的分子
B.甲烷分子具有正四面体结构
C.甲烷分子中4个C—H键完全相同
D.甲烷分子中具有非极性键
难度: 中等查看答案及解析
-
下列条件一定能使反应速率加快的是
①增加反应物的物质的量②升高温度③缩小反应容器的体积④加入生成物⑤加入MnO2
A. 全部 B. ①②⑤ C. ② D. ②③
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.密闭容器中充入1mol N2和3mol H2可生成2mol NH3
B.一定条件下,可逆反应达到平衡状态,该反应就达到了这一条件下的最大限度
C.对于任何反应增大压强,化学反应速率均增大
D.化学平衡是一种动态平衡,条件改变,原平衡状态不会被破坏
难度: 中等查看答案及解析
-
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )
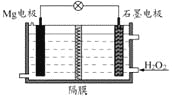
A.Mg 电极是该电池的正极
B.H2O2在石墨电极上发生氧化反应
C.石墨电极附近溶液的pH 增大
D.溶液中Cl-向正极移动
难度: 中等查看答案及解析
-
在一定条件下,将3molA和1molB两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)=xC(g)+2D(g)。2 min时测得生成0.8 mol D、0.4 mol C。下列判断不正确的是
A. x=1
B. 2 min时,A的浓度为0.9mol·L-1
C. 2 min内A的反应速率为0.3 mol·L-1·min-1
D. B的转化率为60%
难度: 中等查看答案及解析
-
下列叙述中说明某化学平衡一定发生移动的是 ( )
A.反应物的转化率改变 B.正、逆反应速率改变
C.混合物中各组分的浓度改变 D.混合体系中气体密度发生变化
难度: 简单查看答案及解析
-
下列说法错误的是( )
A.化学键的断裂和形成是化学反应中能量变化的主要原因
B.铁在空气中被氧化属于吸热反应
C.化学反应中的能量变化,通常表现为热量的变化——放热或者吸热
D.放热反应和吸热反应取决于反应物的总能量与生成物的总能量的相对大小
难度: 简单查看答案及解析
-
下列有关说法中错误的是( )
A. 甲烷燃料电池用KOH作电解质,负极的电极反应式为CH4 - 8e-+10OH- =CO32- + 7H2O
B. Zn粒与稀硫酸反应制氢气时,滴加几滴CuSO4溶液可加快反应速率
C. 常温下用铜和铁作电极,浓硝酸作电解质溶液的原电池中铜为负极
D. 原电池中电子从负极出发,经外电路流向正极,再从正极经电解液回到负极
难度: 中等查看答案及解析
-
一定温度下,某体积不变的密闭容器进行的可逆反应:3A(s)
2B(g)+C(g),下列各关系中能说明反应已达到平衡状态的是( )
A.生成 B和C的速率比为2:1 B.生成2n molB同时生成n molC
C.混合气体的密度不变 D.混合气体的平均相对分子量不变
难度: 中等查看答案及解析
-
1 molX气体跟a molY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)
b Z(g)。反应达到平衡后,测得X的转化率为25%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b的数值可能是( )
A.a=2,b=1 B.a=1,b=2 C.a=2,b=2 D.a=3,b=2
难度: 中等查看答案及解析
-
下列事实不能用勒夏特列原理解释的是 ( )
A.密闭容器中有一定量红棕色的NO2,加压(缩小体积)后颜色先变深后变浅
B.高压条件比常压条件有利于SO2和O2合成SO3
C.由H2(g)、I2(g)、HI(g)组成的平衡体系加压(缩小体积)后颜色变深
D.实验室用排饱和食盐水的方法收集氯气
难度: 中等查看答案及解析
-
下列有关元素的性质及其递变规律正确的是
A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性从上到下依次减弱
D.同周期金属元素的化合价越高,其原子失电子能力越强
难度: 中等查看答案及解析
-
如图是甲醇燃料电池的结构示意图。电池总反应为:2CH3OH+3O2→2CO2+4H2O。下列说法正确的是( )
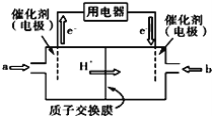
A. 左电极为电池的负极,a处通入的物质是空气
B. 右电极为电池的负极,b处通入的物质是甲醇
C. 负极反应式为:CH3OH+H2O-6e-= CO2+6H+
D. 正极反应式为:O2+2H2O -4e-= 4OH-
难度: 中等查看答案及解析
-
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
A. 若X+和Y2-的核外电子层结构相同,则原子序数:X>Y
B. 由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S
C. 硅、锗都位于金属与非金属的交界处,都可以做半导体材料
D. Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2
难度: 中等查看答案及解析
-
可逆反应aA(g)+bB(g)
cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是
A. T1<T2,Q>0
B. 增大压强,B的转化率减小
C. 当反应达平衡时,混合气体的密度不再变化
D. a+b>c+d
难度: 中等查看答案及解析
-
下列各组物质中化学键的类型相同的是( )
A.HCl、MgCl2、NH4Cl B.NH3、H2O、CO2
C.H2O、Na2O、CO2 D.CaCl2、NaOH、H2O
难度: 中等查看答案及解析
-
一定温度下,在体积为10L的密闭容器中,3molX和1molY进行反应:2X(g)+Y(g)
Z(g),经2min达到平衡,生成0.6mol Z,下列说法正确的是( )
A.以X浓度变化表示的反应速率为0.01 mol/(L·s)
B.将容器体积变为20L,Z的平衡浓度为原来的
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应是放热反应
难度: 中等查看答案及解析
-
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A
B
C
D
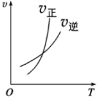

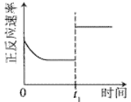

升高温度,正反应方向是放热反应
0~3s内,反应速率为:v(NO2)=0.2 mol·L-1·s-1
t1时仅加入催化剂,平衡正向移动
达平衡时,仅改变x,则x为c(O2)
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B
2C若维持温度和压强不变,当达到平衡时,容器的体积为V升,其中C气体的体积占10%,下列推断正确的是( )
①原混和气体的体积为1.2V升;
②原混和气体的体积为1.1V升;
③反应达平衡时气体A消耗掉0.05V升;
④反应达平衡时气体B消耗掉0.05V升。
A.②③ B.②④ C.①③ D.①④
难度: 简单查看答案及解析
