-
化学与社会、生产、生活密切相关。下列做法值得提倡的是
A.小苏打用作净水剂 B.“地沟油”加工为生物燃料
C.饮高度酒预防新冠肺炎 D.漂粉精作食品漂白剂
难度: 简单查看答案及解析
-
下列说法正确的是
A.氯气有氧化性,可使干燥布条漂白褪色
B.常温下,铁、铝不与浓硫酸反应,因此可用铁、铝容器贮存运输浓硫酸
C.已知电离能力H2CO3>HClO>
,则向氯水中加入碳酸氢钠晶体,能提高溶液中HClO的浓度
D.向BaCl2溶液中通入SO2可产生白色浑浊
难度: 中等查看答案及解析
-
异丁烯(
)是重要的化工原料,主要用于制备丁基橡胶、聚异丁烯塑料等。下列关于异丁烯的说法错误的是
A.异丁烯与HCl在一定条件下能发生加成反应且只能得到一种加成产物
B.异丁烯在一定条件下可以和氢气发生加成反应,加成产物的二氯代物有3种
C.异丁烯发生加聚反应生成聚异丁烯
D.异丁烯和环丁烷(
)互为同分异构体
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.1molN2与3molH2反应生成的NH3分子数为2NA
B.14g乙烯(C2H4)和丙烯(C3H6)混合气体中的原子总数为3NA
C.1molFe溶于过量硝酸,电子转移数为2NA
D.标准状况下,2.24LCCl4含有的共价键数为0.4NA
难度: 中等查看答案及解析
-
如图为乙酸丁酯制备的实验装置,下列说法正确的是

A.玻璃导管的主要作用是平衡试管内外压强
B.该装置适用于乙酸乙酯的制备
C.加入过量乙酸可以提高丁醇的转化率
D.分离提纯乙酸丁酯的方法是将混合物直接分液
难度: 简单查看答案及解析
-
某甲烷燃料电池构造示意图如图所示,关于该电池的说法不正确的是
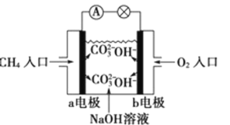
A.应该甲烷燃料电池的总反应:CH4+2O2=CO2+2H2O
B.正极的电极反应是:O2+2H2O+4e-=4OH-
C.a极是负极,发生氧化反应
D.甲烷燃料电池是环保电池
难度: 简单查看答案及解析
-
Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。下列说法正确的是
A.Y的原子半径比X的大
B.Q的最高价氧化物的水化物的酸性比Z的强
C.X、Y和氢3种元素形成的化合物中都只有共价键
D.Q的单质具有半导体的性质,Q与Z可形成化合物QZ4
难度: 简单查看答案及解析