-
某元素R最高价含氧酸的化学式为HaROb,则其最低价气态氢化物中R元素的化合价( )
A. 2b-a B. a-2b C. 8+a-2b D. 2b-a-8
难度: 简单查看答案及解析
-
把石灰石浸入盐酸中,下列措施能使反应速率增大的是( )
①加大盐酸用量 ②增大盐酸浓度 ③粉碎石灰石 ④增大体系压强
A.①③ B.②③
C.①④ D.③④
难度: 简单查看答案及解析
-
下列说法中不正确的是( )
A.充电电池不能无限制地反复充电、放电
B.燃料电池是一种高效且对环境友好的新型电池
C.化学电池的反应原理是自发的氧化还原反应
D.铅蓄电池和锌锰干电池都是可充电电池
难度: 简单查看答案及解析
-
金刚石和石墨是碳元素的两种结构不同的单质(同素异形体),在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热能,据此,试判断在100kPa下,下列结论正确的是( )
A.石墨比金刚石稳定
B.金刚石比石墨稳定
C.1mol石墨比1mol金刚石总能量高
D.金刚石转化为石墨是物理变化
难度: 中等查看答案及解析
-
某元素原子L层电子数是K层电子数的3倍,那么此元素是( )
A.F B.C
C.O D.N
难度: 简单查看答案及解析
-
关于
F-微粒叙述正确的是
A.质量数为19,电子数为9 B.质子数为9,中子数为10
C.质子数为9,电子数为9 D.中子数为10,电子数为8
难度: 简单查看答案及解析
-
下列各组物质中,化学键类型完全相同的是
A.SO2和NaOH B.CO2和H2O C.Cl2和HCl D.CCl4和KCl
难度: 简单查看答案及解析
-
下列有关叙述不正确的是
A.第三周期元素形成的简单离子的半径依次减小
B.HClO4、H2SO4、H3PO4、H2SiO3的酸性依次减弱
C.HCl、H2S、PH3的稳定性依次减弱
D.Na+、Mg2+、Al3+的氧化性依次增强
难度: 简单查看答案及解析
-
下列表示物质结构的化学用语正确的是( )
A.H、D、T表示同一种核素
B.CaCl2的电子式:
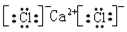
C.Cl-离子的结构示意图:
D.NH4Cl的电子式:
难度: 中等查看答案及解析
-
反应A+B→C分两步进行:①A+B→X(ΔH>0),②X→C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )
A.
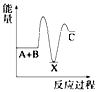 B.
B.
C.
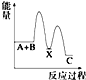 D.
D.
难度: 简单查看答案及解析
-
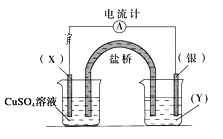
化学能可与热能、电能等相互转化。下列表述不正确的是( )
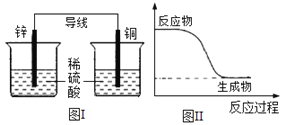
A. 化学反应中能量变化的主要原因是化学键的断裂与形成
B. 能量变化是化学反应的基本特征之一
C. 图I所示的装置能将化学能转变为电能
D. 图II所示的反应为放热反应
难度: 简单查看答案及解析
-
下列各项实验基本操作中,正确的是
A.为了加快锌和稀硫酸反应的速率,可以向稀硫酸中加入少量硫酸铜
B.在做中和滴定实验时清洗滴定管后,直接装液滴定
C.为了加快过滤速度,用玻璃棒搅拌过滤器中的液体
D.为了使配制的氯化铁溶液保持澄清,加入盐酸和铁片
难度: 简单查看答案及解析
-
反应A→C分两步进行:①A→B,②B→C。反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能)。下列说法错误的是( )
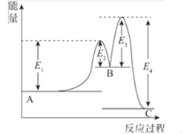
A. 三种物质中B最不稳定 B. A→B反应的活化能为E1
C. B→C反应的ΔH=E4-E3 D. 加入催化剂不能改变反应的焓变
难度: 困难查看答案及解析
-
在反应2A(g) + B(g)
3C(s) + 4D(g) 中,下列关系正确的是
A. 2ν(A)=ν(B) B. 3ν(B)=ν(C)
C. 4ν(C)=3ν(D) D. 2ν(A)=ν(D)
难度: 简单查看答案及解析
-
某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表一种元素,其中O点代表氢元素。下列说法中不正确的是
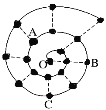
A.离O点越远的元素原子半径越大 B.虚线相连的元素处于同一族
C.B、C最高价氧化物对应的水化物可相互反应 D.A、B组成的化合物中可能含有共价键
难度: 中等查看答案及解析
-
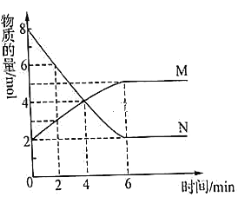
将等物质的量的A、B混合于2L的恒容密闭容器中,发生如下的反应:3A(g )+B(g)
xC(g)+2D(g),经5min后,测得D的量为1mol,C的平均反应速率为0.1mol/(L﹒min)。则x的值为( )
A.4 B.3 C.2 D.1
难度: 简单查看答案及解析