-
2020年,突如其来的疫情使全国人民都带起了口罩,以阻挡病毒的传播。通常人们戴的是一次性使用医科口罩(SMS)或防雾霾的3M(SMMMS)口罩,其原料都是聚丙烯。纺粘层即S层,其纤维直径比较粗,在20um左右;熔喷层即M层,纤维直径比较细,在2um左右。下列说法正确的是( )
A.聚丙烯可以使溴水或酸性高锰酸钾溶液褪色
B.用聚丙烯制作的餐具可供婴幼儿使用
C.熔喷层具有杀菌消毒功能
D.使用过的医科口罩只要还很干净,经酒精消毒后,用吹风机吹干,可再次使用
难度: 中等查看答案及解析
-
锡为ⅣA族元素,四碘化锡是常用的有机合成试剂(SnI4,熔点114.5℃,沸点364.5℃,易水解)。实验室以过量锡箔为原料通过反应Sn+2I2
SnI4制备SnI4,装置如图(夹持、加热装置略去)。下列说法正确的是( )
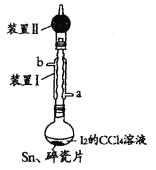
A.SnI4不溶于CCl4
B.装置Ⅰ中b为冷凝水进水口
C.加入碎瓷片的目的是防止暴沸
D.装置Ⅱ的主要作用是吸收挥发的I2
难度: 中等查看答案及解析
-
牛至是一种质地坚硬、树枝茂密的多年生药草。从牛至精油中提取的三种活性成分的结构简式如图所示。下列说法错误的是( )
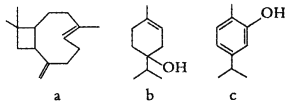
A.a、b、c均能发生加成反应和取代反应
B.b分子存在属于芳香族化合物的同分异构体
C.c分子中至少有8个碳原子共面
D.完全燃烧1mol三种物质时,消耗氧气的量a>b>c
难度: 中等查看答案及解析
-
第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态,其电路工作原理如图所示。下列说法中正确的是( )

A.放电时乙为正极,充电时乙为阴极
B.汽车上坡时发生图中虚线所示的过程
C.放电时负极的电极反应式为:MHn-ne-=M+nH+
D.电池充电时,OH-由甲侧向乙侧移动
难度: 困难查看答案及解析
-
由下列实验及现象推出的相应结论正确的是( )
选项
实验
现象
结论
A
相同条件下,用20mL1.0mol·L-1CH3COOH溶液和50mL1.0mol·L-1的盐酸分别做导电性实验
醋酸溶液对应的灯泡较暗
CH3COOH是弱电解质
B
某溶液中滴加K3[Fe(CN)6]溶液
产生蓝色沉淀
原溶液中有Fe2+,无Fe3+
C
将石蜡油蒸汽通过炽热的碎瓷片,产生的气体通入酸性高锰酸钾溶液
溶液紫红色褪去
产生的气体一定是乙烯
D
向鸡蛋清溶液中滴加饱和Na2SO4溶液
有白色不溶物析出
Na2SO4能使蛋白质变性
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
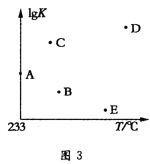
向20mL0.5mol·L-1的醋酸溶液中逐滴加入一定物质的量浓度的烧碱溶液,混合溶液的温度与所加NaOH溶液的体积关系如图所示。下列有关说法正确的是( )
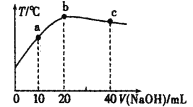
A.a点:c(CH3COOH)>c(OH-)+c(Na+)
B.醋酸的电离常数:b点<a点
C.b点:c(CH3COOH)+c(CH3COO-)=0.5mol·L-1
D.c点:n(OH-)-n(H+)-n(CH3COOH)=0.01mol
难度: 中等查看答案及解析
-
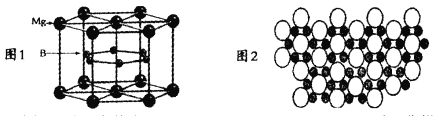
短周期主族元素W、X、Y、Z的原子序数依次增大,这四种元素仅处于两个周期,其中X元素的最外层电子数是其层数的3倍,这四种元素构成的一种离子化合物的结构如图所示。下列说法正确的是( )
A.原子半径Y>Z>X
B.单质W在其同族元素形成的单质中熔点最低
C.Z的最高价氧化物对应的水化物是中强酸
D.该化合物中的所有元素均满足8电子稳定结构
难度: 中等查看答案及解析


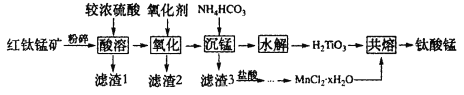


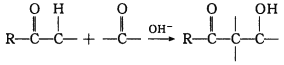
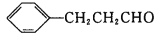 )的合成路线流程__(无机试剂任选)。
)的合成路线流程__(无机试剂任选)。