-
我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指
A.氨水 B.硝酸 C.醋 D.卤水
难度: 简单查看答案及解析
-
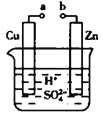
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关。下列各组物质在反应中的产物与物质的浓度有关的是( )
①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液
A.①③
B.③④
C.①②
D.①③④
难度: 中等查看答案及解析
-
下列措施不合理的是
A.用SO2漂白纸浆和草帽辫 B.用硫酸清洗锅炉中的水垢
C.高温下用焦炭还原SiO2制取粗硅 D.用 Na2S作沉淀剂,除去废水中的Cu2+和Hg2+
难度: 中等查看答案及解析
-
a、b、c、d为短周期元素,a的原子中只有1个电子,b2−和C+离子的电子层结构相同,d与b同族。下列叙述错误的是
A.a与其他三种元素形成的二元化合物中其化合价均为+1
B.b与其他三种元素均可形成至少两种二元化合物
C.c的原子半径是这些元素中最大的
D.d和a形成的化合物的溶液呈弱酸性
难度: 中等查看答案及解析
-
几种短周期元素的原子半径及主要化合价如下表:
元素代号
X
Y
Z
W
原子半径/pm
160
143
70
66
主要化合价
+2
+3
+5、+3、-3
-2
下列叙述正确的是
A.X、Y元素的金属性X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.同周期主族元素的原子半径以ⅦA族的为最大
B.同主族两种元素原子的核外电子数的差值可能为32
C.短周期中次外层电子数是最外层电子数2倍的元素一定是非金属元素
D.科学家在周期表中金属与非金属分界线处找到了优良的催化剂
难度: 简单查看答案及解析
-
关于化学键的叙述正确的是
A.离子化合物中只存在离子键
B.非金属元素组成的化合物中可能存在离子键
C.由不同种元素组成的多原子分子里,一定只存在极性共价键
D.含金属元素的化合物中一定存在离子键
难度: 简单查看答案及解析
-
下列各组中的性质比较正确的是( )
①酸性:HClO4>HBrO4>HIO4 ②碱性:KOH>Ca(OH)2>Mg(OH)2 ③稳定性:HCl>H2S>PH3 ④还原性:F->Cl->Br- ⑤熔点:Li<Na<K<Rb<Cs
A. ①③⑤ B. ②③④ C. ①②③ D. ③④⑤
难度: 中等查看答案及解析
-
下列表示物质的化学用语正确的是( )
A.8个中子的碳原子的核素符号:12C
B.HF的电子式:H+[
]-
C.Cl-离子的结构示意图:
D.CO2的结构式:O=C=O
难度: 简单查看答案及解析
-
若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的粒子间的主要相互作用依次是
A.氢键、氢键、共价键
B.氢键、氢键、离子键
C.氢键、共价键、分子间作用力
D.分子间作用力、氢键、共价键
难度: 简单查看答案及解析
-
检验铵盐的方法是将待检物取出少量放入试管中,然后( )
A.加热,用红色石蕊试纸放在试管口检验
B.加水溶解,用红色石蕊试纸检验溶液的酸碱性
C.加入碱溶液,加热,再滴入酚酞溶液
D.加入苛性钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验
难度: 简单查看答案及解析
-
燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极。下列叙述不正确的是( )。
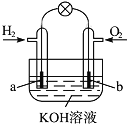
A.氢氧燃料电池是一种具有应用前景的绿色电源
B.a极是负极,该电极上发生氧化反应
C.总反应方程式为2H2+O2=2H2O
D.b极反应是O2+4OH--4e-=2H2O
难度: 中等查看答案及解析
-
为了说明影响化学反应快慢的因素,某同学分别设计了如下A~D四个实验,你认为结论不正确的是( )
A.将大小、形状相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大
B.在相同条件下,等质量的大理石块和大理石粉与相同浓度的盐酸反应,大理石粉反应快
C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解
D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同
难度: 简单查看答案及解析
-
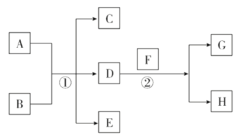
如图所示,对 A 生成 C 的反应,下列结论正确的是( )

A.该反应为吸热反应
B.该反应进行时,一定有能量放出
C.A 比 C 稳定
D.该反应不需要加热一定就可以进行
难度: 简单查看答案及解析
-
下列说法中不正确的是( )
A.当一个可逆反应达到平衡状态时,就是这个反应在该条件下所能达到的限度
B.当一个可逆反应达到平衡状态时,这个反应的正反应速率和逆反应速率相等
C.可以通过控制反应条件,使2 mol SO2与1 mol O2反应生成2 mol SO3
D.化学反应的限度可以通过改变条件来改变
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.氢氧化钠晶体熔化时只破坏了离子键
B.HCl、HBr、HI均是强酸
C.BF3分子中所有原子的最外层都达到8电子稳定结构
D.碘升华只克服了分子间作用力
难度: 简单查看答案及解析
-
应用元素周期律分析下列推断,其中正确的组合是
①碱金属单质的熔点随原子序数的增大而降低
②砹(At)是VIIA族,其氢化物的稳定性大于HC1
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(Tl)与铝同主族,其单质既能与盐酸反应又能与氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
A.①③④ B.①③⑥ C.③④⑤ D.②④⑥
难度: 中等查看答案及解析
-
如图所示是
的两个性质实验,下列有关说法中正确的是
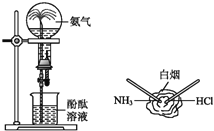
A. 两个实验均表现了
易溶于水
B. 两个实验均表现了
易挥发
C. 两个实验均表现了
是碱性气体
D. 两个实验均表现了
是还原性气体
难度: 简单查看答案及解析
-
如图所示为元素周期表的一部分,其中X、Y、Z、W为四种短周期元素。Z元素原子核外K层与M层上的电子数相等。下列说法中正确的是( )
A.Y元素的最高价氧化物对应的水化物的化学式为H3YO4
B.Y的最简单气态氢化物的水溶液显弱碱性
C.原子半径由小到大的顺序为X<Z<Y<W
D.X、Z两种元素的氧化物中所含化学键的类型相同
难度: 中等查看答案及解析
-
下列电子式或用电子式表示化合物形成过程正确的是( )
A.NH
B.CCl4
C.MgCl2
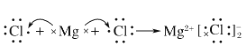
D.HCl
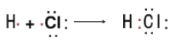
难度: 中等查看答案及解析
-
根据原子结构及元素周期律的知识,下列推断正确的是( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐增大
D.
Cl与
Cl得电子能力相同
难度: 中等查看答案及解析
-
在一定温度下的恒容密闭容器中,能说明反应X2(g)+Y2(g)
2XY(g)已达到平衡的是
A. 容器内的总压不随时间变化 B. 容器中气体的平均相对分子质量不随时间变化
C. XY气体的物质的量分数不变 D. X2和Y2的消耗速率相等
难度: 简单查看答案及解析
-
用以下三种途径来制取相同质量的硝酸铜:①铜跟浓硝酸反应,②铜跟稀硝酸反应,③铜跟氧气反应生成氧化铜,氧化铜再跟稀硝酸反应。以下叙述正确的是( )
A.三种途径所消耗的铜的物质的量不相等
B.三种途径所消耗的硝酸的物质的量相等
C.所消耗铜的物质的量:途径③>途径①>途径②
D.所消耗硝酸的物质的量:途径①>途径②>途径③
难度: 中等查看答案及解析
-
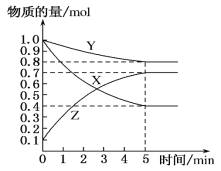
已知某反应的各物质浓度数据如下:
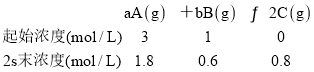
据此可推算出上述反应化学方程式中,各物质的化学计量数之比是( )
A.9:3:4 B.2:1:3 C.3:1:2 D.3:2:1
难度: 简单查看答案及解析