-
下列属于电解质的是
A. 明矾 B. 盐酸 C. 氨气 D. 钾钠合金
难度: 中等查看答案及解析
-
下列关于电解质说法正确是( )
A. 能导电的物质叫电解质 B. NaCl晶体不导电,所以NaCl不是电解质
C. 熔融的KOH导电,所以KOH是电解质 D. 电解质在通电时发生电离
难度: 中等查看答案及解析
-
下列各组物质,前者属于电解质,后者属于非电解质的是( )
A.NaCl晶体、BaSO4 B.铜、二氧化硫
C.硫酸、乙醇 D.熔融的KNO3、硫酸溶液
难度: 简单查看答案及解析
-
已知某溶液中存在H+、Ba2+、Fe3+三种阳离子,则其中可能大量存在的阴离子是( )
A.SO
B.CO
C.NO
D.OH-
难度: 简单查看答案及解析
-
在无色透明溶液中,能大量共存的离子组是( )
A.Mg2+、Na+、SO
B.K+、H+、HCO
C.Cu2+、NO
、SO
D.Ba2+、NO
、CO
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是( )
A.钠与水反应:Na+2H2O=Na++2OH-+H2↑
B.稀盐酸与苏打溶液反应:HCO3-+H+=CO2↑+H2O
C.向次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
D.铁盐腐蚀铜质电路板:2Fe3++Cu=2Fe2++Cu2+
难度: 中等查看答案及解析
-
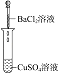
下列实验过程中产生的现象与图形相符合的是( )

A.稀硫酸滴加到 B a (O H)2 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
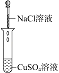
B.铁粉加到一定量 CuSO4 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量)
C.CO2 通入一定量 NaOH 溶液中(横坐标是 CO2 的体积,纵坐标为溶液的导电能力)
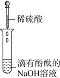
D.稀盐酸滴加到一定量 NaOH 溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)
难度: 中等查看答案及解析
-
下表中对离子方程式的评价合理的是
选项
化学反应及其离子方程式
评价
A
H2SO4溶液与Ba(OH)2溶液反应: H++ SO42-+Ba2++OH−
BaSO4↓+H2O
正确
B
向碳酸镁浊液中加入足量稀盐酸:
CO32-+2H+
CO2↑+H2O
错误,碳酸镁不应写成离子形式
C
向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O
Fe(OH)3↓+3H+
正确
D
向NaOH溶液中通入少量CO2反应:OH−+CO2
HCO3-
正确
A. A B. B C. C D. D
难度: 中等查看答案及解析