-
将1.92g铜粉投入到某硫酸和硝酸的混合溶液中,其中,硫酸以及硝酸的浓度均为1mol/L,溶液体积为40mL,待充分反应后若只生成NO气体,则最多可收集到标准状况下的NO体积为( )
A. 336 mL B. 112 mL C. 448 mL D. 224 mL
难度: 中等查看答案及解析
-
化学在生产和日常生活中有着重要的应用。下列说法正确是
A.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2
B.向煤中加入适量石灰石,使煤燃烧产生的SO2最终生成CaSO3,可减少对大气的污染
C.高纯度的硅单质广泛用于制作光导纤维
D.大量燃烧化石燃料排放的废气中含CO2、SO2,从而使雨水的pH=5.6形成酸雨
难度: 简单查看答案及解析
-
下列不能说明氯元素的非金属性比硫元素强的事实是
①HCl比H2S稳定
②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤氯原子最外层有7个电子,硫原子最外层有6个电子
A. ②⑤ B. ①② C. ①②④ D. ①③⑤
难度: 中等查看答案及解析
-
下列关于卤族元素由上到下性质递变规律的叙述,正确的是( )
①单质的氧化性增强 ②单质的颜色加深 ③气态氢化物的稳定性增强 ④单质的沸点升高 ⑤阴离子的还原性增强
A.①②③ B.②③④ C.②④⑤ D.①③⑤
难度: 简单查看答案及解析
-
下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是
A.CuCl2 B.FeCl2 C.FeCl3 D.AlCl3
难度: 中等查看答案及解析
-
下列关于元素周期表的叙述正确的是( )
A.周期表中有八个主族,八个副族
B.目前使用的元素周期表中,最长的周期含有32种元素
C.短周期元素是指1~20号元素
D.原子的最外层电子数都等于该元素所在的族序数
难度: 中等查看答案及解析
-
下列说法正确的是
A.原子最外层电子数等于或大于3(小于8)的元素一定是非金属元素
B.原子最外层只有1个电子的元素一定是金属元素
C.最外层电子数比次外层电子数多的元素一定位于第二周期
D.某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期
难度: 中等查看答案及解析
-
某元素最高价氧化物对应水化物的化学式为H2XO3。这种元素的气态氢化物的化学式是( )
A.HX B.H2X C.XH3 D.XH4
难度: 简单查看答案及解析
-
下列关于物质性质的叙述中,正确的是( )
A.Cl2能与金属活动顺序表中大多数金属反应
B.N2是大气中的主要成分之一,雷雨时,可直接转化为NO2
C.硫是一种淡黄色的能溶于水的晶体,既有氧化性又有还原性
D.硅是应用广泛的半导体材料,常温下化学性质活泼
难度: 中等查看答案及解析
-
高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
SiO2
Si(粗)
SiHCl3
Si(纯),下列说法正确的是( )
A.步骤①的化学方程式为SiO2+C
Si+CO2↑
B.步骤①、②、③中每生成或反应1 mol Si,转移4 mol电子
C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D.SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点67.6 ℃),通过蒸馏(或分馏)可提纯SiHCl3
难度: 中等查看答案及解析
-
从海带中提取碘单质,成熟的工艺流程如下,下列关于海水制碘的说法,不正确的是
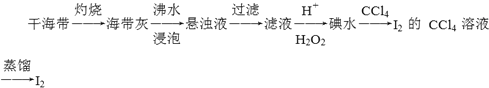
A.实验室在蒸发皿中灼烧干海带,并且用玻璃搅拌
B.含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C.在碘水中加入几滴淀粉溶液,溶液变蓝色
D.碘水中加入CCl4得到I2的CCl4的溶液,该操作为“萃取”
难度: 简单查看答案及解析
-
“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是
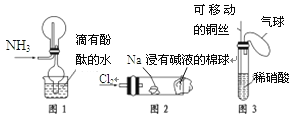
①实验室收集氨气采用图1所示装置
②实验室做氯气与钠的反应实验时采用图2所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
④实验室中采用图3所示装置进行铜与稀硝酸的反应
A. ②③④ B. ①②③ C. ①②④ D. ①③④
难度: 中等查看答案及解析
-
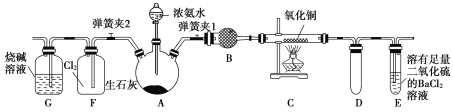
如图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( )

A.a—b—c—d—e—f—g—h B.a—e—d—c—b—h—i—g
C.a—d—e—c一b—h—i—g D.a—c—b—d—e 一h—i—f
难度: 中等查看答案及解析
-
如图所示,相同条件下,两个容积相同的试管分别装满NO2和NO气体,分别倒置于水槽中,然后通过导管缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内充满液体。假设试管内的溶质不向水槽中扩散,则两个试管内溶液物质的量浓度之比为

A.1∶1 B.5∶7 C.7∶5 D.4∶3
难度: 简单查看答案及解析
-
工业上通过氮气和氢气反应合成氨,氨经一系列反应可以得到硝酸。反应历程如下图所示,下列说法不正确的是( )

A. 氨可用作制冷剂
B. 铵态氮肥一般不能与碱性化肥共同使用
C. 硝酸可用于制化肥、农药、炸药、染料、盐类等
D. 某浓硝酸中含有溶质2mol,标准状况下,该浓硝酸与足量的铜完全反应能生成1mol
难度: 中等查看答案及解析
-
将3mol的NO2气体依次通入下列三个分别装有足量①NaHCO3饱和溶液、②浓H2SO4、③Na2O2的装置后,用排水法把残留气体收集起来,则收集到的气体是(同温、同压下测定)( )
A.1mol NO B.1mol NO2和0.05mol O2 C.2mol O2 D.0.25mol O2
难度: 中等查看答案及解析
-
用如图所示实验装置进行物质性质的探究实验。下列说法不合理的是( )
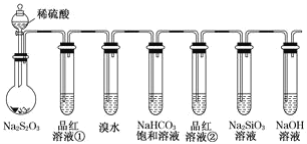
A.若品红溶液①褪色,则说明产物中含有SO2
B.若溴水褪色,则说明SO2具有还原性
C.若烧瓶中产生黄色浑浊和无色气泡,则说明Na2S2O3只作氧化剂
D.若品红溶液②不褪色、Na2SiO3溶液中出现白色浑浊,则说明硅酸比碳酸的酸性弱
难度: 中等查看答案及解析
-
下列各组物质中,任意两种物质在常温下均能发生反应的是( )
选项
甲
乙
丙
A
NH3
CuO
稀 HNO3
B
A1
盐酸
Fe2O3
C
Si
O2
H2
D
SO2
NaOH溶液
新制氯水
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
右图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴定管内盛放某种液体。挤压滴管的胶头,下列与实验事实不相符的是( )

A.CO2(NaHCO3溶液)/无色喷泉 B.NH3(H2O含酚酞)/红色喷泉
C.H2S(CuSO4溶液)/黑色喷泉 D.HCl(AgNO3溶液)/白色喷泉
难度: 中等查看答案及解析
-
浓硫酸与下列物质作用时,既表现氧化性,又表现酸性的是( )
①炽热的木炭 ②H2S气体 ③Cu(加热条件下) ④FeO ⑤NH3 ⑥蔗糖 ⑦CuSO4·5H2O ⑧铁、铝(常温下)
A.③④ B.①②⑤⑧ C.①②③④⑦ D.⑥⑦
难度: 简单查看答案及解析
-
对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则该溶液中一定不含K+
难度: 中等查看答案及解析
-
在15.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀,则下列表示气体X组成的选项中合理的是
A.0.3 mol NO、0.1 mol NO2
B.0.3 mol NO2、0.1 mol NO
C.0.6 mol NO
D.0.3 mol NO2
难度: 中等查看答案及解析
-
将甲气体通入BaCl2溶液,未见沉淀生成,然后通入乙气体,有沉淀生成,则甲、乙气体不可能是
A.SO2、H2S B.SO2、NO2 C.NH3、CO2 D.CO2、SO2
难度: 简单查看答案及解析
-
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素 X。它们有如图所示的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
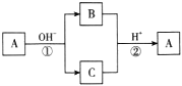
A.X元素不一定为非金属元素 B.单质A可能是Cl2,不能是S
C.反应①和②一定为氧化还原反应 D.反应①和②都为复分解反应
难度: 中等查看答案及解析
-
某核素原子核内质子数为m,中子数为n,则下列叙述中正确的是
A.不能由此确定该元素的相对原子质量
B.这种元素的相对原子质量为m+n
C.若碳原子质量为ωg,则此原子的质量为(m+n)ωg
D.核内中子的总质量小于质子的总质量
难度: 中等查看答案及解析
-
我国稀土资源丰富。下列有关稀土元素
与
的说法正确的是( )
A.
与
互为同位素 B.
与
的质量数相同
C.
与
是同一种核素 D.
与
的核外电子数和中子数均为62
难度: 简单查看答案及解析
-
某元素的一个原子形成的离子可表示为
n-,下列说法正确的是( )
A.
n-中含有的中子数为a+b
B.
n-中含有的电子数为a-n
C.X原子的质量数为a+b+n
D.一个X原子的质量约为
g
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.碱金属元素单质的熔点随原子序数递增而降低
B.同种元素的原子均有相同的质子数和中子数
C.族序数等于其周期序数的元素一定是金属元素
D.ⅦA 族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
难度: 简单查看答案及解析
-
今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是
A.原子半径:W<X
B.常温常压下,Y单质为固态
C.气态氢化物热稳定性:Z<W
D.X的最高价氧化物的水化物是强碱
难度: 中等查看答案及解析
-
下列事实不能用元素周期律解释的是( )
A.气态氢化物的稳定性:HBr>HI B.在短周期中,金属性最强的元素是钠,非金属性最强的元素是氟
C.向Na2SO3溶液中加盐酸,有气泡产生 D.镁条、铝片分别与同浓度盐酸反应,Mg的反应更容易
难度: 中等查看答案及解析