-
某溶液中可能含有Na+、Fe2+、NH4+、K+、Cl-、SO42-、SO32-中的几种,且所含离子物质的量浓度均为0.01mol/L。向溶液中滴加少量溴水后,溶液呈无色。下列关于该溶液的判断正确的是( )
A. 可能含有Na+ B. 可能含有SO42- C. 一定不含Cl- D. 一定含有NH4+
难度: 困难查看答案及解析
-
能够用键能解释的是
A.氮气的化学性质比氧气稳定 B.常温常压下,溴呈液体,碘为固体
C.稀有气体一般很难发生化学反应 D.硝酸易挥发,硫酸难挥发
难度: 简单查看答案及解析
-
化学与生活密切相关。下列有关物质用途的说法错误的是
A.液氨能做制冷剂 B.氯气可用于海水提溴
C.过氧化钠可用作航天员的供氧剂 D.碳酸钡可用于胃肠X射线造影检查
难度: 简单查看答案及解析
-
将后者逐渐滴入(或通入)前者至过量,有沉淀产生且最终消失的是( )
A.氯化铝、氨水 B.氢硫酸、氧气
C.硫酸铝、氢氧化钠 D.氯化亚铁、氯气
难度: 简单查看答案及解析
-
按原子序数递增的顺序(稀有气体除外),对第三周期元素性质的描述正确的是( )
A.原子半径和离子半径均减小
B.氧化物对应的水化物碱性减弱,酸性增强
C.单质的晶体类型金属晶体、原子晶体和分子晶体
D.单质的熔点降低
难度: 中等查看答案及解析
-
以下性质的比较中,错误的是
A.酸性:H2CO3>H2SiO3>H3AlO3 B.沸点:HCl>HBr >HI
C.热稳定性:HF>HCl>H2S D.碱性:KOH>NaOH>Mg(OH)2
难度: 中等查看答案及解析
-
下列事实不能用勒夏特列原理解释的是
A.用浓氨水和氢氧化钠制取氨气
B.加热蒸干AlCl3溶液不能得到无水AlCl3
C.工业上SO2和O2在常压下生成SO3
D.水中的c(H+)比0.1 mol/LNaOH溶液中的大
难度: 中等查看答案及解析
-
能用离子方程式H++ OH-→ H2O 表示的反应是
A.氨水和盐酸 B.氢氧化钠溶液和醋酸
C.硫酸和氢氧化钡溶液 D.硝酸和澄清石灰水
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A.1L0.1mol·L-1的氨水中含有的NH3分子数为0.1NA
B.标准状况下,2.24L的CCl4中含有的C-Cl键数为0.4NA
C.14g由乙烯与环丙烷组成的混合气体含有的碳原子数目为NA
D.常温常压下,Na2O2与足量CO2反应生成2.24L O2,转移电子数为0.2NA
难度: 中等查看答案及解析
-
在强酸性条件下因发生氧化还原反应不能大量共存的是
A.Mg2+、Na+、SO42-、Cl- B.K+、CO32-、Cl-、NO3-
C.Na+、Cl-、NO3-、Fe2+ D.NH4+、OH-、SO42-、NO3-
难度: 中等查看答案及解析
-
如图分别表示红磷、白磷燃烧时的能量变化,有关说法正确的是( )
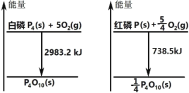
A.白磷比红磷稳定
B.白磷燃烧产物比红磷燃烧产物稳定
C.1mol 白磷转变为红磷放出 2244.7kJ 的热量
D.红磷燃烧的热化学方程式:4P(s)+5O2(g)→P4O10(s)+2954kJ
难度: 中等查看答案及解析
-
下列有关物质性质的比较,错误的是
A.溶解度:小苏打 < 苏打 B.密度:溴乙烷 > 水
C.硬度:晶体硅 < 金刚石 D.碳碳键键长:乙烯 > 苯
难度: 简单查看答案及解析
-
下列关于饱和食盐水的用途及装置设计正确的是

A.a-模拟工业制纯碱 B.b-制乙酸乙酯实验中接受产物
C.c-除去氯化氢中的氯气 D.d-实验室制乙炔
难度: 中等查看答案及解析
-
下列实验中的颜色变化,与氧化还原反应无关的是
A
B
C
D
实验
NaOH溶液滴入FeSO4溶液中
石蕊溶液滴入氯水中
Na2S溶液滴入AgCl浊液中
热铜丝插入稀硝酸中
现象
产生白色沉淀,随后变为红褐色
溶液变红,随后迅速褪色
沉淀由白色逐渐变为黑色
产生无色气体,随后变为红棕色
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列有机物中含有少量杂质
括号中是杂质
,除杂方法正确的是
A.乙醇
乙酸
:加入碳酸钠溶液,振荡,静置,分液
B.硝基苯
硫酸
:将其加入NaOH溶液中,振荡,静置,分液
C.乙醛
乙酸乙酯
:加入氢氧化钠溶液,振荡,静置,分液
D.溴乙烷
溴
:加入四氯化碳,振荡,静置,分液
难度: 中等查看答案及解析
-
用测量压强的仪器测定生铁在90%醋酸溶液中发生腐蚀的装置及容器内压强随时间变化如图所示,下列分析错误的是

A.0~t1,可能发生了析氢腐蚀压强增大
B.0~t1,可能反应放热温度升高压强增大
C.t2时压强小于起始压强,一定发生了吸氧腐蚀
D.整个过程中铁粉发生了还原反应生成Fe2+
难度: 中等查看答案及解析
-
40℃硝酸钾饱和溶液先升温至80℃,在恒温下蒸发部分溶剂至析出少量溶质,然后将溶液逐渐冷却至60℃。下列示意图中能正确表示整个过程中溶液浓度a%与时间t关系的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
测定0.1mol·L-1Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻
①
②
③
④
温度/℃
25
30
40
25
pH
9.66
9.52
9.37
9.25
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比试验,④产生白色沉淀多。下列说法错误的是( )
A. Na₂SO3溶液中存在水解平衡:SO32-+H2O
HSO-3+OH-
B. ④的pH与①不同,是由于SO32-浓度减小造成的
C. ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D. ①与④的Kw值相等
难度: 困难查看答案及解析
-
25℃时,在10 mL浓度均为0.1 mol/L的醋酸和盐酸的混合溶液中,滴加0.1 mol/L的NaOH溶液V mL,则溶液中粒子浓度关系正确的是
A.V=0时:c(H+) >c(Cl-)=c(CH3COOH)
B.V=10 mL时:c(OH-)+c(CH3COO-)=c(H+)
C.V=20 mL时:c(Na+)=c(CH3COO-)+c(Cl-)
D.加入NaOH溶液至pH=7时,V > 20 mL
难度: 中等查看答案及解析
-
用以下图示装置研究物质的性质,能够获得可靠结论的是
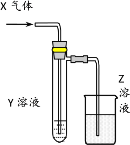
X
Y
Z
结论
A
HCHO
新制Cu(OH)2
NaOH(aq)
验证甲醛的还原性
B
CH3Cl
AgNO3(aq)
NaOH(aq)
验证一氯甲烷含氯元素
C
SO2
KMnO4(aq)
NaOH(aq)
验证二氧化硫的漂白性
D
Cl2
淀粉KI(aq)
NaOH(aq)
验证氯气的强氧化性
A.A B.B C.C D.D
难度: 中等查看答案及解析

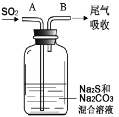
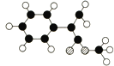
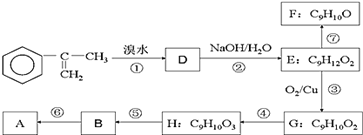
 的合成路线。________。(合成路线常用的表示方式为:A
的合成路线。________。(合成路线常用的表示方式为:A B……
B……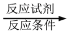 目标产物)
目标产物)