-
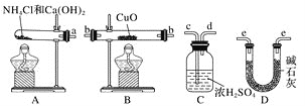
用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是
①二氧化碳 ②氯化氢 ③水蒸气 ④氧气
A. ①②③ B. ②③④ C. ②③ D. ①④
难度: 中等查看答案及解析
-
过滤实验中,有关仪器的作用不正确的是( )
A. 玻璃棒用来搅拌溶液 B. 玻璃棒用来引流溶液
C. 烧杯用来承接滤液 D. 漏斗用来制作过滤器
难度: 简单查看答案及解析
-
在体积相同的两个密闭容器中分别充满O2、O3气体,当两个容器内温度和气体密度相等时,说法正确的是 ( )
A.两种气体的压强相等 B.O2比O3质量小
C.两种气体的分子数目相等 D.两种气体的氧原子数目相等
难度: 简单查看答案及解析
-
用NA代表阿伏加德罗常数的值,下列说法中不正确的是
A.16 g氧气和臭氧的混合物中含有氧原子数为NA
B.44 g CO2与28 g CO所含有的分子数都为NA
C.46 g NO2和N2O4的混合物含有的分子数为NA
D.NA个氮分子与NA个氧分子的质量比为7∶8
难度: 简单查看答案及解析
-
下列变化中需加入氧化剂才能实现的是( )
A.Cl﹣→Cl2 B.Fe3+→Fe2+
C.CuO→Cu D.H2SO4→BaSO4
难度: 简单查看答案及解析
-
下列有关物质的分类中,不合理的是( )
A.NaOH(强碱) B.CO2(氧化物)
C.H2SO4(弱酸) D.盐酸(混合物)
难度: 简单查看答案及解析
-
自来水厂常使用氯气消毒,市场上有些小商小贩用自来水充当纯净水出售。下列试剂中,可用来辨其真伪的是( )
A. 酚酞溶液 B. 氯化钡溶液 C. 氢氧化钠溶液 D. 硝酸银溶液
难度: 简单查看答案及解析
-
将表面已完全钝化的铝条,插入下列溶液中,一段时间后不会有气泡冒出的是
A.稀硫酸 B.稀盐酸 C.浓硫酸 D.氢氧化钠溶液
难度: 简单查看答案及解析
-
以下电离方程式错误的是
A.MgCl2=Mg2++2Cl- B.Fe2(SO4)3=2Fe3++3SO42-
C.NaHCO3=Na++H++CO32- D.KHSO4=K++H++SO42-
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B. 25 ℃,1.01×105Pa,64gSO2中含有的原子数为3NA
C. 在常温常压下,11.2LCl2含有的分子数为0.5NA
D. 标准状况下,11.2LH2O含有的分子数为0.5NA
难度: 中等查看答案及解析
-
氯化钠溶液含有少量的氯化铁。若要得到纯净的固体氯化钠,可供选择的操作有:①加适量盐酸溶液、②加金属铁粉、③蒸发结晶、④加过量氢氧化钠溶液、⑤冷却热饱和溶液、⑥过滤。正确的操作步骤是( )
A. ②⑥③ B. ④⑥①③ C. ④⑥③⑤ D. ②⑥①③⑤
难度: 中等查看答案及解析
-
要除去NaCl溶液中混有的MgCl2应选用的试剂和操作方法是( )
A.加入适量Na2SO4溶液后过滤 B.加入适量NaOH溶液后过滤
C.加入过量NaOH溶液后蒸发 D.加入过量Na2CO3溶液后过滤
难度: 简单查看答案及解析
-
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3∶2∶1时,三种溶液中Cl-的物质的量之比为( )
A.1∶1∶1 B.1∶2∶3 C.3∶2∶1 D.3∶4∶3
难度: 简单查看答案及解析
-
向紫色石蕊试液中加入过量Na2O2粉末,充分振荡,可观察到的现象是( )
A. 溶液仍为紫色
B. 除最终溶液褪色外,无其他现象
C. 溶液最终变为蓝色
D. 溶液中有气泡产生,溶液最终变为无色
难度: 中等查看答案及解析
-
“84消毒液”在日常生活中被广泛使用,该消毒液无色,pH大于7,对某些有色物质有漂白作用。已知,强酸弱碱形成的盐溶液呈碱性,则你认为“84消毒液”的有效成分是( )
A.氯化氢 B.次氯酸钠 C.高锰酸钾 D.碳酸钠
难度: 简单查看答案及解析
-
下列化合物中,只有在水溶液中才能导电的电解质是( )
A.氯化钠 B.酒精 C.硫酸 D.二氧化碳
难度: 简单查看答案及解析
-
关于二氧化氮的下列说法中不正确的是( )
A.二氧化氮是一种红棕色气体
B.二氧化氮是造成酸雨的气体之一
C.二氧化氮易溶于水,不能用排水法收集
D.氮气与氧气反应可直接生成二氧化氮
难度: 简单查看答案及解析
-
已知某酸性溶液中含有Ba2+、Fe3+,则下述离子组中能与上述离子共存的是( )
A.CO32-、Cl- B.NO3-、Cl- C.NO3-、SO42- D.OH-、NO3-
难度: 简单查看答案及解析
-
下列离子方程式正确的是
A. 向盐酸中滴加氨水:H++OH-=H2O
B. 氯化钙与碳酸氢钾溶液混合:Ca2++CO32-=CaCO3↓
C. 氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O
D. Ca(HCO3)2溶液中加入过量KOH溶液:Ca2++HCO3﹣+OH﹣═CaCO3↓+H2O
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值.下列有关叙述正确的是( )
A. l mol OH﹣所含电子数为10NA
B. 2L0.5 mol•L﹣1Na2SO4溶液中阴离子所带电荷数为0.2NA
C. 标准状况下,1.12 L CC14含有的氯原子数为0.2NA
D. 14 g由CO和N2组成的混合气体中含有的分子总数为NA
难度: 中等查看答案及解析
-
某国外化学教材中有一张关于氧化还原反应的插图:由图可知,
在该反应中是( )
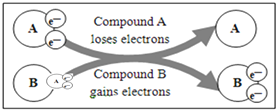
A. 还原剂 B. 氧化剂 C. 氧化产物 D. 还原产物
难度: 简单查看答案及解析
-
《神农本草经》说:“水银…镕化(加热)还复为丹。”《黄帝九鼎神丹经》中的“柔丹”、“伏丹”都是在土釜中加热Hg制得的。这里的“丹”是指( )
A.氯化物 B.合金 C.硫化物 D.氧化物
难度: 简单查看答案及解析
-
下列关于硝酸的说法不正确的是( )
A.浓硝酸是一种易挥发的液体混合物
B.浓硝酸在空气中敞口放置,因吸收水蒸气而浓度减小
C.浓硝酸不稳定,易分解生成二氧化氮、氧气和水
D.常温下,浓硝酸常保存在棕色试剂瓶中
难度: 简单查看答案及解析
-
在标准状况下,质量为m的气体A与质量为n的气体B的分子数相同,下列说法中不正确的是( )
A.气体A与气体B的相对分子质量比为m:n
B.同质量气体A与气体B的分子个数比为n:m
C.同温同压下,A气体与B气体的密度比为n:m
D.相同状况下,同体积的A气体与B气体的质量比为m:n
难度: 中等查看答案及解析
-
下列有关二氧化硅的叙述正确的是( )
A.二氧化硅不与任何酸反应
B.二氧化硅能与水反应生成硅酸
C.二氧化硅是酸性氧化物,能与烧碱溶液反应
D.二氧化硅是两性氧化物,能与碱和氢氟酸反应
难度: 简单查看答案及解析