-
具有下列性质的物质可能属于离子晶体的是
A. 熔点801 ℃,易溶于水 B. 熔点10.31 ℃,液态不导电
C. 熔点112.8 ℃,能溶于CS2 D. 熔点97.81 ℃,固态能导电
难度: 简单查看答案及解析
-
能说明二氧化硫具有还原性的事实是
A.使品红溶液褪色 B.使溴水褪色
C.与氢硫酸反应 D.与烧碱反应
难度: 中等查看答案及解析
-
按照有机物的命名规则,下列命名正确的是
A.1,2-二甲基戊烷 B.2-乙基丁烷
C.3-乙基己烷 D.3,4-二甲基戊烷
难度: 中等查看答案及解析
-
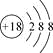
U是重要的核工业原料,在自然界的丰度很低。
U的浓缩一直为国际社会所关注。下列有关
U的说法中正确的是( )
A.
U原子核中含有92个中子 B.
U原子核外有143个电子
C.
U与
U互为同位素 D.
U与
U互为同素异形体
难度: 简单查看答案及解析
-
既能和盐酸反应,又能和氢氧化钠溶液反应的物质是( )
A.Fe B.Fe2O3 C.Al D.AlCl3
难度: 简单查看答案及解析
-
有关HF和HCl判断正确的是
A.键长:HF>HCl B.键能:HF>HCl
C.稳定性:HCl>HF D.共用电子对偏移程度:HCl>HF
难度: 中等查看答案及解析
-
可用来鉴别乙醇、乙醛的试剂是
A.银氨溶液 B.乙酸溶液 C.氯化铁溶液 D.氢氧化钠溶液
难度: 简单查看答案及解析
-
下列化学用语表述正确的是
A.S2-的结构示意图:
B.氮原子的轨道表示式:
C.CO2的比例模型:
D.氨气分子的结构式:
难度: 中等查看答案及解析
-
下列化工生产涉及的变化主要是物理变化的是( )
A.煤的干馏 B.石油的分馏
C.石油的裂化 D.石油的裂解
难度: 中等查看答案及解析
-
关于晶体的叙述中,正确的是( )
A.原子晶体中,共价键的键能越大,熔、沸点越高
B.分子晶体中,分子间的作用力越大,该分子越稳定
C.分子晶体中,共价键的键能越大,熔、沸点越高
D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体
难度: 简单查看答案及解析
-
下列分子中,属于含有极性键的非极性分子的是
A.PCl3 B.H2S C.P4 D.C2H4
难度: 中等查看答案及解析
-
下列变化需克服共价键的是
A.金刚石熔化 B.汞受热变成汞蒸气 C.蔗糖溶于水 D.食盐溶于水
难度: 简单查看答案及解析
-
在密闭容器中,反应
达到平衡后,若将容器体积缩小一半,对反应产生的影响是
A.
减小,
增大 B.
增大,
减小
C.
、
都减小 D.
、
都增大
难度: 简单查看答案及解析
-
布洛芬片常用来减轻感冒症状,其结构简式如图,下列有关说法错误的是( )

A.布洛芬的分子式为C13H18O2
B.布洛芬与苯乙酸是同系物
C.1mol 布洛芬最多能与3mol 氢气发生加成反应
D.布洛芬在苯环上发生取代反应,其一氯代物有4种
难度: 中等查看答案及解析
-
配制一定物质的量浓度的
溶液时,下列因素会导致溶液浓度偏高的是
A.溶解时有少量液体溅出 B.洗涤液未全部转移到容量瓶中
C.容量瓶使用前未干燥 D.定容时液面未到刻度线
难度: 中等查看答案及解析
-
下列离子在溶液中能大量共存的是( )
A.H+、AlO2-、CO32- B.K+、Ba2+、SO42-
C.NH4+、OH-、NO3- D.Fe3+、NO3-、Cl-
难度: 中等查看答案及解析
-
下列有关元素的性质及其递变规律正确的是
A.Ⅰ A族与ⅦA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,正价从+1递增到+7
C.同主族元素的简单阴离子还原性越强,水解程度越大
D.同周期金属元素的化合价越高,其原子失电子能力越强
难度: 中等查看答案及解析
-
下列化学用语所表示的微粒,对水的电离平衡没有影响的是
A.
B.
C.1s22s22p63s1 D.
难度: 中等查看答案及解析
-
一定条件下,在体积为10L的密闭容器中,1molA和1molB进行反应:2A(g)+B(g)
2C(g),达到平衡时生成0.6molC。下列说法正确的是( )
A.当容器内密度保持不变时,可以判断反应已达到平衡
B.其他条件不变,将容器体积变为5L,C的平衡浓度变为原来的2倍
C.达到平衡时,C的体积百分含量为0.353
D.其他条件不变,若增大压强,则物质A的转化率减小
难度: 中等查看答案及解析
-
工业上常用NaHSO3处理含Cr2O72-的废液,反应的离子方程式为:5H++Cr2O72-+3HSO3-→2Cr3++3SO42-+4H2O下列判断错误的是( )
A.氧化产物是SO42- B.氧化剂与还原剂的物质的量之比是1:3
C.Cr2O72-表现了氧化性 D.还原1molCr2O72-,电子转移3mol
难度: 困难查看答案及解析

 合成
合成 的合成路线________。
的合成路线________。 )
)