-
下列物质在水溶液中的电离方程式错误的是( )
A.NaHCO3=Na++H+ +CO32- B.NaHSO4=Na+ +H+ +SO42-
C.MgCl2=Mg2++2Cl- D.Ba(OH)2=Ba2+ +2OH-
难度: 中等查看答案及解析
-
下列实验操作的描述中,正确的是( )
A.从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶
B.用稀盐酸洗涤盛放过石灰水的试剂瓶
C.酒精灯不慎碰倒起火时可用水扑灭
D.各放一张质量相同的滤纸于天平的托盘上,将NaOH固体放在左盘纸上称量
难度: 简单查看答案及解析
-
下列实验操作中正确的是( )
A.蒸馏时温度计插入蒸馏烧瓶的混合液中
B.进行分液操作时,先取下分液漏斗上口的玻璃塞,然后再慢慢旋开活塞
C.分液操作时下层液体从分液漏斗下口放出,上层液体从下口放出到另外一个烧杯中
D.蒸发操作时,应使混合物的水分完全蒸干后,才能停止加热
难度: 简单查看答案及解析
-
对于易燃、易爆、有毒的化学物质,往往会在其包装上面贴上危险警告标签。下列所列物质,贴错了包装标签的是( )

A.A B.B C.C D.D
难度: 简单查看答案及解析
-
朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差斑驳的黑影……”月光穿过薄雾所形成的种种美景的本质原因是( )
A.空气中的小水滴颗粒大小约为
B.月光是一种胶体
C.雾是一种胶体
D.发生丁达尔效应
难度: 中等查看答案及解析
-
下列事实与胶体性质无关的是 ( )
A. 水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
B. 将植物油倒入水中用力搅拌形成油水混合物
C. 一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路
D. 氢氧化铁胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解
难度: 中等查看答案及解析
-
下列说法正确的是(NA表示阿伏伽德罗常数)( )
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.在常温常压下,1molHe含有的原子数目为NA
C.71gCl2所含分子数为2NA
D.在同温同压下,相同体积的任何气体单质所含原子数相同
难度: 简单查看答案及解析
-
下列溶液中Cl-的浓度与50mL1mol·L-1AlCl3溶液中Cl-的物质的量浓度相等的是( )
A.150mL3mol/LKCl溶液 B.75mL0.5mol/LMgCl2溶液
C.100mL1mol/LNaCl溶液 D.25mL2mol/LAlCl3溶液
难度: 简单查看答案及解析
-
由K2SO4、Al2(SO4)3、KAl(SO4)2形成的混合溶液,其中Al3+的物质的量浓度为0.4 mol·L-1,SO42-的物质的量浓度为0.7 mol·L-1,则此溶液中K+的物质的量浓度(mol·L-1)为
A.0.1 B.0.15 C.0.2 D.0.25
难度: 中等查看答案及解析
-
冬季的降雪给交通带来了诸多不便,其中醋酸钾(CH3COOK)是融雪效果最好的融雪剂,下列关于醋酸钾或醋酸的说法正确的是( )
A.1molCH3COOK的质量为98g/mol
B.CH3COOH摩尔质量就是它的相对分子质量
C.一个CH3COOH的质量约为
g
D.含有6.02×1023个碳原子的CH3COOK的物质的量是1mol
难度: 简单查看答案及解析
-
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是
A.Na+、K+、OH-、Cl- B.Na+、Cu2+、SO42-、NO3-
C.Ba2+、HCO3-、NO3-、K+ D.Mg2+、Na+、SO42-、Cl-
难度: 简单查看答案及解析
-
一系列物质: NaCl、 Cl2、 NaClO、 Cl2O5、 HClO4是按某一规律排列的,下列组合中也完全照此规律排列的是( )
A.Na2CO3、C、CO2、CO、NaHCO3
B.Na2S、S、SO2、Na2SO3、Na2SO4
C.NH4Cl、N2、NaNO2、NO2、HNO3
D.P2O5、H3PO4、Na3PO4、Na2HPO4、NaH2PO4
难度: 中等查看答案及解析
-
利用下列实验装置完成相应的实验,能达到实验目的的是( )
A.浓硫酸稀释
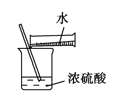
B.除去酒精中溶有的少量水
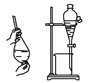
C.实验室中制取少量蒸馏水
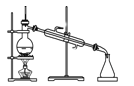
D.制备并检验氢气的可燃性
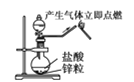
难度: 简单查看答案及解析
-
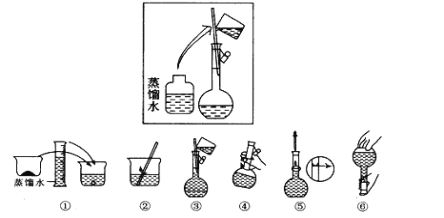
化学实验的基本操作是完成化学实验的关键,下列实验操作正确的是( )
①用50 mL量筒量取5.2 mL稀硫酸
②用分液漏斗分离苯和四氯化碳的混合物
③用托盘天平称量117.7 g氯化钠晶体
④用量筒量取23.10 mL溴水
⑤用蒸发皿高温灼烧石灰石
⑥用250 mL容量瓶配制250 mL 0.2 mol·L-1的NaOH溶液;
A.③⑥ B.②③④⑤ C.①②④ D.②⑤⑥
难度: 中等查看答案及解析
-
从下列混合物中分离出其中一成分,所采取的分离方法正确的是( )
A.由于碘在酒精中溶解度大,所以可用酒精把碘水中的碘萃取出来
B.水的沸点为100℃,酒精的沸点为78.5℃,所以用加热蒸馏的方法使含水的酒精变为无水酒精
C.由于汽油和水不相溶,因此可用分液的方法分离二者的混合物
D.NaCl的溶解度随温度下降而减少,所以用冷却法从热的含少量KNO3的NaCl浓溶液中分离,得到纯净的NaCl
难度: 简单查看答案及解析
-
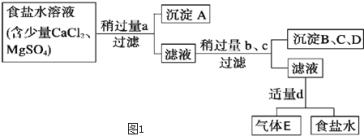
为确定某溶液的离子组成进行如下实验:
①取少量溶液滴加BaCl2溶液,产生白色沉淀
②然后继续加入稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的气体,白色沉淀部分溶解
③取上层清液继续滴加Ba(NO3)2溶液至再无沉淀生成时,再滴加AgNO3溶液,产生白色沉淀
根据实验,以下推测不正确的是( )
A.一定有SO42- B.一定有CO32-
C.不能确定Cl-是否存在 D.不能确定SO42-是否存在
难度: 中等查看答案及解析
-
下列针对物质的叙述正确的是( )
选项
物质
叙述
判断
A
1molH2O
标况下,其体积约为22.4L
正确
B
2gH2
常温常压下,有NA个氢气分子
错误
C
1L0.1mol/LNaCl溶液
取出100mL,NaCl的物质的量浓度为0.1mol/L
正确
D
1mol/LNa2SO4
将1molNa2SO4固体溶于1L水中可配的溶液
正确
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
等体积NaCl,MgCl2,AlCl3三种溶液分别于等体积等物质的量浓度的AgNO3溶液恰好完全反应,则NaCl,MgCl2,AlCl3三种溶液的物质的量浓度之比为( )
A.1:2:3 B.3:2:1 C.6:3:2 D.1:1:1
难度: 简单查看答案及解析
-
在两个密闭容器中,分别充有质量相等的甲乙两种气体。若两容器的温度和压强均相等,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多 B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小 D.甲的相对分子质量比乙的相对分子质量小
难度: 简单查看答案及解析
-
三种气体X、Y、Z的相对分子质量关系为Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是( )
A.原子数相等的三种气体,质量最大是Z
B.若一定条件下,三种气体体积均为2.24L,则他们的物质的量一定均为0.1mol
C.同温同压下,同质量的三种气体,气体密度最小的是X
D.同温下,体积相同的两容器分别充2gY气体和1gZ气体,则压强比为2:1
难度: 中等查看答案及解析
-
把VL含有MgSO4、K2SO4的混合溶液分为两等份,一份加入amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含有bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡,则原混合溶液中钾离子的浓度为( )
A.
mol/L B.
mol/L C.
mol/L D.
mol/L
难度: 简单查看答案及解析
-
下列离子方程式,书写正确的是( )
A.盐酸和碳酸钡反应CO32-+2H+=CO2↑+H2O
B.硫酸铜溶液中滴加氢氧化钡溶液Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓
C.硝酸银溶液中加入铜粉Ag++Cu=Cu2++Ag↓
D.铁与稀盐酸反应2Fe+6H+=2Fe3++3H2↑
难度: 简单查看答案及解析
-
为除去某物质中所含的杂质,周佳敏同学做了以下四组实验,其中她所选用的试剂或操作方法正确的是( )
序号
物质
杂质
除杂试剂或操作方法
①
NaCl溶液
Na2CO3
加入盐酸,蒸发
②
FeSO4溶液
CuSO4
加入过量铁粉并过滤
③
H2
CO2
依次通过盛有NaOH溶液和浓硫酸的洗气瓶
④
NaNO3
CaCO3
加稀盐酸溶解、过滤、蒸发、结晶
A.①②③ B.②③④ C.①③④ D.①②③④
难度: 中等查看答案及解析