-
下列试剂能使pH试纸变红色的是
A. 久置氯水 B. 氢氧化钠溶液 C. 浓硫酸 D. 次氯酸钠溶液
难度: 简单查看答案及解析
-
下列说法正确的是 ( )
A.硅材料广泛应用于光纤通讯 B.工艺师利用盐酸刻蚀石英制作艺术品
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 D.粗硅制备单晶硅不涉及氧化还原反应
难度: 简单查看答案及解析
-
下列属于碱性氧化物的是
A.NH3·H2O B.MgO
C.K2FeO4 D.SO3
难度: 简单查看答案及解析
-
分离CCl4和水一定不需要选用的仪器是
A.
B.

C.
D.

难度: 简单查看答案及解析
-
下列物质属于电解质且能导电的是
A.金属铜 B.液态HCl
C.酒精 D.熔融KNO3
难度: 简单查看答案及解析
-
下列说法正确的是
A.花生油的主要成分是高级脂肪酸甘油酯,属于高分子化合物
B.只有不同种类的氨基酸之间才能形成多肽
C.向鸡蛋清的溶液中加入饱和硫酸钠溶液产生沉淀,加水后沉淀可溶解
D.向淀粉溶液中加入硫酸溶液,加热后滴入几滴氢氧化铜悬浊液,再加热至沸腾,未出现红色物质,说明淀粉未水解
难度: 中等查看答案及解析
-
下列表示正确的是( )
A.离子结构示意图:
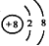 可以表示16O2-,也可以表示18O2-
可以表示16O2-,也可以表示18O2-B.比例模型
表示CH4分子或CCl4分子
C.乙烯的结构简式:CH2CH2
D.硅的分子式:Si
难度: 简单查看答案及解析
-
下列说法正确的是
A. 检验(NH4)2Fe(SO4)2·12H2O晶体中的NH4+:取少量晶体溶于水,加入足量浓NaOH溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体
B. 验证FeCl3与KI反应的限度:可将少量的FeCl3溶液与过量的KI溶液混合,充分反应后用CCl4萃取,静置,再滴加KSCN溶液
C. 受溴腐蚀至伤时,先用稀NaOH溶液洗,再用水洗
D. 用激光笔检验硫酸铜溶液具有丁达尔效应
难度: 中等查看答案及解析
-
下列说法正确的是
A.寻找更多化石燃料,利用燃烧放热,使水分解产生氢气
B.沼气和天然气的主要成分为甲烷,两者均属于可再生能源
C.绿色化学的核心是对环境污物进行无害化处理
D.乙醇可以直接作为燃料,也可以和汽油混合后作为发动机燃料
难度: 简单查看答案及解析
-
一定条件下,物质的量均为0.3mol的X(g)与Y(g)在容积固定的密闭容器中发生反应:X(g)+3Y(g)
2Z(g),ΔH=-akJ·mol-1,下列说法正确的是( )
A.反应一段时间后,X与Y的物质的量之比仍为1:1
B.达到平衡时,反应放出0.1akJ的热量
C.达到平衡后,向平衡体系中充入稀有气体,正反应速率不发生变化
D.X的体积分数保持不变,说明反应已达到平衡
难度: 中等查看答案及解析
-
如图为一重要的烃的衍生物,以下关于它的说法中不正确的是( )
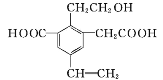
A.1mol该物质,最多可以和4molH2发生加成反应
B.1mol该物质消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
C.可以用酸性高锰酸钾溶液检验其中的碳碳双键
D.该物质能够在催化剂作用下被氧化为醛
难度: 中等查看答案及解析
-
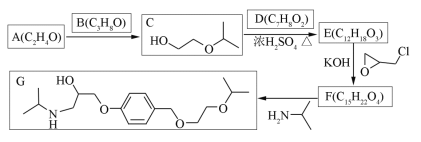
某有机物X的结构简式如图所示,则下列有关说法中正确的是( )
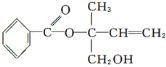
A.X的分子式为C12H16O3
B.X在一定条件下能发生加成、加聚、取代、消去等反应
C.在Ni作催化剂的条件下,1molX最多只能与1molH2加成
D.可用酸性高锰酸钾溶液区分苯和X
难度: 简单查看答案及解析
-
关于羟基和氢氧根的说法中不正确的是( )
A.两者不相同 B.羟基比氢氧根少一个电子
C.两者的组成元素相同 D.羟基比氢氧根稳定
难度: 简单查看答案及解析
-
下列物质仅用溴水即可鉴别的是( )
A. 苯、己烷、己烯 B. 己烷、己烯、己炔
C. 苯、四氯化碳、苯乙烯 D. 溴苯、四氯化碳、己烯
难度: 中等查看答案及解析
-
主链上有4个碳的某烷烃有两种同分异构体,则与该烷烃等碳且主链上四个碳的烯烃的同分异构体有几种( )
A.3 B.4 C.5 D.6
难度: 中等查看答案及解析
-
四种短周期主族元素 X、Y、Z、W 的相对位置如表,元素 X 的原子核外电子数是 Z的 2 倍。下列说法不正确的是
A.W 元素的简单气态氢化物的热稳定性比 Z 元素的简 单气态氢化物的高
B.气体分子(ZW)2 的结构式为 N≡C—C≡N
C.X、Y、W 三种元素的简单离子半径最大的是 Y
D.元素 X 位于周期表中第三周期、第ⅡA族,其单质制备可用电解熔融 XCl2 的方法。
难度: 中等查看答案及解析
-
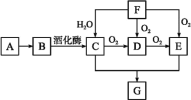
用原电池原理可以处理硫酸工业产生的SO2尾气。现将SO2 通入如图装置(电极均为惰性材料) 进行实验。下列说法不正确的是
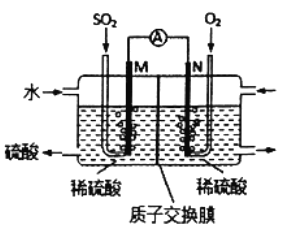
A.M极为负极,电极上发生氧化反应
B.溶液中H+移向N区,SO42-移向M区
C.N极发生的电极反应为O2+4H++4e-=2H2O
D.相同条件下,M、N两极上消耗的气体体积之比为2:1
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.在光照条件下,甲苯能与Cl2发生取代反应
B.乙炔和乙烯都能使溴水褪色,其褪色原理相同
C.总质量一定的甲苯和甘油混合物完全燃烧时生成水的质量一定
D.对二氯苯只有一种结构,说明苯环结构中不存在单双建交替的结构
难度: 中等查看答案及解析
-
下列说法不正确的是
A.1L浓度为0.1mol/L的NH4Cl溶液阳离子数目多于氯离子数目
B.比较浓度均为0.1mol·L-1的HI和醋酸溶液的导电能力可判断HI为强酸
C.常温下,pH=3的醋酸溶液水加稀释1000倍后溶液的pH<6
D.常温下,同体积的pH=9的NaClO溶液和pH=5的NH4Cl溶液水电离的OH-数相同
难度: 中等查看答案及解析
-
根据如下能量关系示意图,下列说法正确的是( )
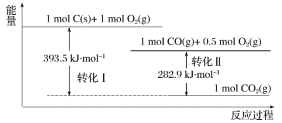
A.1molC(g)与1molO2(g)的能量之和为393.5kJ
B.反应2CO(g)+O2(g)=2CO2(g)中,生成物的总能量大于反应物的总能量
C.由C→CO的热化学方程式为:2C(s)+O2(g)=2CO(g) ΔH=-221.2kJ·mol-1
D.热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH=-10.1 kJ·mol-1
难度: 中等查看答案及解析
-
下列离子方程式书写中,正确的是( )
A.氯化铁溶液吸收H2S:S2-+2Fe3+=2Fe2++S↓
B.用氢氧化钠溶液吸收氯气:Cl2+2OH-=ClO-+Cl-+H2O
C.将少量SO2通入NaClO溶液:SO2+H2O+2ClO-=SO32-+2HClO
D.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.分子式满足C6H12的有机物所有碳原子可能位于同一平面上
B.1mol乙烷在光照条件下最多能与3molCl2发生取代反应
C.甲烷、苯和油脂均不能使酸性KMnO4溶液褪色
D.分子式为C4H10O且能与金属钠反应的有机物有3种
难度: 中等查看答案及解析
-
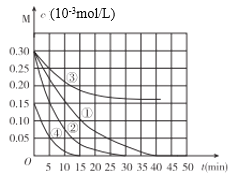
用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果.设计如下对比实验探究温度、浓度、pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示,下列说法不正确的是( )
实验编号
温度°C
pH
①
25
1
②
45
1
③
25
7
④
25
1
A.实验①在15min内M的降解速率为1.33×10-5mol/(L·min)
B.若其他条件相同,实验①②说明升高温度,M降解速率增大
C.若其他条件相同,实验①③证明pH越高,越不利于M的降解
D.实验①④说明M的浓度越小,降解的速率越快
难度: 中等查看答案及解析
-
将一定量的氯气通入
的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、
共存体系(不考虑氯气和水的反应)。下列说法正确的是
A.若反应中转移的电子为n mol,则
B.溶液中
可能为
C.与NaOH反应的氯气物质的量:
D.当溶液中
时,反应的离子方程式为:
难度: 中等查看答案及解析
-
下列混合物总物质的量一定时,组内各物质按任意比混合,完全燃烧时消耗O2的物质的量不变的是( )
A.甲烷、甲醇、甲醛 B.乙炔、苯、1,3-丁二烯
C.丙烯、2-丁烯、环已烷 D.乙醇、乙烯、丙烯酸(CH2=CH-COOH)
难度: 中等查看答案及解析