-
下列说法正确的是( )
A.乙烯的分子式可写成(CH2)2
B.乙烯的结构简式为CH—CH
C.乙烯与HCl反应生成CH3CH2Cl
D.乙烯的结构简式为CH2CH2
难度: 简单查看答案及解析
-
太原市自2016年11月1日零时起,将汽车用油全部更换为”国V标准”车用燃料,进而 改善太原市空气质量。下列物质中,不会造成空气污染的是

A. NO B. SO2 C. CO2 D. 粉尘
难度: 简单查看答案及解析
-
从南方往北方长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液的氧化性,催熟水果
D.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
难度: 中等查看答案及解析
-
下列陈述Ⅰ,Ⅱ正确并且有因果关系的是( )
选项
陈述Ⅰ
陈述Ⅱ
A
SO2有漂白性
SO2可使溴水褪色
B
SiO2有导电性
SiO2可用于制备光导纤维
C
浓硫酸有氧化性
浓硫酸可用于干燥H2和CO
D
Fe3+有氧化性
Fe3+溶液可用于回收废旧电路板中的铜
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
如图是课外活动小组的同学设计的4个喷泉实验方案。下列有关操作不可能引发喷泉现象的是( )
A.挤压装置①的胶头滴管使CCl4全部进入烧瓶,片刻后打开止水夹
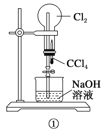
B.挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹
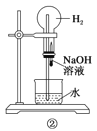
C.用鼓气装置从装置③的a处不断鼓入空气并打开止水夹

D.向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹

难度: 简单查看答案及解析
-
下列指定反应的离子方程式正确的是
A.SO2通入Ba(OH)2溶液中出现白色沉淀,因为Ba2++SO2+2OH-=BaSO4↓+2H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe
2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O
Al(OH)3↓+3
D.向Na2CO3溶液中滴加稀盐酸:Na2CO3+2H+
H2CO3+2Na+
难度: 简单查看答案及解析
-
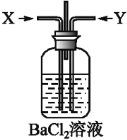
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100mL甲气体依次通过下图实验的处理,结果得到酸性溶液,几乎无气体剩余,则甲气体的组成为
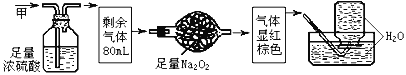
A.NH3、NO2、N2 B.NH3、NO、CO2
C.NH3、NO2、CO2 D.NO、CO2、N2
难度: 中等查看答案及解析
-
我国具有独立知识产权的电脑芯片“龙芯一号”的问世,填补了我国计算机制造史上的一项空白.下列对晶体硅的有关叙述正确的是( )
A.晶体硅和金刚石的物理性质相似
B.硅在地壳中含量居第二位,可以以游离态存在于自然界中
C.晶体硅是一种良好的半导体材料,但是它提炼工艺复杂,价格昂贵
D.晶体硅具有金属光泽,故它属于金属材料,可以导电
难度: 中等查看答案及解析
-
如图所示,有关化学反应和能量变化的说法正确的是( )
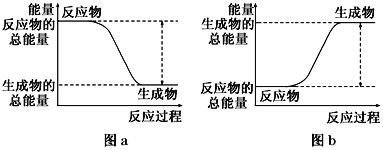
A. 图a表示的是吸热反应的能量变化
B. 图b中反应物比生成物稳定
C. 图a可以表示氯化铵固体与氢氧化钡晶体反应的能量变化
D. 图a不需要加热就能发生,图b一定需要加热才能发生
难度: 中等查看答案及解析
-
下列烧杯中盛放的都是稀硫酸,在铜电极上能产生大量气泡的是
A.
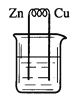 B.
B. 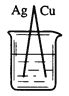 C.
C.  D.
D. 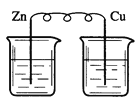
难度: 简单查看答案及解析
-
下列反应属于取代反应的是
A.CH4
C+2H2
B.2HI+Cl2====2HCl+I2
C.CH4+2O2
CO2+2H2O
D.CH4+Cl2
CH3Cl+HCl
难度: 中等查看答案及解析
-
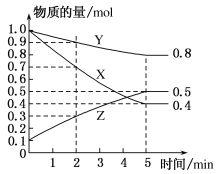
已知汽车尾气无害化处理反应为
。
下列说法不正确的是 ( )
A.升高温度可使该反应的逆反应速率降低 B.使用高效催化剂可有效提高正反应速率 C.反应达到平衡后,N0的反应速率保持恒定 D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
难度: 中等查看答案及解析
-
下列有关烷烃的叙述中,正确的是
①在烷烃分子中,所有的化学键都是单键
②烷烃中除甲烷外,很多都能使酸性KMnO4溶液的紫色褪去
③分子通式为CnH2n+2的烃不一定是烷烃
④所有的烷烃在光照条件下都能与氯气发生取代反应
⑤光照条件下,乙烷通入溴水中,可使溴水褪色
A.①③⑤ B.②③ C.①④ D.①②④
难度: 简单查看答案及解析
-
可以充分说明可逆反应P(g)+Q(g)
R(g)+S(g)在恒温条件下达到平衡状态的事实是
A.反应器内的压强不随时间的变化而变化
B.反应器内P、Q、R、S四种气体共存
C.生成P的速率与生成S的速率相等
D.生成1molP必有1molQ生成
难度: 简单查看答案及解析
-
向容积为2L的密闭容器中充入2molA气体和1mol B气体,在一定条件下发生如下反应:2A(g)+B(g)
3C(g);经2s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是( )
①用物质A表示该反应的平均速率为0.2 mol·L-1·s-1
②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2 mol·L-1
A. ①②③ B. ①③ C. ②④ D. ①④
难度: 中等查看答案及解析
-
下列说法中正确的一组是( )
A.H2和D2互为同位素
B.
和
是同一种物质
C.正丁烷和异丁烷是同系物
D.
和
互为同分异构体
难度: 简单查看答案及解析