-
下列物质不互为同分异构体的是( )
A. 葡萄糖和果糖 B. 蔗糖和麦芽糖 C. 正丁烷和异丁烷 D. 淀粉和纤维素
难度: 中等查看答案及解析
-
2019年12月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。以下是人们在面对“新型冠状病毒肺炎”时的一些认识,你认为符合科学道理的是
A.家庭消毒时,消毒液越浓越好
B.吸烟、喝酒可以预防“新型冠状病毒”
C.应经常保持室内清洁卫生和通风
D.必须每天吃药,补充人体所需化学物质
难度: 简单查看答案及解析
-
2015年长庆油田油气产量当量为5480万吨,自2014年后再次成为中国产量最大的油田。下列关于石油的说法正确的是
A.石油属于可再生矿物能源
B.石油主要含有碳、氢两种元素
C.石油的裂化是物理变化
D.石油分馏的各馏分均是纯净物
难度: 简单查看答案及解析
-
在下列自然资源的开发利用中,不涉及化学变化的是
①石油的分馏;②煤的干馏;③用石油裂解生产乙烯;④用铝热反应焊接钢轨;⑤用乙烯制取聚乙烯;⑥用铁矿石冶炼铁;⑦用煤生产水煤气;⑧海水蒸馏法制取淡水
A.①②③④ B.①②⑤⑦ C.①⑧ D.①②⑥
难度: 简单查看答案及解析
-
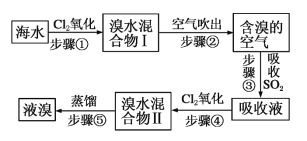
下列不能作为海水淡化方法的是
A.蒸馏法 B.电渗析法 C.离子交换法 D.过滤法
难度: 简单查看答案及解析
-
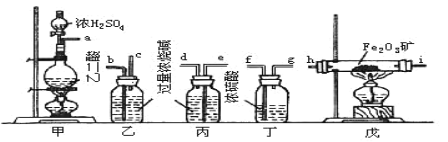
下列化学反应在冶金工业中没有得到广泛应用的是 ( )
A. MgCl2(熔融)
Mg+Cl2↑ B. Al2O3+3C
2Al+3CO ↑
C. Fe2O3 +3CO
2Fe +3CO2↑ D. 2Ag2O
4Ag+O2↑
难度: 简单查看答案及解析
-
“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合绿色化学概念的是
A.乙烯聚合为聚乙烯高分子材料 B.甲烷与氯气制备一氯甲烷
C.以铜和浓硝酸为原料生产硝酸铜 D.用二氧化硅制备高纯硅
难度: 中等查看答案及解析
-
下列说法中正确的是
A.石油干馏可得到汽油、煤油等
B.开发太阳能等新能源,推广甲醇汽油,使用无磷洗涤剂都可直接降低碳排放
C.煤干馏可以得到甲烷、苯和氨等重要化工原料
D.石油分馏可获得乙烯、丙烯和丁二烯
难度: 简单查看答案及解析
-
下列混合物能用分液法分离的是
A.乙醇与乙酸 B.苯和溴苯
C.乙酸乙酯和Na2CO3溶液 D.苯和四氯化碳
难度: 简单查看答案及解析
-
乙醇分子结构中各种化学键如图所示,
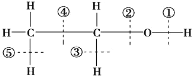 ,下列说法正确的是
,下列说法正确的是A.与金属钠反应时断裂② B.与乙酸反应时断裂①
C.在铜丝催化下与O2反应断裂②③ D.燃烧时断裂①③
难度: 简单查看答案及解析
-
提纯下列物质(括号中为少量杂质),选择试剂和分离方法都正确的是
被提纯的物质
除杂试剂
分离方法
A
甲烷(乙烯)
酸性高锰酸钾溶液
洗气
B
苯(碘)
水
过滤
C
乙酸乙酯(乙醇)
饱和碳酸钠溶液
过滤
D
乙醇(H2O)
生石灰
蒸馏
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有
A.4种 B.3种 C.2种 D.1种
难度: 简单查看答案及解析
-
设NA代表阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,22.4L乙烷和乙烯含碳原子数为2NA
B.室温下,42.0g乙烯含C—H键为3NA
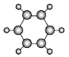
C.标准状况下,22.4L苯所含的分子数为NA
D.标准状况下,2.24L甲烷和乙烯混合气体中含氢原子数为0.4NA
难度: 简单查看答案及解析
-
下列反应不属于取代反应的是( )
A.CH3CH2OH+HBr→CH3CH2Br+H2O
B.2CH3CH2OH
CH3CH2OCH2CH3+H2O
C.CH2=CH2+H2O
CH3CH2OH
D.

难度: 简单查看答案及解析
-
下列化学用语中,书写或说法正确的是
A.乙烯的结构简式:CH2CH2
B.乙醇含有的官能团是—OH,带一个单位负电荷
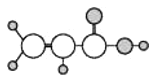
C.丙烷的球棍模型为
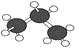
D.乙酸的分子式:C2H4O
难度: 中等查看答案及解析
-
某有机物的结构为
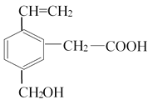 ,这种有机物不可能具有的性质是( )
,这种有机物不可能具有的性质是( )A. 能跟NaOH溶液反应 B. 能使酸性KMnO4溶液褪色
C. 能发生酯化反应 D. 能发生水解反应
难度: 中等查看答案及解析
-
下列反应前后物质的总能量变化能用图表示的是
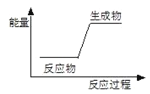
A.氢氧化钠和盐酸的反应
B.Ba(OH)2·8H2O晶体和NH4Cl晶体的反应
C.铝与NaOH溶液的反应
D.甲烷在氧气中燃烧
难度: 简单查看答案及解析
-
下列各组金属与酸的反应,反应刚开始时,放出H2的速率最大的是
金属(粉末状)/mol
酸的浓度及体积
反应温度
A
Mg
0.1
3mol·L-1盐酸
10mL
25℃
B
Fe
0.1
3mol·L-1盐酸
10mL
25℃
C
Mg
0.1
3mol·L-1盐酸
10mL
35℃
D
Mg
0.1
6mol·L-1硝酸
10mL
60℃
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
将4molA气体和2molB气体置于1L的密闭容器中,混合后发生如下反应:
。若经2s后测得C的浓度为1.2mol/L,则下列说法正确的是( )
A.用物质A表示的反应速率为
B.用物质B表示的反应速率为
C.2s内物质A的转化率为30%
D.2s时物质B的浓度为0.6mol/L
难度: 中等查看答案及解析
-
下列关于SO2的说法正确的是( )
A.SO2气体通入滴有酚酞的NaOH溶液中,红色褪去,说明SO2具有漂白性
B.SO2和Cl2混合通入品红溶液中,一定能使红色褪色
C.SO2气体通入溴水中,溴水的颜色褪去,说明SO2具有漂白性
D.二氧化硫的排放会导致酸雨的产生
难度: 中等查看答案及解析
 ;③能与水在一定条件下反应生成C
;③能与水在一定条件下反应生成C