-
X元素最高价氧化物对应的水化物为HXO3,它的气态氢化物为( )
A. HX B. H2X C. XH3 D. XH4
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.可加热NH4NO3晶体制备氨气
B.可以用湿润的红色石蕊试纸检验氨气
C.将蘸有浓氨水和浓硫酸的玻璃棒靠近,观察到白烟
D.除去碘中混有的少量氯化铵,可采用升华的方法
难度: 简单查看答案及解析
-
下列化学用语使用正确的是( )
A.次氯酸的结构式:H—Cl—O
B.氮气的电子式:NN
C.甲烷分子的比例模型为
D.乙烯的结构简式:CH2CH2
难度: 简单查看答案及解析
-
用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
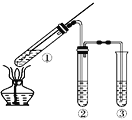
A.抽动①中铜丝可控制SO2的量
B.②中选用品红溶液验证SO2的生成
C.③中选用NaOH溶液吸收多余的SO2
D.为确认CuSO4生成,向①中加水,观察颜色
难度: 简单查看答案及解析
-
俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子,结果4次成功合成4个第115号元素的原子。这4个原子生成数微秒后衰变成第113号元素。下列有关叙述正确的是( )
A.113号元素在第七周期ⅢA族
B.镅元素和115号元素不在同一周期
C.115号和113号元素都是非金属元素
D.115号元素衰变成113号元素属于化学变化
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.Li通常保存在煤油中,以隔绝空气
B.碱金属阳离子,氧化性最强的是Li+
C.卤素单质与水反应均可用X2+H2O
HXO+HX表示
D.从Li到Cs,碱金属的密度越来越大,熔、沸点越来越高
难度: 简单查看答案及解析
-
关于氢键,下列说法不正确的是( )
A.NH3的稳定性很强,是因为其分子间能形成氢键
B.水在结冰时体积膨胀,是由于水分子之间存在氢键
C.HF的沸点比HCl的沸点高是由于HF分子间存在氢键所致
D.在氨水中水分子和氨分子之间也存在着氢键
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.CHCl3只有一种结构,说明甲烷是以碳原子为中心的正四面体结构
B.1mol甲烷生成CCl4最多消耗2mol氯气
C.标准状况下,11.2LCCl4中含有C—Cl键的数目为2NA
D.在点燃甲烷气体之前必须检验其纯度
难度: 简单查看答案及解析
-
下列各组物质性质比较的表示中,正确的是( )
A.还原性:F->Cl->Br->I-
B.稳定性:HCl>H2S>PH3
C.碱性:NaOH>KOH>Ca(OH)2>Mg(OH)2
D.酸性:H3PO4>H2SO4>HC1O4
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.烃
的分子式为C3H6,符合通式CnH2n,故该分子属于烯烃
B.可用酸性高锰酸钾溶液来除去甲烷中混有的少量乙烯
C.正戊烷分子中所有的碳原子均在同一条直线上
D.丁烷的一氯代物有4种
难度: 简单查看答案及解析
-
由乙烯推测丙烯的结构或性质,正确的是( )
A.分子中3个碳原子在同一直线上
B.分子中所有原子都在同一平面上
C.分子中共价键的夹角均为120°
D.分子中共价键数为8,其中有一个碳碳双键
难度: 中等查看答案及解析
-
几种短周期元素的原子半径及主要化合价如下表:
元素代号
X
Y
Z
W
原子半径/pm
160
143
70
66
主要化合价
+2
+3
+5、+3、-3
-2
下列叙述正确的是( )
A.X、Y元素的金属性X<Y
B.Y的最高价氧化物的水化物能溶于稀氨水
C.一定条件下,W单质可以将Z单质从其氢化物中置换出来
D.一定条件下,Z单质与W的常见单质直接生成ZW2
难度: 简单查看答案及解析
-
短周期主族元素X和Y形成能够离子化合物XY2。且该离子化合物中阴、阳离子具有相同的电子层结构。下列说法不正确的是( )
A.离子半径:X2+<Y-
B.原子序数:X<Y
C.该化合物中只存在离子键
D.原子最外层电子数X<Y
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.H2和D2互为同位素
B.CH2=CH2和CH2=CH-CH=CH2互为同系物
C.
和
互为同分异构体
D.
和
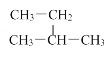 是同一种物质
是同一种物质难度: 简单查看答案及解析
-
下列说法不正确的是
①共价化合物中含共价键,也可能含离子键
②因为H2CO3酸性<H2SO3酸性,所以非金属性C<S
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤熔融状态能导电的物质是离子化合物
⑥由分子组成的化合物中一定存在共价键
A.①③⑤ B.②④⑥
C.①②④⑤ D.①③⑤⑥
难度: 简单查看答案及解析
-
下列各表为元素周期表中的一部分,表中数字为原子序数,其中M的原子序数为37的是( )
A.
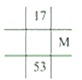 B.
B.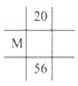 C.
C.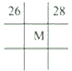 D.
D.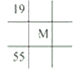
难度: 简单查看答案及解析
-
将碳与浓硫酸共热产生的气体X和铜与浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中,下列有关说法正确的是( )
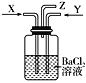
A.在Z导管口有红棕色气体生成
B.从Z导管中逸出的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.洗气瓶中产生的沉淀是碳酸钡
难度: 简单查看答案及解析
-
已知R2+核内共有N个中子,R的质量数为A,则mgR2+中含有电子的物质的量为( )
A.
mol B.
mol
C.
mol D.
mol
难度: 简单查看答案及解析