-
中华民族有着灿烂光辉的发明史,下列发明创造不涉及化学反应的是( )
A.
 用胆矾炼铜 B.
用胆矾炼铜 B.  用铁矿石炼铁
用铁矿石炼铁C.
 烧结粘土制陶瓷 D.
烧结粘土制陶瓷 D.  打磨磁石制指南针
打磨磁石制指南针难度: 简单查看答案及解析
-
有句谚语“每天一个苹果,医生远离我”,苹果主要能为人体提供的营养素是( )
A. 油脂 B. 无机盐 C. 维生素 D. 蛋白质
难度: 简单查看答案及解析
-
LiFePO4新型锂离子电池以其独特的优势成为绿色能源的新宠,已知钾的化合价为+1价,P的化合价为+5,则LiFePO4中Fe的化合价是( )
A.+2 B.0 C.+3 D.+6
难度: 中等查看答案及解析
-
下列实验操作中,正确的是( )

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
古语道:“人要实,火要虚”.此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺.从燃烧的条件看,“火要虚”的实质是
A. 增大可燃物的热值 B. 提高空气中氧气的含量
C. 提高可燃物的着火点 D. 增大可燃物与空气的接触面积
难度: 中等查看答案及解析
-
如图所示:甲瓶中盛放的是浓H2SO4,乙瓶中放的是用石蕊溶液染成紫色的干燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花不变色;若关闭阀门Ⅱ,打开阀门Ⅰ,紫色小花()
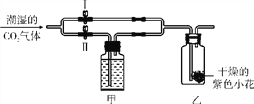
A. 变红色 B. 变蓝色 C. 变白色 D. 不变色
难度: 中等查看答案及解析
-
为除去下表物质中杂质(括号内为杂质),所选试剂及操作方法均正确的是( )
选项
物质
所选试剂及操作方法
A
Cu(CuO)
通入氧气并加热
B
CO2(HCl)
气体通过盛有足量氢氧化钠溶液的洗气瓶
C
N2(O2)
气体通过炽热的铜粉
D
KCl溶液(K2CO3)
加入过量氯化钙溶液充分反应后过滤
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
尿素[CO(NH2)2]是一种常用的化肥,工业上生产尿素的反应的微观示意图如图所示:
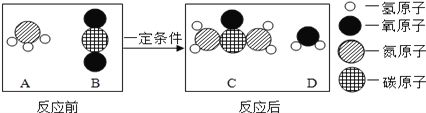
则下列说法正确的是( )
A. 图中A、B、D三种物质都是氧化物
B. 该反应属于复分解反应
C. 该反应前后分子种类、原子种类均没有改变
D. 反应中A、B物质的质量比为17:22
难度: 中等查看答案及解析
-
豆浆被称为“植物奶”,其中含有的异黄酮(C15H10O2)具有防癌功能。下列关于异黄酮的说法正确的是( )
A. 异黄酮中共含有27个原子
B. 1个异黄酮分子中含有1个氧分子
C. 异黄酮中碳元素的质量分数最大
D. 异黄酮中C、H、O三种元素的质量比为15:10:2
难度: 简单查看答案及解析
-
下列四个图像中,能正确反映对应变化关系的是
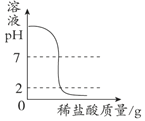
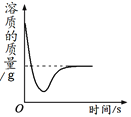
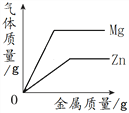
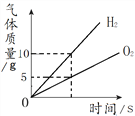
A.向一定量的氢氧化钠溶液中逐滴加入pH=2的稀盐酸至过量
B.某温度时,向一定量的饱和石灰水中加入少量生石灰
C.向两份完全相同的稀盐酸中分别加入锌粉、镁粉
D.将水通电一段时间
A. A B. B C. C D. D
难度: 困难查看答案及解析









