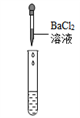
-
下列说法正确的是
A. 中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B. 分子、原子都是不带电的粒子,但是不带电的粒子不一定是分子、原子
C. 碱性溶液能使紫色石蕊溶液变蓝,但能使紫色石蕊溶液变蓝的不一定是碱溶液
D. 为促进植物生长,增强农作物的抗寒、抗旱能力,应该施用氮肥
难度: 困难查看答案及解析
-
下列变化中不涉及化学变化的是( )
A.金刚石刀切割玻璃 B.用粮食发酵酿酒
C.生石灰吸水变成粉末 D.铁矿石在高炉中炼铁
难度: 简单查看答案及解析
-
食品添加剂溴酸钾(KBrO3)会致癌,已被禁用,其中溴元素(Br)的化合价为( )
A.+1 B.+3 C.+5 D.无法确定
难度: 简单查看答案及解析
-
某同学用如图所示装置探究可燃物燃烧的条件,得到以下实验事实:①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧。能证明可燃物必须达到一定温度(着火点)才能燃烧的实验事实是
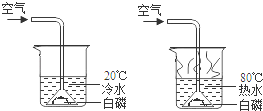
A.①② B.②④ C.①④ D.③④
难度: 困难查看答案及解析
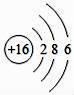
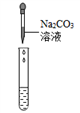
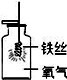 B. 检查装置气密性
B. 检查装置气密性
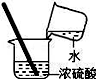
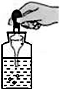 D. 稀释浓硫酸
D. 稀释浓硫酸