-
若把周期表原先的主、副族号取消,由左到右按原顺序编为18列。如碱金属为第1列,稀有气体为第18列,按这个规定,下列说法不正确的是( )
A. 第3列元素种类最多,第14列元素的化合物种类最多
B. 第10列元素全部是金属元素
C. 第18列元素单质全部是气体
D. 只有第2列元素的原子最外层有2个电子
难度: 简单查看答案及解析
-
1999年1月,俄美科学家联合小组宣布合成出114号元素的一种同位素,该同位素原子的质量数为298。以下叙述不正确的是( )
A. 该元素属于第七周期 B. 该元素为金属元素,性质与82Pb相似
C. 该元素位于ⅢA族 D. 该同位素原子含有114个电子,184个中子
难度: 简单查看答案及解析
-
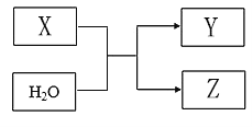
W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X可生成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z原子最外层的电子数与W的电子总数相同。下列叙述正确的是
A. X与其他三种元素均可形成两种或两种以上的二元化合物
B. Y与其他三种元素分别形成的化合物中只含有离子键
C. 四种元素的简单离子具有相同的电子层结构
D. W的氧化物对应的水化物均为强酸
难度: 中等查看答案及解析
-
下列说法正确的有几句( )
①离子键与共价键的本质都是静电作用;②任何物质中都存在化学键;③氢键是极弱的化学键;④离子键就是阴、阳离子之间的静电吸引力;⑤活泼金属与活泼非金属化合时能形成离子键;⑥任何共价键中,成键后原子均满足8电子稳定结构;⑦验证化合物是否为离子化合物的实验方法是可以看其熔化状态下能否导电;⑧两种非金属元素形成的化合物不可能含有离子键;⑨化学键断裂,一定发生化学变化
A. 1 B. 2 C. 3 D. 4
难度: 中等查看答案及解析
-
下列说法不正确的有几个( )
①质子数相同的微粒一定属于同一种元素
②同一元素的核素种数由中子数决定
③18gH2O中含有的中子数为10NA
④标准状况下,等体积CH4和HF所含的分子数相同
⑤通过化学变化可以实现16O与18O之间的相互转化
A.2个 B.3个 C.4个 D.5个
难度: 中等查看答案及解析
-
在盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的
A.腐蚀品
 B.易燃液体
B.易燃液体
C.剧毒品
 D.爆炸品
D.爆炸品
难度: 简单查看答案及解析
-
下列粒子结构示意图中,表示具有稳定结构的原子是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述不正确的是
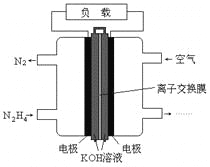
A.电流从右侧电极经过负载后流向左侧电极
B.负极发生的电极反应式为N2H4+4OH--4e-=N2+4H2O
C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极 表面的吸附量,并使它们与电解质溶液充分接触
D.该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
难度: 中等查看答案及解析
-
下列物质中,既含有离子键又含有非极性共价键的是( )
A.HClO B.Ba(OH)2 C.Na2O2 D.Ar
难度: 中等查看答案及解析
-
实验是化学研究的基础,关于下列各实验装置图的叙述正确的是( )
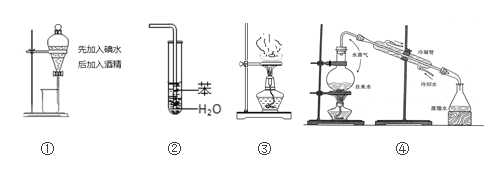
A.装置①中溶液上层无色,下层紫红色 B.装置②可用于吸收SO2气体,并防止倒吸
C.装置③中液体蒸干后停止加热 D.装置④可用于制取蒸馏水
难度: 简单查看答案及解析
-
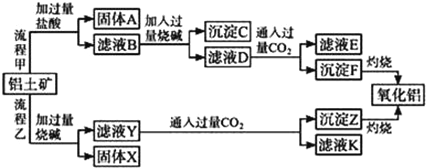
镭是周期表中第7周期第ⅡA主族元素,下列关于镭的性质描述中不正确的是( )
A.在化合物中呈+2价 B.镭比钙的金属性强
C.氢氧化物呈两性 D.碳酸盐难溶于水
难度: 简单查看答案及解析
-
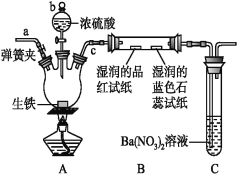
为了验证Fe3+的性质,某化学兴趣小组设计了下图所示的一组实验,其中实验方案设计错误的是( )

A.只有④ B.只有③
C.③和④均错误 D.全部错误
难度: 简单查看答案及解析
-
根据下列各反应,判断有关物质还原性由强到弱的顺序是
①H2SO3+I2+H2O=2HI+H2SO4
②2FeCl3+2HI=2FeCl2+2HCl+I2
③3FeCl2+4HNO3=2FeCl3+NO+2H2O+Fe(NO3)3
A.
B.
C.
D.
难度: 中等查看答案及解析
-
如图所示是部分短周期元素原子半径与原子序数的关系,则下列说法正确的是( )
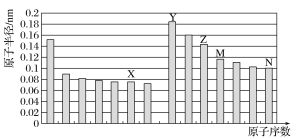
A.Z、N两种元素形成的化合物熔融状态下可以导电
B.X、N两种元素的气态氢化物的沸点相比,前者较低
C.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液中
D.由X与M两种元素组成的化合物能与水反应
难度: 中等查看答案及解析
-
五种短周期元素的某些性质如表所示(其中只有W、Y、Z为同周期元素)。下列说法正确的是 ( )
元素代号
X
W
Y
Z
Q
原子半径(×10-12m)
37
64
66
70
154
主要化合价
+1
-1
-2
+5、-3
+1
A.由Q与Y形成的化合物中只存在离子键
B.Z与X之间形成的化合物具有还原性
C.由X、Y、Z三种元素形成的化合物的水溶液呈碱性
D.W的最高正价为+7
难度: 中等查看答案及解析
-
胆矾(CuSO4•5H2O)高温时发生反应:2CuSO4•5H2O
2CuO + 2SO2↑+ O2↑+ 10H2O。下列装置能达到实验目的的是( )
A.
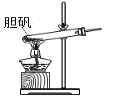 可用于胆矾分解 B.
可用于胆矾分解 B. 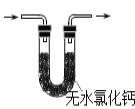 可用于检验产物是否含H2O
可用于检验产物是否含H2OC.
可用于收集SO2 D.
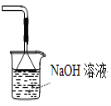 可用于吸收胆矾分解的SO2
可用于吸收胆矾分解的SO2难度: 中等查看答案及解析
-
下列有机物中,既能发生加成反应,又能发生酯化反应,还能被新制Cu(OH)2悬浊液氧化的物质是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列物质一定互为同系物的是
A.
和
B.
和
C.
和
D.
和
难度: 简单查看答案及解析
-
将足量的O2和NH3混合成448 mL,通过预先加热的催化剂三氧化二铬充分反应后,再通过足量的水,最终收集到44.8mL的无色气体。则原混合气体中O2的体积可能是(氨全部被氧化;气体体积均已换算成标准状况)( )
A.231.5 mL B.268.8 mL C.287.5 mL D.56 mL
难度: 中等查看答案及解析
-
向2.0 L 浓度均为1.0 mol·L−1 的 CuSO4、Fe2(SO4)3 和 H2SO4 的混合液中加入足量的铁粉,反应停止后,铁粉有剩余,此时溶液中 Fe2+ 的物质的量浓度是(溶液的体积变化忽略不计)( )
A.1.5 mol·L−1 B.2.0 mol·L−1 C.3.0 mol·L−1 D.5.0 mol·L−1
难度: 中等查看答案及解析