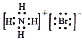-
下列有关多电子原子的叙述中正确的是( )
A.在一个多电子原子中,不可能有两个运动状态完全相同的电子
B.在一个多电子原子中,不可能有两个能量相同的电子
C.在一个多电子原子中,N层上的电子能量肯定比M层上的电子能量高
D.某个多电子原子的3p轨道上仅有两个电子,它们的自旋状态必须相反
-
化学与环境、材料、信息、能源关系密切,下列说法错误的是( )
A.低碳生活注重节能减排,减少温室气体的排放
B.推广使用可降解塑料及布质购物袋,以减少“白色污染”
C.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅
D.启用大气中细颗粒物(PM2.5)的监测,以追根溯源,采取措施,改善空气质量
-
下列有关化学用语的表示正确的是( )
A.质量数为37的氯原子: Cl
Cl
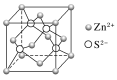
B.二氧化碳分子的比例模型:
C.NH4Br的电子式: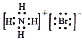
D.对羟基苯甲醛的结构简式:
-
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.含有0.1mol·L-1Fe3+的溶液中:K+、Mg2+、I-、SO42-
B.c(Al3+)=0.5mol·L-1的溶液中:Na+、K+、AlO2-、SO42-
C.能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl-
D.能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3-
-
下列说法错误的是( )
A.ns电子的能量可能低于(n-1)p电子的能量
B.6C的电子排布式1s22s22p ,违反了洪特规则
,违反了洪特规则
C.电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理
D.电子排布式(22Ti)1s22s22p63s23p10违反了泡利不相容原理
-
下列图示与对应的叙述相符的是( )
A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化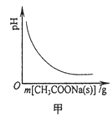
B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b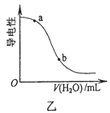
C.图丙表示催化剂能改变化学反应的焓变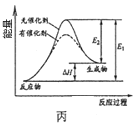
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0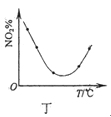
-
短周期主族元素X 、Y 、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价.下列说法正确的是( )
A.简单离子半径大小顺序:rW>rZ>rY
B.元素W的氧化物对应水化物的酸性比Y 的强
C.X与Y形成的原子晶体X3Y4的熔点可能比金刚石高
D.X与W形成的化合物和Z与W形成的化合物的化学键类型相同
-
下列有关说法正确的是( )
A.在轮船表面涂刷富锌油漆,能有效防止船体在海水中被腐蚀
B.0.1mol·L-1氨水加水稀释后,溶液中 的值减小
的值减小
C.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
D.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H>0
-
下列有关核外电子排布式或轨道表示式不正确的是( )
A.24Cr的电子排布式:1s22s22p63s23p63d54s1
B.K的原子实电子排布式:[Ar]4s1
C.N原子的轨道表示式为
D.S原子的轨道表示式为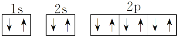

-
下表所列物质晶体的类型全部正确的一组是
| 晶体类型 | 原子晶体 | 离子晶体 | 分子晶体 |
| A. | 氮化硅 | 磷酸 | 单质硫 |
| B. | 单晶硅 | 碳酸氢铵 | 水银 |
| C. | 金刚石 | 烧碱 | 冰 |
| D. | 铁 | 尿素 | 冰醋酸 |
A.A B.B C.C D.D
-
下表为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是 ( )
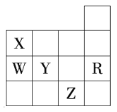
A.W、R元素单质分子内都存在非极性键
B.X、Z元素都能形成双原子分子
C.键长W—H<Y—H,键的极性Y—H>W—H
D.键长X—H<W—H,键能X—H<W—H
-
常温下,用0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1CH3COOH溶液的滴定曲线如图所示。下列说法正确的是

A.点①所示溶液中:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
B.点②所示溶液中:c(Na+)+c(H+)=c(CH3COO-) +c(CH3COOH) +c(OH-)
C.点③所示溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.在整个滴定过程中:溶液中 始终不变
始终不变