-
化学与生产、生活、材料密切相关,下列说法正确的是( )
A.新漆家具和装饰材料中含苯等有毒有机物
B.放置较久的红薯比新挖出土的甜,可能与葡萄糖的水解有关
C.酒精浓度越高,杀菌消毒效果越好
D.涤纶、棉花、蚕丝都是天然纤维
难度: 中等查看答案及解析
-
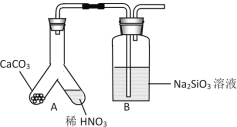
考古中常用
进行断代,这里的“6”是指该原子的( )
A.质子数 B.中子数 C.质量数 D.原子个数
难度: 简单查看答案及解析
-
物质发生化学变化时,一定发生变化的是( )
A.原子数 B.最外层电子数 C.质子数 D.化学键
难度: 简单查看答案及解析
-
下列物质的成分表示正确的是( )
A.水煤气——CH4 B.裂解气——C2H6
C.淀粉——(C6H10O5)n D.油脂——C17H35COOH
难度: 中等查看答案及解析
-
俄国科学家门捷列夫对化学的突出贡献在于( )
A.提出了元素周期律 B.提出化学元素的概念
C.提出氧化学说 D.提出原子学说
难度: 简单查看答案及解析
-
下列各组化合物中,化学键类型完全相同的是( )
A.NaCl和 H2S B.Na2O和 Na2O2
C.CO2 和SO2 D.HCl和 NaOH
难度: 简单查看答案及解析
-
下列实验过程中发生取代反应的是( )
A.乙烷与Cl2混合在光照条件下反应
B.乙烯使酸性KMnO4溶液褪色
C.十六烷催化加热得到辛烷和辛烯
D.将苯滴入溴水中,振荡后水层接近无色
难度: 简单查看答案及解析
-
下列事实能够说明元素X原子得电子能力比元素Y强的是( )
A.X原子得电子数目比元素Y多
B.对应氢化物水溶液的酸性:X>Y
C.对应阴离子的还原性:X>Y
D.相同条件下单质与铁反应,所得产物中铁的价态分别为+3价和+2价
难度: 简单查看答案及解析
-
番茄电池的示意图如图所示。电池工作时,下列有关说法错误的是( )

A.番茄内阳离子向Fe片移动
B.Zn片质量减少
C.Fe片极发生氧化反应
D.实现了化学能向电能的转化
难度: 简单查看答案及解析
-
下列属于放热反应的是( )
A.氯化铵固体与消石灰反应
B.C+CO2
2CO
C.2H2O
2H2↑+O2↑
D.铁粉与硫粉混合后加热
难度: 简单查看答案及解析
-
下列说法错误的是( )
A.乙烯的产量是衡量一个国家石油化工发展水平的标志
B.含碳元素的化合物都是有机化合物
C.蛋白质水解最终生成氨基酸
D.乙烯、苯分子中的所有原子在同一平面上
难度: 中等查看答案及解析
-
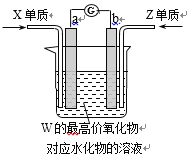
a、b、c、d四种金属片两两相连浸入稀硫酸中都可组成原电池。a、b相连时,a的质量减少;a、c相连时,阳离子移向c;b、d相连时,b上有气泡逸出;c、d相连时,外电路电流从d流向c。据此判断这四种金属活动性由大到小的顺序是( )
A.acbd B.acdb C.cdba D.cabd
难度: 简单查看答案及解析
-
下列化学用语表示正确的是( )
A.CO2电子式:
B.钾原子结构示意图:
C.甲烷分子球棍模型:
D.异丁烷结构简式:
难度: 简单查看答案及解析
-
X是形成化合物种类最多的元素,Y元素次外层电子数是最外层电子数的2倍,下列说法正确的是( )
A.X、Y一定是第2周期元素 B.X、Y一定是同一主族元素
C.X的原子半径可能比Y大 D.X的最高价氧化物对应的水化物为弱酸
难度: 中等查看答案及解析
-
下列有机化学方程式书写正确的是( )
A.H2C=CH2+Br2
CH3CHBr2
B.CH3CH2OH+Na
CH3CH2ONa+H2
C.
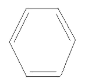 +HO-NO2
+HO-NO2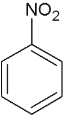 +H2O
+H2OD.nCH2=CH-CH3
难度: 中等查看答案及解析
-
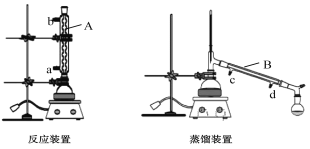
下列实验装置和对应的说法均正确的是( )
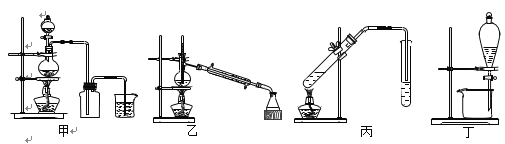
A.甲装置可制取干燥、纯净的Cl2
B.利用乙装置分离苯和四氯化碳
C.利用丙装置制取乙酸乙酯
D.丁装置用于酒精萃取碘水中的碘单质
难度: 中等查看答案及解析
-
以下反应不能设计成原电池的是( )
A.NaOH+HNO3 =NaNO3+H2O
B.CH4+2O2 = CO2+2H2O
C.Zn+H2SO4 = ZnSO4+H2↑
D.Fe+2FeCl3 =3FeCl2
难度: 中等查看答案及解析
-
下列有关有机物结构、性质的叙述正确的是( )
A.乙醇分子中含有氢氧根,可以与酸发生中和反应
B.乙酸乙酯中含有酯基,在酸性条件下可完全水解成羧酸和醇
C.肉桂酸(
)中含有羧基,可与乙醇发生酯化反应
D.苯中含有碳碳双键,能发生加成反应
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.所有主族中都有非金属元素
B.周期表中位于金属和非金属分界线附近的元素是过渡元素
C.ⅥA族元素的原子,其半径越大,越容易得到电子
D.同周期主族元素中,IA族元素的原子半径最大
难度: 中等查看答案及解析
-
下列说法错误的是( )
A.金刚石、石墨、C60互为同素异形体,氕、氘、氚互为同位素
B.甲烷和苯都不存在同分异构体
C.向鸡蛋清溶液中加饱和硫酸铵溶液,可见溶液变浑浊,加水后又溶解
D.乙烷和聚氯乙烯都不能使酸性KMnO4溶液褪色
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.单质分子中均存在化学键
B.元素周期表中共有18个纵列、18个族,第9纵列属于第Ⅷ族
C.向氢硫酸中通入Cl2,溶液变浑浊,证明非金属性Cl强于S
D.放热反应的速率一定比吸热反应的速率快
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
A.标准状况下,2.24L乙烷分子中含有的共价键的数目为0.6NA
B.常温常压下,28gCO和C2H4混合气体的分子数为NA
C.标准状况下,11.2LH2O分子中含有的电子数为5NA
D.10g46%乙醇水溶液与足量的钠反应转移电子数为0.1NA
难度: 中等查看答案及解析
-
在密闭容器中充入A2和B2,一定条件下发生反应A2+B2
2AB(正反应为吸热反应),其反应速率与时间的关系如图所示。

下列说法错误的是( )
A.t1时,v(正反应)>v(逆反应)
B.t2时,v(正反应) = v(逆反应)
C.图中虚线表示的转化是A2+B2→2AB
D.升高温度和加催化剂,均有利于加快反应速率
难度: 中等查看答案及解析
-
恒温恒容下反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),能说明反应达到平衡状态的是( )
A.混合气体中H2O的体积分数保持不变
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3 molH2,同时生成1 mol CH3OH
D.反应中CO2与CH3OH的物质的量浓度之比为1:1
难度: 简单查看答案及解析
-
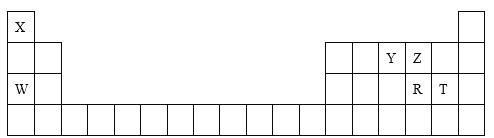
短周期主族元素X、Y、Z、W的原子序数依次增大,四种元素原子最外层电子数之和为20,X的最高正价与最低负价的代数和为2,Y与W同主族,同周期中Z离子的半径最小。下列说法错误的是( )
A.离子半径:Z<Y<W
B.由Y、Z组成的化合物可与氢氧化钠溶液反应
C.简单气态氢化物的稳定性:Y>W
D.X和W的氧化物对应的水化物,均是常见的强氧化剂
难度: 中等查看答案及解析